ADN plastídico
proteins
História e origem cloroplastidial
ADN plastídico, frequentemente abreviado para cpDNA,[1] é a designação dada em biologia molecular ao ADN presente nos cloroplastos das plantas.[2][3] Os cloroplastos são organelas responsáveis pela fotossíntese e parecidas às mitocôndrias em alguns aspectos. Ambos atuam na geração de energia metabólica, evoluíram por endossimbiose, possuem seu próprio sistema genético e reproduzem-se por divisão. Porém, os cloroplastos são maiores e mais complexos comparado com as mitocôndrias e executam outras tarefas críticas além da geração de ATP. Basicamente, os cloroplastos têm como principal função a conversão fotossintética do dióxido de carbono (CO2) em carboidratos. Além disso, participam da síntese de aminoácidos, ácidos graxos e de componentes lipídicos que compõem suas próprias membranas. Nos cloroplastos, também, acontece a redução do nitrito (NO2-) em amônia (NH3), uma etapa essencial na incorporação do nitrogênio em compostos orgânicos. Além disso, os cloroplastos representam apenas um dos vários tipos de organelas relacionadas aos plastídeos (família de organelas de plantas incluindo cloroplastos, cromoplastos, leucoplastos, amiloplastos e elaioplastos) que desempenham um amplo espectro de funções nas células vegetais (Hausman, 2007). No atual momento, a teoria mais amplamente aceita para a origem das mitocôndrias e dos cloroplastos é a teoria endossimbiótica. Em 1883, Andreas Schimper foi um dos primeiros a propor a possível natureza endossimbiótica das células eucarióticas, observando que a divisão dos cloroplastos das plantas era parecida com a das cianobactérias de vida livre. Konstantin Mereschkowsky em 1905 sugeriu a ideia da origem endossimbiótica dos plastídios. E em 1927, e em conjunto com Ivan Wallin, propôs que a célula eucariota fosse composta por microrganismos, hipótese rejeitada pela comunidade científica na época.
Entretanto, após quarenta anos, Lynn Margulis (então Lynn Sagan) publicou o artigo de "On the origin of mitosing cells” (Sobre a Origem das Células em Mitose) em 1967 no Journal of Theoretical Biology, levantando a hipótese de que as mitocôndrias e os plastídeos fotossintéticos já foram células de vida livre (procarióticas) (Sampaio, 2022; Sagan L, 1967; Gray, 2017).
Atualmente, existe um consenso geral que mitocôndrias e cloroplastos tiveram origem de ancestrais comuns, respetivamente, das bactérias α-púrpura (primeiro evento de endossimbiose) e das Cianobactérias (evento seguinte e restrito ao ancestral dos eucariotas fotossintéticos). Essa conclusão baseia-se principalmente na análise dos genomas mitocondrial e plastidial, dos quais permitem determinar com elevado grau de certeza a origem evolutiva dessas organelas (Sampaio, 2022).
Em 1962 os pesquisadores Hans Ris e Walter Plaut examinaram por microscopia eletrônica e métodos citoquímicos a presença de DNA nos cloroplastos de Chlamydomonas moewusii. Tanto a reação de Feulgen quanto a coloração com laranja de acridina indicaram a presença, dentro do cloroplasto, de um ou mais corpos contendo DNA com formato irregular (Sampaio, 2022; Ris. H e Plaut. W, 1962).
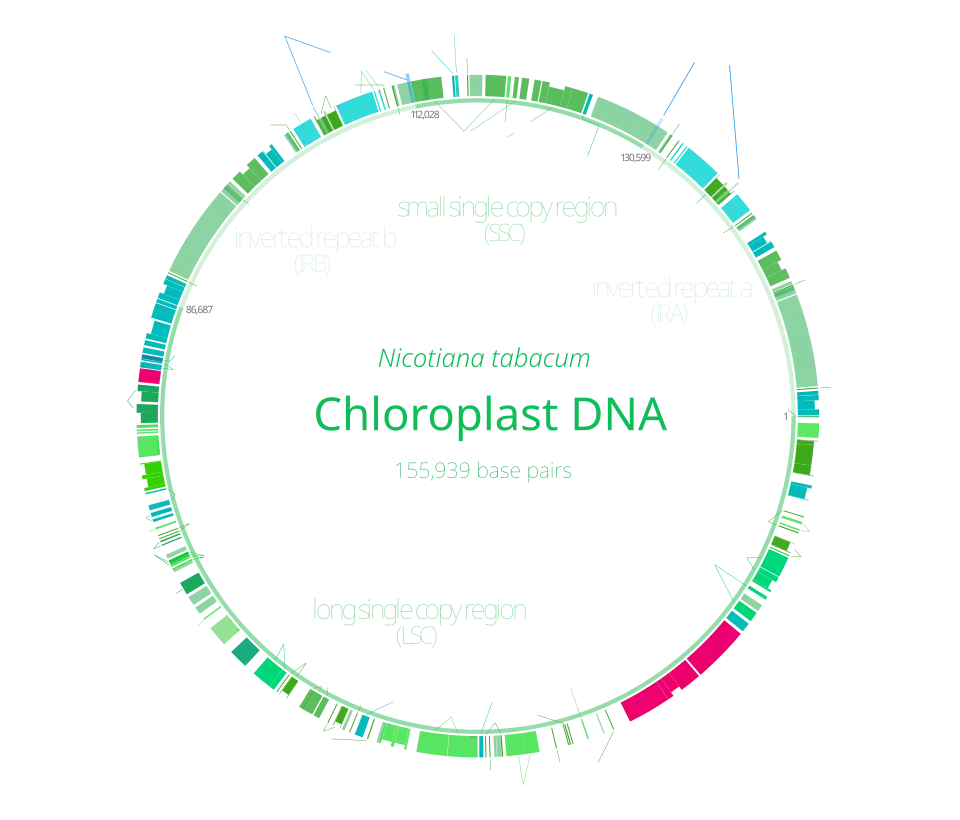
Além disso, em 1986 foi analisada a primeira sequência completa de nucleotídeos de genomas de plastídeos pelo Katzuo Shinozaki (Nagoya, Japão) com cloroplastos de tabaco e por Kanji Ohyama (Quioto, Japão) com cloroplastos da hepática Marchantia polymorpha. Embora as duas plantas investigadas sejam muito distantemente relacionadas, seus genomas de plastídeos são bastante semelhantes em composição e organização gênica (Shinozaki K et al., 1986; Heldt HW, 2021)
Funções genéticas e plastidiais
O DNA cloroplastidial, também chamado genoma plastidial, representa um remanescente da endossimbiose entre uma célula eucariótica ancestral e uma cianobactéria, preservando assim, parte de sua autonomia metabólica (KEELING, 2010). Apesar de reduzido, esse genoma contém genes essenciais para fotossíntese, expressão gênica e biogênese plastidial, refletindo tanto sua origem bacteriana quanto sua integração ao metabolismo celular da planta (BOCK, 2017; GREEN, 2011).
Funções genéticas e biologia do plastídeo
Os plastídeos constituem um grupo de organelas essenciais das células vegetais e de alguns protistas fotossintetizantes, sendo os cloroplastos os representantes mais conhecidos. Eles desempenham papéis fundamentais na fotossíntese, no metabolismo primário, na biossíntese de aminoácidos, lipídios e pigmentos, além de participarem de respostas ao estresse e da regulação do desenvolvimento vegetal. A complexidade funcional dos plastídeos é sustentada por seu próprio genoma — o DNA plastidial (ptDNA) —, embora a maior parte das proteínas plastidiais seja codificada pelo núcleo da célula. Assim, a biologia dos plastídeos envolve uma intrincada rede de cooperação gênica entre o genoma organelar e o genoma nuclear.
Quais genes estão tipicamente no DNA plastidial
O genoma plastidial de plantas vasculares é relativamente conservado, com 120–160 kb, e organiza-se em três grandes grupos funcionais (SUGIURA, 2014).
Genes relacionados à fotossíntese
Incluem genes das subunidades dos fotossistemas I e II (psaA, psbA, entre outros), do complexo citocromo b6f (petA, petB) e da ATP sintase (atpA, atpB). O gene rbcL, que codifica a subunidade grande da Rubisco, também está presente (DANIELL et al., 2016). Esses genes garantem a manutenção das reações fotoquímicas e da fixação de carbono.
Genes relacionados à expressão gênica plastidial
O DNA plastidial conserva genes que codificam parte de sua própria maquinaria transcricional e traducional, como as subunidades da RNA polimerase bacteriana — rpoA, rpoB, rpoC1, rpoC2 — além de genes associados à replicação e maturação de RNA (ZOSCHKE; BÖRNER, 2017). A persistência desses genes é crucial para a regulação local da síntese de proteínas envolvidas na fotossíntese (JARVIS; LÓPEZ-JUEZ, 2013).
Genes de rRNAs e tRNAs
O genoma plastidial codifica rRNAs essenciais (16S, 23S, 4.5S e 5S) e entre 30 e 37 tRNAs que permitem ao plastídeo manter um sistema de tradução independente, semelhante ao ribossomo 70S bacteriano (GREEN, 2011; BOCK, 2017).
Relação funcional entre genoma plastidial e núcleo (transferência gênica, coordenação gênica).
A grande maioria das proteínas plastidiais — cerca de 90–95% — é codificada pelo núcleo, evidenciando uma relação de forte dependência funcional (DANIELL et al., 2016). Essa dependência é consequência de um intenso processo de transferência gênica endossimbiótica, no qual genes originalmente plastidiais migraram para o núcleo ao longo da evolução, adquirindo peptídeos de trânsito que direcionam suas proteínas de volta ao plastídeo (KEELING, 2010).
Transferência gênica
A realocação de genes para o genoma nuclear aumentou a estabilidade do genoma plastidial e permitiu maior controle regulatório por parte da célula hospedeira (BOCK et al., 2017).
Coordenação da expressão gênica
A comunicação entre núcleo e plastídeo ocorre por:
- sinalização anterógrada, na qual o núcleo regula a expressão plastidial conforme necessidades metabólicas e condições ambientais;
- sinalização retrógrada, na qual o plastídeo envia sinais ao núcleo sobre seu estado funcional, ajustando a expressão de genes nucleares essenciais para sua biogênese (WOODSON; CHORY, 2008).
Essa coordenação garante que subunidades nucleares e plastidiais dos complexos fotossintéticos sejam produzidas de forma sincronizada (JARVIS; LÓPEZ-JUEZ, 2013).
Implicações genéticas (por exemplo, herança materna/plastidial nas plantas).
Herança materna
Em angiospermas, o DNA plastidial é geralmente herdado apenas pela linhagem materna, já que os gametas masculinos raramente contribuem plastídeos ao zigoto (NEUHAUS; EMES, 2000). Isso gera padrões de herança não mendelianos, relevantes em genética vegetal.
Variegamento e segregação citoplasmática
Mutação no DNA plastidial pode gerar fenótipos como variegamento foliar, decorrente da segregação estocástica dos plastídeos durante a divisão celular (BOCK et al., 2017).
Regulação gênica cloroplastidial
Análises genômicas cloroplastidiais permitem a afirmação de que o seu DNA é composto por aproximadamente 120 à 130 genes, incluindo codificadores de rRNAs, tRNAs e peptídeos não identificados (LINDHOLM et al., 1992). O controle dos processos que permitem a expressão desses genes, isto é, a replicação, a transcrição e a tradução dentro dos cloroplastos, pode ser chamado regulação gênica. Em decorrência da sua origem endossimbiótica, muitos genes cloroplastidiais estão organizados em um arranjo genômico chamado operons – grupos de genes adjacentes que são co-transcritos em mRNAs policistrônicos –, resultando em mecanismos moleculares de regulação gênica diferentes do padrão de expressão gênica nuclear, que, por sua vez, fornecem evidências adicionais a favor da origem procariótica dos cloroplastos. (BOCK et al., 2000).
A regulação dos genes cloroplastidiais envolve mecanismos que atuam em níveis transcricionais, pós-transcricionais, traducionais e pós-traducionais, geralmente relacionados a fatores intra e extra-plastidiais, esses mecanismos são responsáveis pela interação genética entre o núcleo, a mitocôndria e o plastídeo (LEISTER et al., 2005). A interação entre o cloroplasto e o núcleo, por exemplo, é evidenciada por mecanismos moleculares de várias fases da expressão gênica, como a regulação da RNA-polimerase codificada por genes plastidiais (HAJDUKIEWICZ et al., 1997).
Um exemplo de regulação gênica característico de cloroplastos é a edição de RNA, que ocorre na etapa pós-transcricional, essa edição do mRNA em plastídeos ocorre no gene rpl2 de Zea mays e outras espécies vegetais superiores, nela, uma base nitrogenada (C) é substituída por outra (U), no transcrito primário (BOCK et al., 1997). O editamento de RNA dos cloroplastos é um mecanismo adicional que atua no controle da síntese de produtos gênicos funcionais, que pode cancelar ou corrigir desvios do código genético universal. (LINDHOLM et al., 1992).
Aplicações e importância
A configuração simplificada do genoma plastidial (120 genes organizados de forma circular) permite aos cientistas selecionar exatamente em que ponto do código genético irão introduzir o novo gene. As extremidades dos fragmentos de DNA apresentam sequências regulatórias que garantem que o gene só será expresso se estiver inserido no cloroplasto. (Carrer, 2011).
Outra aplicabilidade está relacionada à alta capacidade de produção de proteínas. Quando um gene é introduzido no cloroplasto, a planta consegue produzir a proteína correspondente e em altas quantidades. Isso ocorre porque cada célula vegetal possui, em torno de 10 a 100 cloroplastos, e cada cloroplasto tem de 10 a 100 cópias desse genoma. Isso nos mostra que as células podem ter de 1.000 a 10.000 cópias do genoma do cloroplasto, potencializando a produção da proteína desejada.O cloroplasto pode ser responsável por até 40% da produção total de proteínas pela célula. (Bock; Carrer, 2011).
Adicionalmente, as alterações nos genes do cloroplasto não são transmitidas pelo pólen, que não contém cloroplastos. Isso pode ser vantajoso em algumas situações, pois evita que as modificações genéticas se espalhem para outras plantas de forma descontrolada.
Estudos de DNA cloroplastidial podem ser utilizados em várias áreas da biologia de plantas como em estudos evolutivos e filogenéticos (estabelecer relações filogenéticas entre espécies, gêneros e famílias), busca da base genética de doenças, clonagem gênica e reprodução, contribuindo para a expansão das pesquisas botânicas e agronômicas. Além disso, o sequenciamento de genoma plastidial revela características específicas de cada grupo de planta e de seu funcionamento, os quais podem ser amplamente aplicados através de técnicas da biotecnologia. (Amorim, M.R.C., Martins, L.O & Caldeira, A.J.R., 2021).
Notas
- ↑ Sakamoto, W; Takami, T (1 de junho de 2018). «Chloroplast DNA Dynamics: Copy Number, Quality Control and Degradation.». Plant & cell physiology. 59 (6): 1120-1127. PMID 29860378. doi:10.1093/pcp/pcy084
- ↑ de Vries, Jan; Archibald, John M. (abril de 2018). «Plastid genomes». Current Biology. 28 (8): R336–R337. doi:10.1016/j.cub.2018.01.027
- ↑ C.Michael Hogan. 2010. Deoxyribonucleic acid. Encyclopedia of Earth. National Council for Science and the Environment. eds. S.Draggan and C.Cleveland. Washington DC
Demais referências
Cooper GM, Hausman RE. A célula: uma abordagem molecular. 3ª ed. Porto Alegre: ArtMed; 2007. e-book. p. 408. ISBN: 9788536310985. Disponível em: https://app.minhabiblioteca.com.br/reader/books/9788536310985/. Acesso em: 1 out. 2025.
Ris H, Plaut W. Ultrastructure of DNA-containing areas in the chloroplast of Chlamydomonas. J Cell Biol. 1962;13(3):383–91. doi:10.1083/jcb.13.3.383.
Sampaio AC. Cianobactérias. Rev Ciênc Elem. 2022;10(2):022. doi:10.24927/rce2022.022.
Sagan L. On the origin of mitosing cells. J Theor Biol. 1967;14(3):225–74. doi:10.1016/0022-5193(67)90079-3.
Shinozaki K, Ohme M, Tanaka M, Wakasugi T, Hayashida N, Matsubayashi T, Zaita N, Chunwongse J, Obokata J, Yamaguchi-Shinozaki K, Ohto C, Torazawa K, Meng BY, Sugita M, Deno H, Kamogashira T, Yamada K, Kusuda J, Takaiwa F, et al. The complete nucleotide sequence of the tobacco chloroplast genome: its gene organization and expression. EMBO J. 1986;5(9):2043–9. doi:10.1002/j.1460-2075.1986.tb04464.x.
Heldt HW, Piechulla B, editors. Plant biochemistry. 5th ed. London: Academic Press; 2021. p. 469–501. doi:10.1016/B978-0-12-818631-2.00020-9.
Gray MW. Lynn Margulis and the endosymbiont hypothesis: 50 years later. Mol Biol Cell. 2017;28(10):1285–7. doi:10.1091/mbc.e16-07-0509.
BOCK, R. Structure, function, and inheritance of plastid genomes. In: BOCK, R.; KNOOP, V. (org.). Genomics of Chloroplasts and Mitochondria. Dordrecht: Springer, 2017. p. 1-40. Disponível em: https://link.springer.com/book/10.1007/978-3-319-63726-2. Acesso em:30 out 2025.
DANIELL, H.; LIN, C.-S.; YU, M.; CHANG, W.-J. Chloroplast genomes: diversity, evolution, and applications in genetic engineering. Genome Biology, v. 17, n. 134, p. 1-29, 2016. DOI: 10.1186/s13059-016-1004-2. Disponível em: https://genomebiology.biomedcentral.com/articles/10.1186/s13059-016-1004-2. Acesso em: 01 nov 2025. BioMed Central+1
GREEN, B. R. Chloroplast genomes of photosynthetic eukaryotes. The Plant Journal, v. 66, n. 1, p. 34-44, 2011. Disponível em: [acesso via Wiley Online Library] (link institucional). Acesso em: 10 out 2025.
JARVIS, P.; LÓPEZ-JUEZ, E. Biogenesis and homeostasis of chloroplasts and other plastids. Nature Reviews Molecular Cell Biology, v. 14, p. 787-802, 2013. Disponível em: https://www.nature.com/articles/nrm3641. Acesso em: 3 nov 2025.
KEELING, P. J. The endosymbiotic origin, diversification and fate of plastids. Philosophical Transactions of the Royal Society B, v. 365, n. 1541, p. 729-748, 2010. Disponível em: https://royalsocietypublishing.org/doi/10.1098/rstb.2009.0103. Acesso em: 01 out 2025.
NEUHAUS, H. E.; EMES, M. J. Non-photosynthetic metabolism in plastids. Annual Review of Plant Physiology and Plant Molecular Biology, v. 51, p. 111-140, 2000. Disponível em: https://www.annualreviews.org/doi/10.1146/annurev.arplant.51.1.111. Acesso em: 6 nov 2025.
SUGIURA, M. History of chloroplast genomics. Photosynthesis Research, v. 120, n. 1-2, p. 361-369, 2014. Disponível em: https://link.springer.com/article/10.1007/s11120-014-0039-9. Acesso em: 29 out 2025.
WOODSON, J. D.; CHORY, J. Coordination of gene expression between organellar and nuclear genomes. Nature Reviews Genetics, v. 9, p. 383-395, 2008. Disponível em: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4854206/. Acesso em: 04 nov 2025.
ZOSCHKE, R.; BÖRNER, T. Transcription, translation and replication in chloroplasts. In: BOCK, R.; KNOOP, V. (org.). Genomics of Chloroplasts and Mitochondria. Dordrecht: Springer, 2017. p. 195-231. Disponível em: https://link.springer.com/chapter/10.1007/978-3-319-63726-2_8. Acesso em: 5 out 2025.
BOCK, R.; ALBERTAZZI, F.; FREYER, R.; FUCHS, S.; RUF, S.; ZELTZ, P.; MAIER, R.M. Transcript editing in chloroplasts of higher plants. In: International Colloquium on Endocytobiology and Symbiosis proceedings, Eukaryotism and symbiosis: Berlin: Springer, 1997. p. 123–137.
HAGER, M.; BOCK, R. Enslaved bacteria as new hope for plant biotechnologists. Applied microbiology and biotechnology, v. 54, n. 3, p. 302-310, 2000.
LINDHOLM, J.A. The chloroplast genome of Pinus contorta Dough.: Studies of structure, rearrangements and gene content. University of Umea, Sweden, 1992.
DOS INVENTORES, Blog. Manipulação do DNA do Cloroplasto das Plantas. Disponível em: <https://inventores.com.br/manipulacao-do-dna-do-cloroplasto-das-plantas/>. Acesso em: 9 nov. 2025.
Amorim , M. R. C. Martins, L. O. ., & Caldeira, A. J. R. . (2021). ORIGEM E IMPORTÂNCIA FILOGENÉTICA DO CPDNA. Revista Multidisciplinar Em Saúde, 2(3), 06. https://doi.org/10.51161/rems/1946
Matsushima, R., et al. Chloroplast DNA Dynamics: Copy Number, Quality Control and Degradation(2018). Plant and Cell Physiology. [Ref 1.1 1.5 e 1.9]