Ferrato de potássio
Ferrato de potássio
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||
 | |||||||||||||||
| Nomes | |||||||||||||||
| Nome IUPAC | Ferrato de potássio(VI) | ||||||||||||||
| Outros nomes | Ferrato de potássio Ferrato de dipotássio | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
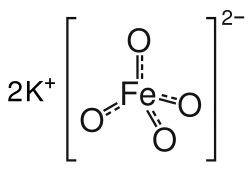
O ferrato de potássio é um sal roxo de fórmula K₂FeO₄. Na maioria dos compostos de ferro, este elemento se apresenta com estados de oxidação +2 e +3, porém, neste sal, o ferro se encontra no estado de oxidação +6, sendo considerado raro. Devido a este alto estado de oxidação, o íon ferrato é altamente oxidante.
O ferrato de potássio atrai a atenção da Química Verde — ramo da Química que pretende diminuir ou eliminar o uso de substâncias que promovem poluição, e recuperar a qualidade do meio ambiente — pois o seu produto secundário, óxido de ferro (FeO), não é nocivo ao meio ambiente. A dificuldade no seu uso ocorre por este óxido ser muito reativo e se decompor facilmente em água, como demonstra a equação abaixo:
4 K₂FeO₄ + 4 H₂O → 3 O₂ + 2 Fe₂O₃ + 8 KOH
Síntese e estrutura
Georg Emst Stahl (1660–1734) foi o primeiro a descobrir que o resíduo deixado pela reação entre nitrato de potássio (KNO₃) e pó de ferro, resultava em uma solução de cor roxa. Edmond Frémy (1814–1894) mais tarde descobriu que a fusão de hidróxido de potássio com óxido de ferro (III) na presença de ar, produzia um composto que era solúvel na água. A composição correspondia àquela do permanganato de potássio.
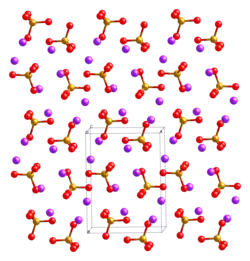
No laboratório, ferrato de potássio é preparado pela oxidação de uma solução alcalina de algum sal de ferro (III), com uma solução concentrada de hipoclorito de sódio (NaClO) . O ferrato de potássio (K₂FeO₄) é isoestrutural (tem estrutura análoga, possuindo um ânion em comum) com manganato de potássio (KMnO₄), sulfato de potássio (K₂SO₄) e cromato de potássio (K₂CrO₄). Possui cátions K+ e ânions FeO₄2- tetraédricos, com a ligação Fe-O possuindo distância de 1,66 Å [4].
Propriedades e aplicações
- Decomposição: sua rapidez de decomposição depende da faixa de pH do meio: em soluções com pH alto é estável, em pH neutro se decompõe rápido e decompõe-se mais rápido ainda em pH baixo.
- Cor: a solução deste sal apresenta cor roxa, semelhante à do permanganato de potássio.
- Agente oxidante: como agente oxidante, é mais forte que o permanganato de potássio.
- O ferrato de potássio tem sido descrito como “oxidante verde”, pois os subprodutos de suas reações redox são óxidos de ferro de caráter ferruginoso. Devido a essa característica esse sal empregou-se no tratamento de esgoto, como oxidante para contaminantes orgânicos e biocida. Afortunadamente, o produto resultante da reação é óxido-hidróxido de ferro (III), um excelente floculante.
- Em síntese orgânica, o ferrato de potássio oxida alcoóis primários.
- O ferrato de potássio também atrai atenção pela sua capacidade de ser um potencial material para o cátodo em uma “super bateria de ferro”.
Referências
- ↑ Catálogo da Sigma-Aldrich, Ferrato de potássio, consultado em 6 de abril de 2011
| Parte ou a totalidade desta página foi traduzida a partir de «en:Potassium ferrate» da Wikipédia noutra língua em 2011-12-16. |