Fenilpiperazina
Fenilpiperazina
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||
 | |||||||||||||||||
| Nomes | |||||||||||||||||
| Outros nomes | 1-Fenilpiperazina | ||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| Página de dados suplementares | |||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||
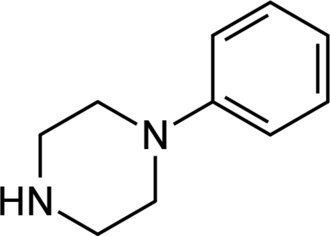
1-Fenilpiperazina (1-PP ou PP) é um composto químico e uma droga que apresenta um grupo fenil ligado a um anel de piperazina.[1] O sufixo '-piprazol' é, por vezes, utilizado em nomes de fármacos para indicar que pertencem a essa classe.[2]
É um análogo rígido da anfetamina.[1][3][4] De forma semelhante à anfetamina, a 1-PP é um agente de liberação de monoamina, com valores de concentração de metade do efeito máximo (EC50) para a liberação de monoaminas de 186 nM para noradrenalina, 880 nM para serotonina e 2.530 nM para dopamina.[1] Com base nesses, é cerca de 4,7 vezes menos potente na liberação de serotonina do que a noradrenalina e cerca de 13,6 vezes menos potente na liberação de dopamina do que a noradrenalina.[1] Assim, a 1-PP é um agente de liberação de noradrenalina (NRA) moderadamente seletivo, podendo também ser classificada como um agente de liberação de serotonina e noradrenalina [en] (SNRA) ou um agente de liberação de serotonina-noradrenalina-dopamina (SNDRA).[1]
A 1-Fenilpiperazina apresenta toxicidade em doses altas; com uma DL50 oral de 210 mg/kg em ratos.[5]
Existem vários derivados da 1-PP, também chamados de fenilpiperazinas substituídas [en].[6][1] Alguns exemplos são meta-clorofenilpiperazina (mCPP), 3-trifluorometilfenilpiperazina (TFMPP) e para-metoxifenilpiperazina (pMeOPP).[6][1][7]
Ver também
Referências
- ↑ a b c d e f g Severinsen K, Kraft JF, Koldsø H, Vinberg KA, Rothman RB, Partilla JS, Wiborg O, Blough B, Schiøtt B, Sinning S (setembro de 2012). «Binding of the amphetamine-like 1-phenyl-piperazine to monoamine transporters». ACS Chem Neurosci. 3 (9): 693–705. PMC 3447394
 . PMID 23019496. doi:10.1021/cn300040f
. PMID 23019496. doi:10.1021/cn300040f
- ↑ World Health Organization (WHO) (2006). «The use of stems in the selection of International Nonproprietary Names (INN) for pharmaceutical substances» (PDF). Consultado em 27 de abril de 2010. Cópia arquivada (PDF) em 14 de dezembro de 2008
- ↑ Oberlender R, Nichols DE (março de 1991). «Structural variation and (+)-amphetamine-like discriminative stimulus properties». Pharmacology, Biochemistry, and Behavior. 38 (3): 581–586. PMID 2068194. doi:10.1016/0091-3057(91)90017-V
- ↑ Glennon RA, Young R, Hauck AE, McKenney JD (dezembro de 1984). «Structure-activity studies on amphetamine analogs using drug discrimination methodology». Pharmacol Biochem Behav. 21 (6): 895–901. PMID 6522418. doi:10.1016/s0091-3057(84)80071-4
- ↑ «1-Phenylpiperazine». pubchem.ncbi.nlm.nih.gov
- ↑ a b Elliott S (2011). «Current awareness of piperazines: pharmacology and toxicology». Drug Test Anal. 3 (7-8): 430–438. PMID 21744514. doi:10.1002/dta.307
- ↑ Baumann MH, Clark RD, Budzynski AG, Partilla JS, Blough BE, Rothman RB (outubro de 2004). «Effects of "Legal X" piperazine analogs on dopamine and serotonin release in rat brain». Ann N Y Acad Sci. 1025: 189–197. PMID 15542717. doi:10.1196/annals.1316.024