Eunicidae
Eunicidae
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ocorrência: Ordoviciano–recente | |||||||||||||
| Classificação científica | |||||||||||||
| |||||||||||||



Eunicidae é uma família de poliquetas marinhos. A família compreende anelídeos marinhos distribuídos em diversos habitats bentônicos na Oceania, Europa, América do Sul, América do Norte, Ásia e África.[1] A anatomia típica inclui um par de apêndices próximos à boca (mandíbulas) e conjuntos complexos de estruturas musculares na cabeça (ossos maxilares) em uma faringe eversível.[2] Um dos mais notáveis é o gigante, de coloração roxo-escura iridescente, conhecido como "verme Bobbit" (Eunice aphroditois), encontrado em marés baixas sob rochas em praias do sul da Austrália. Seu corpo robusto e musculoso pode atingir até 2 m de comprimento.[3] Mandíbulas de Eunicidae são conhecidas desde sedimentos do Ordoviciano.[4][5] A tradição cultural envolve os ciclos reprodutivos de Palola viridis nas ilhas do Pacífico Sul.[6] Os membros de Eunicidae têm valor econômico como isca na pesca recreativa e comercial.[7][8] A criação comercial de Eunicidae pode causar impactos ecológicos negativos.[9] A extração pode reduzir as populações de vermes e da fauna associada,[10] danificar ambientes entremarés locais[11] e introduzir espécies nos ecossistemas aquáticos locais.[12]
Em 2020, Zanol e colegas afirmaram: "Espécies tradicionalmente consideradas pertencentes a Eunice agora também são distribuídas em dois outros gêneros, Leodice e Nicidion, recentemente ressuscitados para reconciliar a taxonomia de Eunicidae com sua hipótese filogenética".[13]
História do conhecimento
Em 1992, Kristian Fauchald detalhou uma história conclusiva da pesquisa e classificação da família Eunicidae.[4] Estudos primários realizados em 1767 em recifes de coral na Noruega classificaram inicialmente espécies de Eunicidae no gênero Nereis [en].[4] Em 1817, Georges Cuvier criou um novo gênero, Eunice, para classificar esses e outros táxons originais.[4] Ao longo do século XIX (1832–1878), espécies foram adicionadas a esse gênero por Jean Victor Audouin e Henri Milne-Edwards, Kinberg, Edwardsia de Quatrefages, Malmgren, Ehlers e Grube.[4] Após as expedições Challenger e Albatross [en], a pesquisa foi ampliada por McIntosh e Chamberlain.[4] Em 1921 e 1922, Treadwell adicionou novas espécies de recifes de coral no mar do Caribe e no oceano Pacífico.[4] As espécies foram revisadas e suas classificações refinadas por Fauvel, Augener e Hartman no início do século XX.[4] Em 1944, Hartman codificou um sistema de classificação separado para a família, agrupando informalmente espécies norte-americanas usando as sugestões originais de Ehlers.[4] O sistema de Hartman foi expandido e especificado por Fauchald em 1970 e posteriormente por Miura em 1986.[4]
Taxonomia
Trinta e três gêneros foram descritos na família Eunicidae.[14][15] Atualmente, apenas doze são considerados válidos:[16]
- Aciculomarphysa (Hartmann-Schroeder, 1998 em Hartmann-Schroder & Zibrowius 1998)
- †Esconites [en] Thompson & Johnson, 1977
- Eunice (Cuvier, 1817)
- Euniphysa (Wesenberg-Lund, 1949)
- Fauchaldius (Carrera-Parra & Salazar-Vallejo, 1998)
- Leodice Lamarck, 1818
- Lysidice [en] (Lamarck, 1818)
- Marphysa [en] (Quatrefages, 1866)
- Nicidion Kinberg, 1865
- Palola (Gray in Stair, 1847)
- Paucibranchia Molina-Acevedo, 2018
- Treadwellphysa Molina-Acevedo & Carrera-Parra, 2017
O icnotáxon fóssil Lepidenteron lewesiensis [en] provavelmente corresponde à toca fossilizada de um membro de Eunicidae. Essas tocas frequentemente são revestidas com os restos fossilizados de presas de seu ocupante, incluindo uma diversidade de táxons de peixes.[17] A aparência de uma toca alongada totalmente revestida com ossos de peixe pode fazer com que essas tocas sejam facilmente confundidas com o esqueleto completo de um peixe semelhante a enguia.[18]
Anatomia
Corpo segmentado
Os membros da família Eunicidae distinguem-se de outras famílias de Eunicida por possuírem um segmento posterior com 1-3 antenas e sem bases aneladas nas antenas.[19] O primeiro segmento corporal dos membros de Eunicidae é inteiro ou composto por dois lóbulos.[19] As brânquias de espécimes vivos são tipicamente identificáveis pela cor vermelha brilhante.[20]
Cabeça e mandíbulas
Um par de apêndices sensoriais delgados e cilíndricos geralmente está situado próximo à cabeça dos membros de Eunicidae.[19] Os lábios podem ser reduzidos ou bem desenvolvidos.[19] Nas espécies de Eunice, os vermes possuem cinco apêndices em dois apêndices segmentados alongados e três antenas próximas à cabeça.[19] Essa característica não faz parte da anatomia de todos os gêneros da família Eunicidae. As mandíbulas são tipicamente bem desenvolvidas e parcialmente visíveis na parte inferior do verme ou na superfície na frente da boca em uma estrutura complexa.[19][20]
Parede corporal
Algumas espécies de Eunicidae possuem extensões da parede corporal que se projetam para o sistema vascular.[19] Essas geralmente consistem em filamentos semelhantes a pentes.[19]
Ecologia
Distribuição e habitat
Os membros de Eunicidae estão distribuídos em diversos habitats bentônicos na Oceania, Europa, América do Sul, América do Norte, Ásia e África. Eles desempenham um papel ecológico nas comunidades bentônicas, exibindo preferência por substratos duros em águas rasas temperadas, águas tropicais e manguezais.[1][4] A maioria das espécies habita fendas e rachaduras em ambientes variados de entulhos, rochas e areia.[4] Em recifes de calcário ou coral, os membros de Eunicidae perfuram corais tubulares duros semelhantes a pergaminho ou permanecem em fendas de algas calcárias.[21]
Dieta
As dietas dos membros de Eunicidae variam entre gêneros. Por exemplo, Eunice aphroditois rasteja no fundo do mar onde se alimenta de forma carnívora de vermes marinhos, pequenos crustáceos, moluscos, algas e detritos geológicos.[2][14][22][23][24] Outras espécies, como Euniphysa tubifex e grandes Eunice, caçam nos arredores de seus habitats de coral e se alimentam da carne em decomposição de animais marinhos mortos.[2][25] Espécies escavadoras de Eunicidae (Lysidice e Palola) são principalmente herbívoras. Essas espécies se alimentam de corais maduros e organismos contidos ou de tipos de algas.[26] A dieta das espécies de Marphysa é variável: algumas são herbívoras,[24] outras carnívoras[27] e outras onívoras.[2][25]
Ameaças
A prática de coletar poliquetas (incluindo espécies da família Eunicidae) como isca pode ter impactos ecológicos negativos em habitats entremarés e nas populações de vermes.[9][11] Em 2019, Cabral e colegas constataram que Marphysa sanguinea está em risco devido à pesca predatória e coleta não licenciada em Portugal.[9] Os impactos ecológicos da coleta de isca também podem afetar populações de fauna associada[10] e a qualidade do sedimento[28] e a biodisponibilidade de metais pesados.[29][9] Pesquisas indicam que a sobrevivência e o crescimento de minhocas também podem ser afetados por mudanças nas taxas de salinidade.[30]
Impacto ecológico
Importar espécies de Eunicidae é uma alternativa estabelecida à exploração de populações locais para isca.[12] Esse processo pode levar a introduções acidentais ou invasões de espécies.[31][32] Espécies introduzidas podem ameaçar a base dos ecossistemas locais ao alterar redes tróficas, estruturas de habitat e fundos genéticos.[31] Espécies introduzidas também podem trazer doenças e parasitas.[32][33] Seis espécies de Eunice, uma espécie de Euniphysa, três espécies de Lysidice e uma espécie de Marphysa sp. foram identificadas como introduzidas em ecossistemas aquáticos locais no mar Mediterrâneo, mar Vermelho, oceano Pacífico dos EUA e mar do Norte.[31] Minhocas vivas são frequentemente despejadas na água pelos pescadores ao final de uma sessão de pesca, prática que também pode introduzir espécies em ecossistemas aquáticos.[12][31][32]
Ciclo de vida
Reprodução sexual
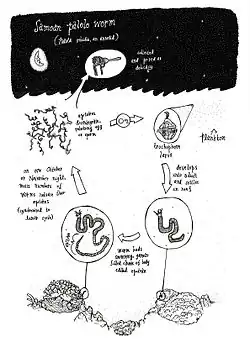
A maioria da classe Polychaeta consiste em animais bentônicos de reprodução sexual e não possuem órgãos reprodutores externos.[34] Durante o acasalamento, as fêmeas produzem um feromônio que induz a liberação mútua de espermatozoides masculinos e óvulos femininos. Esse processo de sincronia reprodutiva [en] é conhecido como epitoquia [en]. Durante esse processo, não há contato real entre macho e fêmea. O enxame reprodutivo é ejetado em águas abertas. Células que se fundem durante a fertilização (gametas) são liberadas por uma glândula excretora (metanefrídio) ou pela ruptura da parede corporal principal do verme.[35] Após a fertilização, a maioria dos ovos torna-se plânctonica; embora alguns permaneçam dentro dos tubos do verme ou se enterrem em massas gelatinosas externas presas aos tubos.[35] As epitoquias podem atrair um número aumentado de predadores pelágicos.[6] Em Florida Keys, por exemplo, o enxame de Eunice fucata é altamente divulgado nas comunidades pesqueiras locais, atraindo uma grande reunião de peixes Megalopidae.[6] Esses eventos massivos de enxame, ou "subidas", são um espetáculo que fundamenta tradições locais em Samoa, Fiji, Tonga, Papua-Nova Guiné, Vanuatu, Quiribáti e Indonésia.[1]

Relações humanas

Como isca na pesca comercial e recreativa
Marphysa sanguinea, conhecida localmente na Itália como "Murrido", "Murone", "Bacone" e "Verme sanguigno", é a isca mais valiosa entre todas as espécies de poliquetas coletadas na Itália.[7] Essa espécie também é cultivada nos Estados Unidos e na Coreia do Sul e geralmente é colhida comercialmente uma vez que atinge seu comprimento ótimo de 20–30 cm.[7] Marphysa sanguinea pode atingir até 50 cm e é coletada escavando em sedimentos profundos.[8] Por exemplo, na Lagoa de Veneza, pescadores cavam abaixo das camadas de sedimento colonizadas por membros da família Nereididae e peneiram material orgânico por telas grossas.[36] Esse processo também é comum em áreas costeiras italianas com fundos lamacentos entremarés e litorâneos rasos.[7] Eunice aphroditois, outra espécie grande (até 1 metro de comprimento) de Eunicidae, é colhida por mergulhadores ao longo das costas da Apúlia italiana.[7] Essa espécie é coletada em fundos oceânicos moles a uma profundidade de 10 metros usando instrumentos especializados de colheita que se encaixam em tubos de pergaminho em forma de U onde o verme vive.[8] Essa espécie de Eunicidae é isca adequada para peixes da família Sparidae e é usada na prática comercial de anzol e linha.[7] Espécies da família Eunicidae também são capturadas por pescadores recreativos e comerciais em estuários ao longo da costa oeste de Portugal e na baía de Arcachon [en] na França.[7][37] Marphysa são propagadas e colhidas em comunidades estuarinas australianas localizadas ao longo da costa de Nova Gales do Sul e Queensland.[37] A coleta de Marphysa moribidii como isca ocorre ao longo da costa oeste da península da Malásia, Marphysa elityeni é capturada em pescarias de subsistência na África e Eunice sebastiani foi relatada como colhida para isca no Brasil.[37] Membros de Eunicidae também são usados como alimento suplementar na aquacultura.[8][38][39][40] Por exemplo, minhocas fazem parte da dieta do camarão Penaeus monodon em alguns criadouros da Tailândia.[38][41]
Nas lendas e na cultura
No Indo-Pacífico, durante 1–2 noites por ano, as epitoquias de Palola viridis são automatizadas.[1][6] As epitoquias grandes (até 30 cm de comprimento) nadam de forma autônoma para cima e se rompem, liberando gametas na superfície do oceano.[1] As epitoquias são compostas por centenas de segmentos, com fêmeas de cor esmeralda e machos transitando de laranja para marrom durante a maturação.[6] Na noite de "subida", é tradição de algumas comunidades locais atrair epitoquias com fontes de luz artificiais ou outros métodos tradicionais.[37] Em Samoa, por exemplo, os locais usam colares feitos de flores e o aroma floral para atrair os vermes.[37] As epitoquias são coletadas das águas rasas com redes e recipientes para serem consumidos crus, cozidos, assados, secos ou congelados para consumo posterior.[37]
Ver também
Referências
- ↑ a b c d e Rouse, G. W; Pleijel, F. (2001). «ROUSE, G. W. & PLEIJEL, F. 2001. Polychaetes. Xiii + 354 pp. Oxford: Oxford University Press. Price £109.50. ISBN 0 19 850608 2». Oxford: Oxford University Press. Geological Magazine (em inglês). 140 (5): 617–618. doi:10.1017/S0016756803278341
- ↑ a b c d Fauchald, K; Jumars, P. A. (1979). «The Diet of Worms: A Study of Polychaete Feeding Guilds». Aberdeen University Press. Oceanography and Marine Biology: An Annual Review. 17: 193–284
- ↑ Keith Davey (2000). «Eunice aphroditois». Life on Australian Seashores. Consultado em 10 de outubro de 2007
- ↑ a b c d e f g h i j k l Fauchald, K. (1992). «A review of the genus Eunice (Polychaeta: Eunicidae) based upon type material» (PDF). Smithsonian Contributions to Zoology. 523 (523): 1–422. Bibcode:1992SCZoo.523....1F. doi:10.5479/si.00810282.523
- ↑ Parry, Luke; Tanner, Alastair; Vinther, Jakob (2015). «The Origin of Annelids». The Palaeontological Association. Palaeontology. 57 (6): 1091–1103. doi:10.1111/pala.12129
- ↑ a b c d e Schulze, Anja; Timm, Laura E. (2011). «Palolo and un: distinct clades in the genus Palola (Eunicidae, Polychaeta)». Marine Biodiversity (em inglês). 42 (2): 161–171. ISSN 1867-1616. doi:10.1007/s12526-011-0100-5
- ↑ a b c d e f g Gambi, M. C.; Castelli, A.; Giangrande, A.; Lanera, P.; Prevedelli, D.; Zunarelli Vandini, R. (1994). «Polychaetes of Commercial and Applied Interest in Italy: An Overview». Mémoires du Muséum National d'Histoire Naturelle. 162: 593–603
- ↑ a b c d Olive, P. J. W. (1994). «Polychaeta as a World Resource: A Review of Patterns of Exploitation as Sea Angling Baits, and Potential for Aquaculture Based Production». Mémoires du Muséum National d'Histoire Naturelle. 162: 603–610
- ↑ a b c d Cabral, Sara; Alves, Ana Sofia; Castro, Nuno; Chainho, Paula; Sá, Erica; Cancela da Fonseca, Luís; Fidalgo e Costa, Pedro; Castro, João; Canning-Clode, João; Pombo, Ana; Costa, José Lino (1 de novembro de 2019). «Polychaete annelids as live bait in Portugal: Harvesting activity in brackish water systems»
 . Ocean & Coastal Management (em inglês). 181. Bibcode:2019OCM...18104890C. ISSN 0964-5691. doi:10.1016/j.ocecoaman.2019.104890. hdl:10400.8/5015
. Ocean & Coastal Management (em inglês). 181. Bibcode:2019OCM...18104890C. ISSN 0964-5691. doi:10.1016/j.ocecoaman.2019.104890. hdl:10400.8/5015
- ↑ a b Birchenough, S. (2013). «Impact of Bait Collecting in Poole Harbour and Other Estuaries within the Southern IFCA District». South. Inshore Fish Conserv. Auth.: 117
- ↑ a b Carvalho, André Neves de; Vaz, Ana Sofia Lino; Sérgio, Tânia Isabel Boto; Santos, Paulo José Talhadas dos (2013). «Sustainability of bait fishing harvesting in estuarine ecosystems – Case study in the Local Natural Reserve of Douro Estuary, Portugal». Revista de Gestão Costeira Integrada. 13 (2): 157–168. ISSN 1646-8872. doi:10.5894/rgci393
 . hdl:10216/76387
. hdl:10216/76387
- ↑ a b c Martin, Daniel; Gil, João; Zanol, Joana; Meca, Miguel A.; Portela, Rocío Pérez (21 de maio de 2020). «Correction: Digging the diversity of Iberian bait worms Marphysa (Annelida, Eunicidae)». PLOS ONE (em inglês). 15 (5). Bibcode:2020PLoSO..1533825M. ISSN 1932-6203. PMC 7241716
 . PMID 32437422. doi:10.1371/journal.pone.0233825
. PMID 32437422. doi:10.1371/journal.pone.0233825
- ↑ Zanol, Joana; Hutchings, Pat A.; Fauchald, Kristian (5 de março de 2020). «Eunice sensu lato (Annelida: Eunicidae) from Australia: description of seven new species and comments on previously reported species of the genera Eunice, Leodice and Nicidion»
 . Zootaxa (em inglês). 4748 (1). PMID 32230084. doi:10.11646/zootaxa.4748.1.1
. Zootaxa (em inglês). 4748 (1). PMID 32230084. doi:10.11646/zootaxa.4748.1.1
- ↑ a b Zanol, J.; Halanych, M.; Fauchald, K. (2013). «Reconciling Taxonomy and Phylogeny in the Bristleworm Family Eunicidae (Polychaete, Annelida)». Zoologica Scripta. 43 (1): 79–100. doi:10.1111/zsc.12034
- ↑ «World Polychaeta Database». www.marinespecies.org. Consultado em 15 de novembro de 2020
- ↑ «WoRMS - World Register of Marine Species - Eunicidae Berthold, 1827». www.marinespecies.org. Consultado em 17 de maio de 2024
- ↑ Bieńkowska-Wasiluk, Małgorzata; Uchman, Alfred; Jurkowska, Agata; Świerczewska-Gładysz, Ewa (1 de dezembro de 2015). «The trace fossil Lepidenteron lewesiensis: a taphonomic window on diversity of Late Cretaceous fishes». Paläontologische Zeitschrift (em inglês). 89 (4): 795–806. Bibcode:2015PalZ...89..795B. ISSN 1867-6812. PMC 5448080
 . PMID 28596622. doi:10.1007/s12542-015-0260-x
. PMID 28596622. doi:10.1007/s12542-015-0260-x
- ↑ «Fossils of the Chalk (2nd Edition) | Fossil Books». ZOIC PalaeoTech Limited (em inglês). Consultado em 10 de setembro de 2024
- ↑ a b c d e f g h Paxton, Hannelore (2000). Polychaetes & Allies: The Southern Synthesis. 4A. [S.l.]: Commonwealth of Australia. pp. 127–130
- ↑ a b Wilson, RS; Hutchings, PA; Glasby, CJ. «Polychaetes: An Interactive Identification Guide». researchdata.museum.vic.gov.au. Consultado em 19 de novembro de 2020
- ↑ Hutchings, P. A. (1986). «Biological Destruction of Coral Reefs: A Review»
 . Coral Reefs (em inglês). 4 (4): 239–252. Bibcode:1986CorRe...4..239H. ISSN 0722-4028. doi:10.1007/BF00298083
. Coral Reefs (em inglês). 4 (4): 239–252. Bibcode:1986CorRe...4..239H. ISSN 0722-4028. doi:10.1007/BF00298083
- ↑ Hempelmann, F. (1931). Kükenthal, W.; Krumbach, T., eds. «Handbuch der Zoologie». Lief. 2: 12–13 – via De Gruyter & Co.
- ↑ Evans, S. M. (1971). «Behavior in Polychaetes». The Quarterly Review of Biology. 46 (4): 379–405. ISSN 0033-5770. doi:10.1086/407004
- ↑ a b Yonge, C.M (1954). «Tabulæ Biologicæ Periodicæ». Nature. 21(3) (3272): 25–45. doi:10.1038/130078c0
- ↑ a b Day, J.H. (1967). «A Monograph on the Polychaeta of Southern Africa Part 1, Errantia: Part 2, Sedentaria». Trustees of the British Muséum (Natural History). Journal of the Marine Biological Association of the United Kingdom. 656: 878 – via CambridgeCore
- ↑ Fauchald, Kristian (1992). «A Review of the Genus Eunice (Polychaeta: Eunicidae) Based upon Type Material»
 . Smithsonian Contributions to Zoology (em inglês). 523 (523): 1–422. Bibcode:1992SCZoo.523....1F. doi:10.5479/si.00810282.523. hdl:10088/6302
. Smithsonian Contributions to Zoology (em inglês). 523 (523): 1–422. Bibcode:1992SCZoo.523....1F. doi:10.5479/si.00810282.523. hdl:10088/6302
- ↑ Desiere, M. (1967). «Annales de la Société Royale Zoologique de Belgique». Société Royale Zoologique de Belgique. 97: 65–90
- ↑ Anderson, Franz E.; Meyer, Lawrence M. (1986). «The interaction of tidal currents on a disturbed intertidal bottom with a resulting change in particulate matter quantity, texture and food quality». Estuarine, Coastal and Shelf Science. 22 (1): 19–29. Bibcode:1986ECSS...22...19A. ISSN 0272-7714. doi:10.1016/0272-7714(86)90021-1
- ↑ Falcão, M.; Caetano, M.; Serpa, D.; Gaspar, M.; Vale, C. (2006). «Effects of infauna harvesting on tidal flats of a coastal lagoon (Ria Formosa, Portugal): Implications on phosphorus dynamics». Marine Environmental Research. 61 (2): 136–148. Bibcode:2006MarER..61..136F. ISSN 0141-1136. PMID 16242182. doi:10.1016/j.marenvres.2005.08.002
- ↑ Garcês, J. P.; Pereira, J. (3 de setembro de 2010). «Effect of salinity on survival and growth of Marphysa sanguinea Montagu (1813) juveniles». Aquaculture International. 19 (3): 523–530. ISSN 0967-6120. doi:10.1007/s10499-010-9368-x
- ↑ a b c d Çinar, Melih Ertan (2012). «Alien Polychaete Species Worldwide: Current Status and their Impacts»
 . Cambridge University Press. Journal of the Marine Biological Association of the United Kingdom (em inglês). 93 (5): 1257–1278. ISSN 0025-3154. doi:10.1017/S0025315412001646 – via CambridgeCore
. Cambridge University Press. Journal of the Marine Biological Association of the United Kingdom (em inglês). 93 (5): 1257–1278. ISSN 0025-3154. doi:10.1017/S0025315412001646 – via CambridgeCore
- ↑ a b c Font, Toni; Gil, João; Lloret, Josep (2017). «The Commercialisation and use of Exotic Baits in Recreational Fisheries in the North-Western Mediterranean: Environmental and Management Implications». Aquatic Conservation: Marine and Freshwater Ecosystems (em inglês). 28 (3): 651–661. doi:10.1002/aqc.2873. hdl:10261/160084

- ↑ Occhipinti Ambrogi, A. (2001). «Transfer of Marine Organisms: A Challenge to the Conservation of Coastal Biocoenoses». Aquatic Conservation: Marine and Freshwater Ecosystems. 11 (4): 243–251. Bibcode:2001ACMFE..11..243O. doi:10.1002/aqc.450

- ↑ Mastrototaro, F.; Giove, A.; D'Onghia, G.; Tursi, A.; Matarrese, A.; Gadaleta, M.V. (2008). «Benthic diversity of the soft bottoms in a semi-enclosed basin of the Mediterranean Sea»
 . Journal of the Marine Biological Association of the United Kingdom (em inglês). 88 (2): 247–252. Bibcode:2008JMBUK..88..247M. ISSN 0025-3154. doi:10.1017/S0025315408000726
. Journal of the Marine Biological Association of the United Kingdom (em inglês). 88 (2): 247–252. Bibcode:2008JMBUK..88..247M. ISSN 0025-3154. doi:10.1017/S0025315408000726
- ↑ a b Ruppert, E.E.; Fox, R.S.; Barnes, R.D. (2004). Invertebrate Zoology. A functional evolutionary approach 7th ed. Thomson Learning: Brooks/Cole. p. 990
- ↑ Hutchings, P. A. (1986). «Biological destruction of coral reefs: A review»
 . Coral Reefs (em inglês). 4 (4): 239–252. Bibcode:1986CorRe...4..239H. ISSN 0722-4028. doi:10.1007/BF00298083
. Coral Reefs (em inglês). 4 (4): 239–252. Bibcode:1986CorRe...4..239H. ISSN 0722-4028. doi:10.1007/BF00298083
- ↑ a b c d e f Cole, Victoria J.; Chick, Rowan C.; Hutchings, Patricia A. (2018). «A review of global fisheries for polychaete worms as a resource for recreational fishers: diversity, sustainability and research needs»
 . Reviews in Fish Biology and Fisheries (em inglês). 28 (3): 543–565. Bibcode:2018RFBF...28..543C. ISSN 0960-3166. doi:10.1007/s11160-018-9523-4
. Reviews in Fish Biology and Fisheries (em inglês). 28 (3): 543–565. Bibcode:2018RFBF...28..543C. ISSN 0960-3166. doi:10.1007/s11160-018-9523-4
- ↑ a b Mandario, Mary Anne E. (2020). «Survival, growth and biomass of mud polychaete Marphysa iloiloensis (Annelida: Eunicidae) under different culture techniques». Aquaculture Research (em inglês). 51 (7): 3037–3049. ISSN 1355-557X. doi:10.1111/are.14649

- ↑ Alava, V. R., Biñas, J. B., & Mandario, M. A. E. (2017). Breeding and culture of the polychaete, Marphysa mossambica, as feed for the mud crab. In E. T. Quinitio, F. D. Parado-Estepa, & R. M. Coloso (Eds.), Philippines : In the forefront of the mud crab industry development : proceedings of the 1st National Mud Crab Congress, 16–18 November 2015, Iloilo City, Philippines (pp. 39–45). Tigbauan, Iloilo, Philippines: Aquaculture Department, Southeast Asian Fisheries Development Center. https://repository.seafdec.org.ph/handle/10862/3197
- ↑ Naessens, E.; Lavens, P.; Gomez, L.; Browdy, C.L.; McGovern-Hopkins, K.; Spencer, A.W.; Kawahigashi, D.; Sorgeloos, P. (1997). «Maturation performance of Penaeus vannamei co-fed Artemia biomass preparations»
 . Aquaculture (em inglês). 155 (1–4): 87–101. Bibcode:1997Aquac.155...87N. doi:10.1016/S0044-8486(97)00111-7
. Aquaculture (em inglês). 155 (1–4): 87–101. Bibcode:1997Aquac.155...87N. doi:10.1016/S0044-8486(97)00111-7
- ↑ Meunpol, Oraporn; Meejing, Panadda; Piyatiratitivorakul, Somkiat (2005). «Maturation diet based on fatty acid content for male Penaeus monodon (Fabricius) broodstock». Aquaculture Research. 36 (12): 1216–1225. Bibcode:2005AqRes..36.1216M. ISSN 1355-557X. doi:10.1111/j.1365-2109.2005.01342.x

Ligações externas
- «WoRMS - World Register of Marine Species - Eunicidae Berthold, 1827» (banco de dados taxonômico). marinespecies.org (em inglês)
- Edição especial da Marine Ecology dedicada aos vermes poliquetas
- Chave para Famílias de Poliquetas, Museu de História Natural de Londres
