Euchambersia
Euchambersia
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ocorrência: Wujiapinguiano | |||||||||||||||||
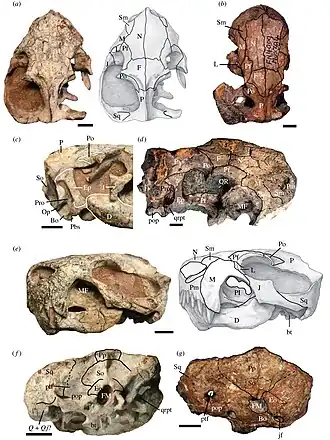 Crânio de E. liuyudongi do topo (a), lados (c, e) e dorso (f), e crânios de E. mirabilis do topo (b; BP/1/4009), lado (d; NHMUK R5696) e dorso (g; NHMUK R5696) | |||||||||||||||||
| Classificação científica | |||||||||||||||||
| |||||||||||||||||
| Espécie-tipo | |||||||||||||||||
| †Euchambersia mirabilis Broom, 1931 | |||||||||||||||||
| Outras espécies | |||||||||||||||||
| |||||||||||||||||
Euchambersia é um gênero extinto de terapsídeos da linhagem Therocephalia que viveu durante o Lopinguiano no que hoje é a África do Sul e a China. O gênero inclui duas espécies. A espécie-tipo E. mirabilis foi nomeada pelo paleontólogo Robert Broom em 1931 a partir de um crânio sem a mandíbula inferior.[1] Um segundo crânio, provavelmente de um indivíduo imaturo, foi descrito posteriormente. Em 2022, uma segunda espécie, E. liuyudongi, foi nomeada por Jun Liu e Fernando Abdala com base em um crânio bem preservado. É um membro da família Akidnognathidae [en], historicamente também referida como Euchambersiidae (nomeada em homenagem a Euchambersia).
Euchambersia era um dinossauro pequeno com focinho curto, possuindo grandes caninos, característica típica do grupo. No entanto, destaca-se entre os membros da linhagem Therocephalia por apresentar cristas nos caninos e uma grande indentação na lateral do crânio. Sugeriu-se que essas estruturas sustentavam um mecanismo de entrega de veneno. Caso isso seja confirmado, seria um dos tetrápodes mais antigos conhecidos com essa característica. Em 2017, a estrutura interna do crânio de E. mirabilis forneceu evidências mais robustas para a hipótese de que era venenoso, embora outras possibilidades, como a indentação abrigar um órgão sensorial, permaneçam plausíveis.
Descoberta e nomenclatura
O espécime-tipo de Euchambersia mirabilis e do gênero Euchambersia foi encontrado por Robert Broom na fazenda Vanwyksfontein, de propriedade do Sr. Greathead, perto da cidade de Norvalspont [en], na África do Sul. Consiste em um único crânio deformado, catalogado como NHMUK R5696, descrito por Broom em 1931.[1] Um segundo crânio, menor, com o número de espécime BP/1/4009, foi encontrado em 1966[2] e descrito por James Kitching [en] em 1977. Ambos os espécimes não possuem a mandíbula. Eles provêm da mesma camada geral de rocha, na zona de agrupamento superior de Cistecephalus do Grupo Beaufort [en] no Supergrupo Karoo [en].[3] A zona de Cistecephalus foi datada do estágio Wujiapinguiano do Lopinguiano,[4] entre 256,2 e 255,2 milhões de anos.[5]
Broom nomeou o gênero Euchambersia, que considerou "o terocefálio mais notável já descoberto", em homenagem ao eminente editor escocês e pensador evolucionista Robert Chambers, cuja obra Vestiges of the Natural History of Creation foi considerada por Broom "um trabalho muito notável", embora "desprezada por muitos".[1]
A segunda espécie, E. liuyudongi, foi nomeada por Jun Liu e Fernando Abdala em 2022 com base em um crânio bem preservado com mandíbula associada, catalogado como IVPP V 31137. Alguns restos pós-cranianos, incluindo seis vértebras e fragmentos de costelas, também pertencem a este espécime, mas não foram descritos pelos autores. O epíteto específico homenageia Liu Yu-Dong, o técnico que descobriu o holótipo em 2020. Esta espécie é originária da Formação Naobaogou [en] da Mongólia Interior, datada de forma mais ampla para a época Lopinguiano (que inclui o Wujiapinguiano). A formação é dividida em três membros com base em ciclos de sedimentação, numerados como membros I, II e III, do mais antigo ao mais recente; E. liuyudongi provém do membro I.[6] Liu e colegas já haviam descrito várias outras espécies novas da porção intermediária da Formação Naobaogou, entre os 80 espécimes escavados em pelo menos três temporadas de campo após 2009.[7][8]
Descrição
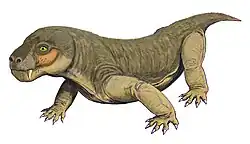
E. mirabilis era pequeno e com focinho curto (o focinho correspondendo a cerca de metade do comprimento do crânio) para um terocefálio, com o crânio-tipo apresentando um comprimento reconstruído de aproximadamente 11,6 cm, considerando a deformação e esmagamento do fóssil. O segundo crânio conhecido pertencia a um indivíduo menor, com 8 cm de comprimento, provavelmente imaturo, a julgar pela falta de fusão no crânio.[2] O crânio-tipo de E. liuyudongi mede 7 cm de comprimento e possui um focinho ainda mais curto (menos de 40% do comprimento do crânio).[6]
Segundo a descrição inicial, a órbita ocular de E. mirabilis era relativamente pequena. Os ramos do pós-orbital e do jugal, que geralmente circundam a parte posterior e inferior da órbita ocular em terocefálios, parecem estar muito reduzidos ou ausentes. A parte superior da órbita é formada pelo pré-frontal, e o frontal também é pequeno. O crânio não possui um forame pineal. Como em Whaitsia, o pterigoide e o palatino do palato não são separados do transpalatino, mais lateral à mandíbula, por qualquer tipo de abertura.[1] E. liuyudongi difere de E. mirabilis em vários detalhes desses ossos: o osso frontal separa o pré-frontal do contato com o pós-orbital, e as fenestras pós-orbitais na parte posterior do crânio são em forma de fenda em vez de arredondadas. Além disso, o epipterigoide e o proótico da caixa craniana estão desconectados em E. liuyudongi.[6]
Dentes
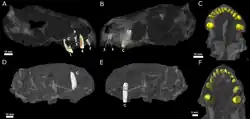
Embora os crânios de E. mirabilis sejam preservados de forma incompleta, exames de tomografia computadorizada sugerem que cada pré-maxila continha cinco incisivos, com os alvéolos dentários aumentando progressivamente de tamanho do primeiro ao quinto incisivo. Como outros teriodontes, as coroas dos incisivos são cônicas; também não possuem serrilhas, ao contrário dos gorgonopsianos e terocefálios do clado Scylacosauria [en]. A borda interna dos incisivos parece ser ligeiramente côncava, e a borda posterior apresenta uma crista. O espécime menor possui um incisivo deslocado preservado dentro de sua cavidade nasal; ele é mais fortemente recurvado e apresenta marcas de desgaste na borda superior, sugerindo que provavelmente é um incisivo inferior. Seu quarto incisivo também tem um dente de substituição crescendo atrás dele, acompanhado de reabsorção da raiz.[2]
O espécime-tipo de E. mirabilis preserva o canino direito.[2] Como outros terocefálios, seu canino era muito grande, resultando em um estilo de vida predatório especializado que incorporava uma mordida de dente de sabre para matar presas.[9] É redondo em seção transversal,[3] e possui uma crista proeminente na lateral de sua superfície frontal. Imediatamente ao lado dessa crista, há uma depressão rasa que se alarga perto do topo do dente, provavelmente a mesma estrutura interpretada por alguns autores como um sulco.[2][10] Diferentemente de E. mirabilis, os caninos de E. liuyudongi não apresentavam cristas nem sulcos.[6] Teriodontes geralmente substituem seus dentes em um padrão alternado,[11][12][13] de modo que o canino esteja sempre funcional; ambos os crânios de E. mirabilis não mostram sinais de caninos de substituição em desenvolvimento, sugerindo que dependia de ter ambos os caninos presentes e funcionais simultaneamente.[2]
Fossa maxilar e canais associados
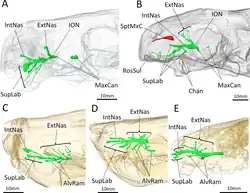
Atrás dos incisivos e caninos, não havia dentes adicionais nas mandíbulas superior e inferior (conforme confirmado por E. liuyudongi).[6] Onde os dentes estariam localizados em terocefálios que possuem dentes pós-caninos, havia uma grande depressão, ou fossa, na lateral do osso maxilar, também delimitada abaixo por parte do lacrimal e possivelmente parte do jugal.[1] Essa fossa corresponde a 48% do comprimento da mandíbula no espécime-tipo de E. mirabilis e 38% no segundo crânio. Em ambos os crânios, a fossa é dividida em duas partes: uma crista mais rasa no topo e uma depressão maior e mais profunda na parte inferior. Um sulco largo que começa atrás do canino entra em contato com a parte inferior da fossa e passa para o interior da boca. A porção inferior da fossa é fortemente perfurada e apresenta uma pequena abertura, ou forame, nas superfícies frontal e posterior.[2] Em E. liuyudongi, essa fossa é ainda mais profunda; uma barra do maxilar cobre o topo da fossa e entra em contato com o jugal, e a parede interna da fossa possui uma grande abertura para a cavidade nasal. A fossa quase alcança a metade da altura do focinho.[6]
Exames de tomografia computadorizada mostram que as aberturas de E. mirabilis levam a canais que se conectam ao nervo trigêmeo, que controla a sensibilidade facial. O canal direcionado para a frente também se divide nos três ramos principais do nervo infraorbital,[14] todos conectados ao alvéolo do canino; a junção ocorre cerca de 3 a 6 mm ao longo do canal, outro ponto de variação entre os dois crânios. O ramo superior, o ramo nasal externo, divide-se em quatro ramos no crânio-tipo, mas não se divide no segundo crânio. Em outros terapsídeos como Thrinaxodon, Bauria e Olivierosuchus [en], o ramo nasal externo geralmente se divide em três ou mais ramos. Todos esses canais teriam levado nervos e tecidos ricos em nutrientes à raiz dos caninos e ao restante da mandíbula superior.[2][14]
Classificação
Em 1934, Euchambersia foi atribuída à família recém-nomeada Euchambersiidae por Lieuwe Dirk Boonstra [en].[15][16] Boonstra inicialmente escreveu o nome incorretamente como Euchambersidae (latim impróprio), sendo corrigido por Friedrich von Huene em 1940. Inicialmente, Euchambersiidae era considerada distinta das famílias Moschorhinidae e Annatherapsididae; em 1974, Christiane Mendez reconheceu esses grupos como subfamílias estreitamente relacionadas (renomeadas Annatherapsidinae, Moschorhininae e Euchambersiinae) dentro do grupo mais amplo de sua Moschorhinidae redefinida (embora também a tenha chamado de Annatherapsididae).[17]
A análise filogenética de 1986 de James Hopson [en] e Herb Barghusen apoiou a hipótese de Mendez de três subfamílias dentro de Moschorhinidae, mas eles optaram por usar o nome Euchambersiidae. Em 2009, Adam Huttenlocker argumentou que os nomes Annatherapsididae, Moschorhinidae e Euchambersiidae são sinônimos de Akidnognathidae [en], já que Akidnognathus [en] (também pertencente à mesma família) foi nomeado antes de qualquer outro membro da família.[17] Esse nome ganhou maior aceitação entre os pesquisadores.[17][18][19] Huttenlocker e Christian Sidor [en] posteriormente redefiniram Moschorhininae como todos os Akidnognathidae, exceto Annatherapsidus [en] e Akidnognathus.[20]
Em 2008, Mikhail Ivakhnenko [en] incluiu os Akidnognathidae (como Euchambersiidae) como grupo-irmão da família Whaitsiidae [en] na superfamília Whaitsioidea.[16] No entanto, outros pesquisadores não incluem os Akidnognathidae em Whaitsioidea. Filogenias de Huttenlocker e Sidor indicaram que os Akidnognathidae eram mais próximos dos Chthonosauridae, formando juntos o grupo-irmão do grupo que contém Whaitsioidea e Baurioidea [en].[20] Liu e Abdala realizaram uma nova análise filogenética em 2022 para a descrição de E. liuyudongi. Eles descobriram que as duas espécies formam um grupo unificado dentro dos Akidnognathidae, com o restante da topologia semelhante à encontrada por Huttenlocker e Sidor. A topologia recuperada por sua análise é mostrada abaixo, com rótulos de grupos seguindo Huttenlocker e Sidor.[6]
| Therocephalia |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Paleobiologia
Veneno
As grandes fossas maxilares de Euchambersia têm sido objeto de debate contínuo sobre sua função. No entanto, a maioria dos pesquisadores concorda que abrigavam algum tipo de glândula secretora. Embora Broom inicialmente sugerisse que as fossas poderiam conter glândulas salivares parótidas,[1] essa proposta foi rejeitada por Boonstra e Jean-Pierre Lehman [en], que notaram que as glândulas parótidas geralmente ficam atrás do olho; eles sugeriram, respectivamente, que as fossas abrigavam glândulas lacrimais modificadas e glândula de Harder.[2] No entanto, a última também é improvável, pois as glândulas de Harder geralmente estão dentro da órbita ocular. Franz Nopcsa sugeriu que as fossas maxilares abrigavam glândulas de veneno (possivelmente derivadas de glândulas lacrimais), com os caninos com cristas e os entalhes atrás dos caninos permitindo que o veneno fluísse passivamente para a corrente sanguínea da vítima.[21] Essa hipótese foi amplamente aceita ao longo do século XX[18][22][23][24] e a morfologia característica de Euchambersia foi usada para apoiar possíveis adaptações de veneno em vários outros animais pré-históricos,[10][25][26] incluindo os terocefálios relacionados Megawhaitsia[16] e Ichibengops [en].[27]
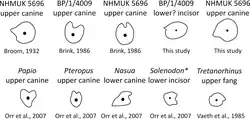
Muito dessa aceitação baseou-se na suposição errônea de que os caninos eram sulcados em vez de cristas;[3] caninos sulcados em Euchambersia seriam paralelos às presas de várias cobras venenosas, bem como aos incisivos de entrega de veneno dos solenodontes vivos.[24] Essa interpretação, que apareceu consistentemente na literatura publicada após 1986, foi considerada por Julien Benoit como resultado da propagação do diagrama excessivamente reconstruído do crânio por Broom, sem o contexto dos espécimes reais. Assim, ele considerou necessário reavaliar a hipótese de uma mordida venenosa em Euchambersia.[3] Além disso, Benoit argumentou que caninos sulcados e com cristas não estão necessariamente associados a animais venenosos, como mostrado por sua presença em hipopótamos, muntíacos e babuínos, nos quais desempenham um papel na higiene ou afiação dos dentes;[3][24][28] nos dois últimos, caninos com cristas também são acompanhados por uma fossa distinta à frente do olho, totalmente desconectada do veneno.[24][29] Além disso, dentes sulcados e com cristas em cobras não venenosas são usados para reduzir a resistência ao capturar presas escorregadias, como peixes ou invertebrados.[30]
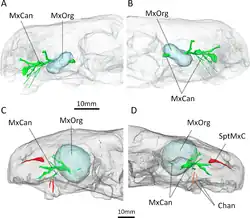
A tomografia computadorizada dos espécimes conhecidos de Euchambersia por Benoit e colegas foi posteriormente usada para fornecer suporte mais concreto à hipótese do veneno. Os canais que levam às fossas maxilares, revelados pelas tomografias, teriam sustentado principalmente o nervo trigêmeo, bem como vasos sanguíneos.[31][32][33] No entanto, o fato de os canais também levarem diretamente à raiz dos caninos sugere que tinham um papel secundário na entrega de veneno. Em resumo, Euchambersia parece ter tido uma glândula de veneno (alojada nas fossas maxilares), um mecanismo de entrega de veneno (os canais maxilares) e um instrumento para infligir uma ferida para entrega de veneno (os caninos com cristas), que satisfazem os critérios de um animal venenoso conforme definido por Wolfgang Bücherl.[34] Benoit et al. observaram que isso não demonstra conclusivamente que Euchambersia era de fato venenoso, especialmente considerando as objeções mencionadas anteriormente. Além disso, não há animais vivos com um sistema de entrega análogo ao proposto para Euchambersia (a maioria entrega veneno pela mandíbula inferior,[35][36] enquanto as cobras possuem dutos especializados.[2][37]
Uma hipótese alternativa sugerida por Benoit et al. envolve algum tipo de órgão sensorial ocupando a fossa maxilar. Unicamente entre os terapsídeos,[14] o canal dentro da maxila está exposto na parte posterior da fossa maxilar, o que implica que o canal, carregando o nervo trigêmeo, provavelmente se estendia pela fossa, fora do contorno do crânio. Benoit et al. levantaram a hipótese de que a fossa pode ter suportado um órgão sensorial especializado análogo ao órgão de fosseta de crotalíneos e algumas outras cobras,[38] ou alternativamente um gânglio de células nervosas. Também é possível que esse órgão funcionasse como substituto do olho parietal em Euchambersia, como o órgão de fosseta faz nos crotalíneos.[39] No entanto, um órgão sensorial tão expandido seria inédito entre tetrápodes, e os poucos outros terocefálios que também não possuem um olho parietal não têm uma fossa maxilar.[40] Assim, Benoit et al. consideraram a hipótese do veneno como mais plausível.[2]
No entanto, no espécime bem preservado da segunda espécie, E. liuyudongi, nem o focinho nem a órbita mostraram sinais de glândula venenosa. Apenas as glândulas pré-orbitais (olfativas) foram encontradas, apoiando a "hipótese da glândula olfativa", embora tomografias sejam necessárias para mais informações sobre a dentição e o crânio da nova espécie.[6]
Paleoecologia
E. mirabilis
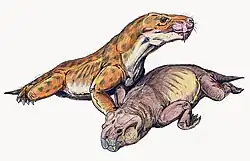
A Zona de Agrupamento de Cistecephalus, de onde E. mirabilis é conhecida, representa uma planície de inundação coberta por muitos riachos pequenos e relativamente retos. O nível de água nesses riachos provavelmente dependia da sazonalidade.[4] A partir de pólen preservado na zona de Cistecephalus, o táxon de pólen Pityosporites (provavelmente originado de uma planta semelhante a Glossopteris) era muito comum, formando cerca de 80% a 90% do pólen descoberto (embora os sedimentos predominantes não fossem ideais para a preservação de pólen).[41]
Na zona de Cistecephalus, outros terocefálios coexistentes incluíam Hofmeyria [en], Homodontosaurus [en], Ictidostoma [en], Ictidosuchoides [en], Ictidosuchops [en], Macroscelesaurus [en], Polycynodon [en] e Proalopecopsis. Mais numerosos, no entanto, eram os gorgonopsianos, que incluíam Aelurognathus, Aelurosaurus, Aloposaurus, Arctognathus, Arctops, Cerdorhinus [en], Clelandina [en], Cyonosaurus [en], Dinogorgon, Gorgonops, Lycaenops [en], Leontocephalus, Pardocephalus, Prorubidgea, Rubidgea, Scylacops [en], Scymnognathus e Sycosaurus [en].[4]
De longe, o herbívoro mais abundante era Diictodon, com mais de 1.900 espécimes conhecidos na zona de Cistecephalus. Outros espécimes do clado Dicynodontia incluíam Aulacephalodon [en], Cistecephalus [en], Dicynodon, Dicynodontoides [en], Digalodon [en], Dinanomodon [en], Emydops [en], Endothiodon [en], Kingoria, Kitchinganomodon [en], Oudenodon [en], Palemydops [en], Pelanomodon [en], Pristerodon [en] e Rhachiocephalus [en]. Os membros do clado Biarmosuchia Lemurosaurus [en], Lycaenodon [en], Paraburnetia e Rubidgina [en] também estavam presentes, junto com os cinodontes Cynosaurus [en] e Procynosuchus. Não-sinapsídeos incluíam o arcosauromorfo Youngina [en]; os parareptilianos Anthodon, Milleretta [en], Nanoparia [en], Owenetta e Pareiasaurus; e o membro da ordem Temnospondyli Rhinesuchus [en].[4]
E. liuyudongi
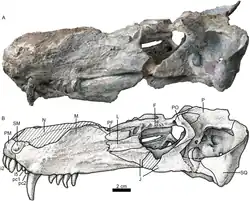
A Formação Naobaogou, de onde E. liuyudongi é conhecido, faz parte de uma série de depósitos fluviais e lacustres do Lopinguiano na Mongólia Interior, depositados por rios entrelaçados, planícies de inundação e lagos de planície de inundação.[42] Terocefálios foram relatados na Formação Naobaogou desde 1989,[43] mas esses fósseis foram posteriormente perdidos. Posteriormente, Liu e Abdala confirmaram sua presença na formação ao descreverem dois outros membros da família Akidnognathidae além de E. liuyudongi, Shiguaignathus[7] e Jiufengia,[44] bem como Caodeyao [en], um terocefálio não pertencente à família Akidnognathidae estreitamente relacionado ao russo Purlovia.[45] Diferentemente do mais especializado E. liuyudongi, a análise filogenética de Liu e Abdala de 2022 considerou Shiguaignathus e Jiufengia membros menos especializados (basais) de Akidnognathinae, enquanto originários do membro III mais jovem da formação. Assim, E. liuyudongi fornece evidências de um gênero de terocefálio existindo tanto no sul quanto no norte da Pangeia e de um gênero da família Akidnognathidae especializado no norte da Pangeia.[6]
Como na zona de Cistecephalus e outros paleoambientes do Permiano, os membros de Dicynodontia eram os animais mais comumente preservados na Formação Naobaogou.[8] Daqingshanodon [en] foi descrito em 1989.[43] Espécimes descobertos posteriormente consistem em pelo menos sete tipos diferentes que podem pertencer a espécies distintas, com um descrito como Turfanodon jiufengensis [en], dois relacionados a Daqingshanodon e três ou quatro relacionados a Jimusaria [en].[8] Não-sinapsídeos incluíam Gansurhinus [en],[46] Elginia wuyongae [en][47] e Laosuchus hun [en].[48]
Referências
- ↑ a b c d e f Broom, R. (1931). «Notices of some new genera and species of Karroo fossil reptiles». Records of the Albany Museum. 4 (1): 161–166
- ↑ a b c d e f g h i j k Benoit, J.; Norton, L.A.; Manger, P.R.; Rubidge, B.S. (2017). «Reappraisal of the envenoming capacity of Euchambersia mirabilis (Therapsida, Therocephalia) using μCT-scanning techniques». PLOS ONE. 12 (2): e0172047. Bibcode:2017PLoSO..1272047B. PMC 5302418
 . PMID 28187210. doi:10.1371/journal.pone.0172047
. PMID 28187210. doi:10.1371/journal.pone.0172047
- ↑ a b c d e Benoit, J. (2016). «A review of the "venomous therocephalian" hypothesis and how multiple re-portrayals of Euchambersia have influenced its success and vice versa». Bulletin de la Société Géologique de France. 187 (4): 217–224. doi:10.2113/gssgfbull.187.4-5.217
- ↑ a b c d Smith, R.; Rubidge, B.; van der Walt, M. (2011). «Therapsid Biodiversity Patterns and Palaeoenvironments of the Karoo Basin, South Africa». In: Chinsamy-Turan, A. Forerunners of Mammals: Radiation, Histology, Biology. Bloomington: Indiana University Press. pp. 31–64. ISBN 978-0-253-00533-5
- ↑ Rubidge, B.S.; Erwin, D.H.; Ramezani, J.; Bowring, S.A.; de Klerk, W.J. (2013). «High-precision temporal calibration of Late Permian vertebrate biostratigraphy: U-Pb zircon constraints from the Karoo Supergroup, South Africa». Geology. 41 (3): 363–366. Bibcode:2013Geo....41..363R. doi:10.1130/G33622.1
- ↑ a b c d e f g h i Liu, J.; Abdala, F. (2022). «The emblematic South African therocephalian Euchambersia in China: a new link in the dispersal of late Permian vertebrates across Pangea». Biology Letters. 18 (7): 20220222. PMC 9278400
 . PMID 35857894. doi:10.1098/rsbl.2022.0222
. PMID 35857894. doi:10.1098/rsbl.2022.0222
- ↑ a b Liu, J.; Abdala, F. (2017). «The tetrapod fauna of the upper Permian Naobaogou Formation of China: 1. Shiguaignathus wangi gen. et sp. nov., the first akidnognathid therocephalian from China». PeerJ. 5: e4150. PMC 5723136
 . PMID 29230374. doi:10.7717/peerj.4150
. PMID 29230374. doi:10.7717/peerj.4150
- ↑ a b c Liu, J. (2019). «The tetrapod fauna of the upper Permian Naobaogou Formation of China: 4. The diversity of dicynodonts». Vertebrata PalAsiatica. 57 (3): 173-180. doi:10.19615/j.cnki.1000-3118.190522
- ↑ Andersson, K.; Norman, D.; Werdelin, L. (2011). «Sabretoothed Carnivores and the Killing of Large Prey». PLOS ONE. 6 (10): e24971. Bibcode:2011PLoSO...624971A. PMC 3198467
 . PMID 22039403. doi:10.1371/journal.pone.0024971
. PMID 22039403. doi:10.1371/journal.pone.0024971
- ↑ a b Sues, H.-D. (1991). «Venom-conducting teeth in a Triassic reptile». Nature. 351 (6322): 141–143. Bibcode:1991Natur.351..141S. doi:10.1038/351141a0
- ↑ Kermack, D.W.; Kermack, K.A. (1984). «Dentitions, Tooth-Replacement and Jaw Articulation». The Evolution of Mammalian Characters. [S.l.]: Springer US. pp. 66–68. ISBN 978-1-4684-7819-8. doi:10.1007/978-1-4684-7817-4
- ↑ Kermack, K.A. (1956). «Tooth Replacement in Mammal-Like Reptiles of the Suborders Gorgonopsia and Therocephalia». Philosophical Transactions of the Royal Society B. 240 (670): 95–133. Bibcode:1956RSPTB.240...95K. doi:10.1098/rstb.1956.0013

- ↑ Hopson, J.A. (1964). «Tooth replacement in cynodont, dicynodont, and therocephalian reptiles». Journal of Zoology. 142 (4): 625–654. doi:10.1111/j.1469-7998.1964.tb04632.x
- ↑ a b c Benoit, J.; Manger, P.R.; Rubidge, B.R. (2016). «Palaeoneurological clues to the evolution of defining mammalian soft tissue traits». Scientific Reports. 6. 25604 páginas. Bibcode:2016NatSR...625604B. PMC 4860582
 . PMID 27157809. doi:10.1038/srep25604
. PMID 27157809. doi:10.1038/srep25604
- ↑ Boonstra, L.D. (1934). «A contribution to the morphology of the mammal-like reptiles of the suborder Therocephalia». Annals of the South African Museum. 31: 215–267
- ↑ a b c Ivakhnenko, M.F. (2008). «The First Whaitsiid (Therocephalia, Theromorpha)». Paleontological Journal. 42 (4): 409–413. doi:10.1134/S0031030108040102
- ↑ a b c Huttenlocker, A. (2009). «An investigation into the cladistic relationships and monophyly of therocephalian therapsids (Amniota: Synapsida)». Zoological Journal of the Linnean Society. 157 (4): 865–891. doi:10.1111/j.1096-3642.2009.00538.x

- ↑ a b Rubidge, B.S.; Sidor, C.A. (2001). «Evolutionary Patterns Among Permo-Triassic Therapsids». Annual Review of Ecology and Systematics. 32: 449–480. doi:10.1146/annurev.ecolsys.32.081501.114113
- ↑ Sigurdsen, T. (2006). «New features of the snout and orbit of a therocephalian therapsid from South Africa». Acta Palaeontologica Polonica. 51 (1): 63–75
- ↑ a b Huttenlocker, A.K.; Sidor, C.A. (2016). «The first karenitid (Therapsida, Therocephalia) from the upper Permian of Gondwana and the biogeography of Permo-Triassic therocephalians». Journal of Vertebrate Paleontology. 36 (4): e1111897. Bibcode:2016JVPal..36E1897H. doi:10.1080/02724634.2016.1111897
- ↑ Nopcsa, F. (1933). «On the biology of the theromorphous reptile Euchambersia». Annals and Magazine of Natural History. 10. 12 (67): 125–126. doi:10.1080/00222933308673757
- ↑ Watson, D.M.; Romer, A.S. (1956). «A classification of therapsid reptiles». Bulletin of the Museum of Comparative Zoology. 114: 35–89
- ↑ Van Valen, L. (1960). «Therapsids as Mammals». Evolution. 14 (3): 304–313. JSTOR 2405973. doi:10.2307/2405973
- ↑ a b c d Folinsbee, K.E.; Muller, J.; Reisz, R.R. (2007). «Canine Grooves: Morphology, Function, and Relevance to Venom». Journal of Vertebrate Paleontology. 27 (2): 547–551. JSTOR 30126324. doi:10.1671/0272-4634(2007)27[547:cgmfar]2.0.co;2
- ↑ Sues, H.-D. (1996). «A reptilian tooth with apparent venom canals from the Chinle Group (Upper Triassic) of Arizona». Journal of Vertebrate Paleontology. 16 (3): 571–572. doi:10.1080/02724634.1996.10011340
- ↑ Gong, E.; Martin, L.D.; Burnham, D.A.; Falk, A.R. (2009). «The birdlike raptor Sinornithosaurus was venomous». Proceedings of the National Academy of Sciences of the United States of America. 107 (2): 766–768. Bibcode:2010PNAS..107..766G. PMC 2818910
 . PMID 20080749. doi:10.1073/pnas.0912360107
. PMID 20080749. doi:10.1073/pnas.0912360107
- ↑ Huttenlocker, A.K.; Sidor, C.A.; Angielczyk, K.D. (2015). «A new eutherocephalian (Therapsida, Therocephalia) from the upper Permian Madumabisa Mudstone Formation (Luangwa Basin) of Zambia». Journal of Vertebrate Paleontology. 35 (5): e969400. Bibcode:2015JVPal..35E9400H. doi:10.1080/02724634.2015.969400
- ↑ Mitchell, J.S.; Heckert, A.B.; Sues, H.-D. (2010). «Grooves to tubes: evolution of the venom delivery system in a Late Triassic "reptile"». Naturwissenschaften. 97 (12): 1117–1121. Bibcode:2010NW.....97.1117M. PMID 21060984. doi:10.1007/s00114-010-0729-0
- ↑ Orr, C.M.; Delezene; Scott, J.E.; Tocheri, M.W.; Schwartz, G.T. (2007). «The comparative method and the inference of venom-delivery systems in fossil mammals». Journal of Vertebrate Paleontology. 27 (2): 541–546. doi:10.1671/0272-4634(2007)27[541:TCMATI]2.0.CO;2
- ↑ Vaeth, R.H.; Rossman, D.A.; Shoop, W. (1985). «Observations of Tooth Surface Morphology in Snakes». Journal of Herpetology. 19 (1): 20–26. JSTOR 1564416. doi:10.2307/1564416
- ↑ Bellairs, A.D'A. (1949). «Observations on the snout of Varanus, and a comparison with that of other lizards and snakes». Journal of Anatomy. 83 (2): 116–146. PMC 1273152
 . PMID 17105074
. PMID 17105074
- ↑ Abdel-Kader, T.G.; Ali, R.S.; Ibrahim, N.M. (2011). «The Cranial Nerves of Mabuya quinquetaeniata III: Nervus Trigeminus» (PDF). Life Science Journal. 8 (4): 650–669
- ↑ Leitch, D.B.; Catania, K.C. (2012). «Structure, innervation and response properties of integumentary sensory organs in crocodilians». Journal of Experimental Biology. 215 (23): 4217–4230. PMC 4074209
 . PMID 23136155. doi:10.1242/jeb.076836
. PMID 23136155. doi:10.1242/jeb.076836
- ↑ Bücherl, W. (1968). «Introduction». In: Bücherl, W.; Buckley, E.E.; Deulofeu, V. Venomous Animals and their Venoms. 1. New York: Academic Press. pp. 9–12. ISBN 9781483229492. doi:10.1016/B978-1-4832-2949-2.50006-0
- ↑ Fry, B.G.; Wroe, S.; Teeuwisse, W.; van Osch, M.J.P.; Moreno, K.; Ingle, J.; McHenry, C.; Ferrara, T.; Clausen, P.; Scheib, H.; Winter, K.L.; Greisman, L.; Roelants, K.; van der Weerd, L.; Clemente, C.J.; Giannakis, E. (2009). «A central role for venom in predation by Varanus komodoensis (Komodo Dragon) and the extinct giant Varanus (Megalania) priscus». Proceedings of the National Academy of Sciences of the United States of America. 106 (22): 8969–8974. Bibcode:2009PNAS..106.8969F. PMC 2690028
 . PMID 19451641. doi:10.1073/pnas.0810883106
. PMID 19451641. doi:10.1073/pnas.0810883106
- ↑ Ligabue-Braun, R.; Verli, H.; Carlini, C.R. (2012). «Venomous mammals: A review». Toxicon. 59 (7): 680–695. PMID 22410495. doi:10.1016/j.toxicon.2012.02.012
- ↑ Weinstein, S.A.; Smith, T.L.; Kardong, K.V. (2009). «Reptile Venom Glands: Form, Function, and Future» (PDF). In: Mackessy, S.P. Handbook of Venoms and Toxins of Reptiles. Boca Raton: CRC Press. pp. 65–91
- ↑ Goris, R.C. (2011). «Infrared Organs of Snakes: An Integral Part of Vision». Journal of Herpetology. 45 (1): 2–14. doi:10.1670/10-238.1
- ↑ Krochmal, A.R.; Bakken, G.S.; LaDuc, T.J. (2004). «Heat in evolution's kitchen: evolutionary perspectives on the functions and origin of the facial pit of pitvipers (Viperidae: Crotalinae)». Journal of Experimental Biology. 207 (24): 4231–4238. PMID 15531644. doi:10.1242/jeb.01278

- ↑ Benoit, J.; Abdala, F.; Manger, P.R.; Rubidge, B.S. (2016). «The Sixth Sense in Mammalian Forerunners: Variability of the Parietal Foramen and the Evolution of the Pineal Eye in South African Permo-Triassic Eutheriodont Therapsids». Acta Palaeontologica Polonica. 61 (4): 777–789. doi:10.4202/app.00219.2015

- ↑ Anderson, J.M. (1977). «The microfloral succession: conclusions and discussion». A Review of Gondwana Permian Palynology with Particular Reference to the Northern Karoo Basin of South Africa. Col: Memoirs of the Botanical Survey of South Africa. 41. [S.l.]: Botanical Research Institute. pp. 42–58
- ↑ Liu, J.; Li, L. (2013). «Large Tetrapod Burrows from the Permian Naobaogou Formation of the Daqingshan Area, Nei Mongol, China». Acta Geologica Sinica. 87 (6): 1501–1507. doi:10.1111/1755-6724.12154
- ↑ a b Zhu, Y.L. (1989). «The discovery of dicynodonts in Daqingshan Mountain, Nei Mongol (Inner Mongolia)» (PDF). Vertebrata PalAsiatica. 27 (1): 9–27
- ↑ Liu, J.; Abdala, F. (2019). «The tetrapod fauna of the upper Permian Naobaogou Formation of China: 3. Jiufengia jiai gen. et sp. nov., a large akidnognathid therocephalian». PeerJ. 7: e6463. PMC 6388668
 . PMID 30809450. doi:10.7717/peerj.6463
. PMID 30809450. doi:10.7717/peerj.6463
- ↑ Liu, J.; Abdala, F. (2020). «The tetrapod fauna of the upper Permian Naobaogou Formation of China: 5. Caodeyao liuyufengi gen. et sp. nov., a new peculiar therocephalian». PeerJ. 8: e9160. PMC 7261480
 . PMID 32523808. doi:10.7717/peerj.9160
. PMID 32523808. doi:10.7717/peerj.9160
- ↑ Reisz, R.R.; Liu, J.; Li, J.-L.; Müller, J. (2011). «A new captorhinid reptile, Gansurhinus qingtoushanensis, gen. et sp. nov., from the Permian of China». Naturwissenschaften. 98 (5): 435–441. Bibcode:2011NW.....98..435R. PMID 21484260. doi:10.1007/s00114-011-0793-0
- ↑ Liu, J.; Bever, G.S. (2018). «The tetrapod fauna of the upper Permian Naobaogou Formation of China: a new species of Elginia (Parareptilia, Pareiasauria)». Papers in Palaeontology. 4 (2): 197–209. doi:10.1002/spp2.1105
- ↑ Liu, J.; Chen, J. (2018). «The tetrapod fauna of the upper Permian Naobaogou Formation of China: 7. Laosuchus hun sp. nov. (Chroniosuchia) and interrelationships of chroniosuchians». Journal of Systematic Palaeontology. 18 (24): 2043–2058. doi:10.1080/14772019.2021.1873435


