Estrutura e genoma do HIV
Genoma e proteínas do HIV (vírus da imunodeficiência humana) têm sido objeto de extensa pesquisa desde a descoberta do vírus em 1983.[1][2]
Na busca pelo agente causador, acreditava-se inicialmente que o vírus era uma forma do vírus da leucemia de células T humanas (HTLV), o qual, na época, era conhecido por afetar o sistema imunológico humano e causar certas leucemias. Contudo, pesquisadores do Instituto Pasteur em Paris isolaram um retrovírus anteriormente desconhecido e geneticamente distinto em pacientes com AIDS, que mais tarde foi denominado HIV.[3]
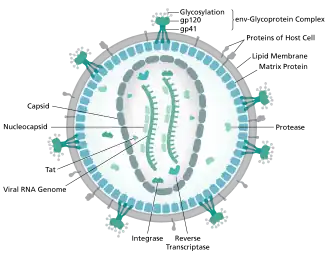
Cada vírion é composto por um envelope viral e uma matriz associada que envolve um cápside, a qual, por sua vez, contém duas cópias do genoma de RNA de fita simples e diversas enzimas. A descoberta do próprio vírus ocorreu dois anos após o relato dos primeiros casos significativos de doenças associadas à AIDS.[4][5]
Estrutura
.jpg)
A sequência completa do genoma do HIV-1, extraída de vírions infecciosos, foi solucionada com resolução de nucleotídeo único.[6] O genoma do HIV codifica um pequeno número de proteína virals, estabelecendo invariavelmente associações cooperativas entre as proteínas do HIV e entre o HIV e as proteínas do hospedeiro, para invadir células hospedeiras e sequestrar suas máquinas internas.[7] O HIV apresenta uma estrutura diferente de outros retrovírus. O vírion do HIV tem aproximadamente 100 nm de diâmetro. Sua região mais interna consiste em um núcleo em forma de cone que inclui duas cópias do genoma de ssRNA (sentido positivo), as enzimas transcriptase reversa, integrase e protease, algumas proteínas menores e a principal proteína do núcleo.[8] O genoma do vírus da imunodeficiência humana (HIV) codifica 8 proteínas virais que desempenham papéis essenciais durante o ciclo de vida do HIV.[7]
O HIV-1 é composto por duas cópias de RNA de fita simples, ligadas não covalentemente, não empalhadas e de sentido positivo, encerradas por um cápside cônico composto pela proteína viral p24, típica dos lentivírus.[9][10] Os dois RNAs são frequentemente idênticos, mas não são independentes, formando um dímero compacto dentro do vírion.[11] Várias razões para a inclusão de duas cópias de RNA, em vez de apenas uma, foram propostas, possivelmente incluindo uma combinação destas vantagens: uma vantagem é que as duas cópias das cadeias de RNA são vitais para contribuir com a recombinação do HIV-1, que ocorre durante a transcrição reversa na replicação viral, aumentando assim a diversidade genética.[11] Outra vantagem é que ter duas cópias de RNA permitiria à transcriptase reversa trocar de molde ao encontrar uma quebra no RNA viral, completando assim a transcrição reversa sem perda de informação genética.[11] Outra razão é que a natureza dimerizada do genoma de RNA do vírus pode desempenhar um papel estrutural na replicação viral.[11] A contenção de duas cópias de RNA de fita simples dentro de um vírion, mas a produção de apenas um provírus de DNA, é denominada pseudodiploidia.[12] O componente de RNA tem 9749 nucleotídeos de comprimento[13][14] e possui uma [[capa 5']|capa 5']] (Gppp), uma cauda poli(A) e muitos quadros de leitura abertos (ORFs).[15] Proteínas estruturais virais são codificadas por ORFs longos, enquanto ORFs menores codificam reguladores do ciclo de vida viral: adesão, fusão de membrana, replicação e montagem.[15]
O RNA de fita simples está fortemente ligado às proteínas do nucleocapsídeo p7, à proteína de montagem tardia p6 e às enzimas essenciais para o desenvolvimento do vírion, como a transcriptase reversa e a integrase. O tRNA de lisina é o primer da transcriptase reversa dependente de magnésio.[9] O nucleocapsídeo associa-se ao RNA genômico (uma molécula por hexâmero) e protege o RNA da digestão por nucleases. Também contidos na partícula do vírion estão o Vif, o Vpr, o Nef e a protease viral.[carece de fontes] O envelope viral do vírion é formado por uma membrana plasmática de origem da célula hospedeira, sustentada por uma matriz composta pela proteína viral p17, garantindo a integridade da partícula do vírion. Na superfície do vírion pode ser encontrada uma quantidade limitada de glicoproteína (Env) do envelope do HIV, um trímero formado por heterodímeros de gp120 e gp41.[16]
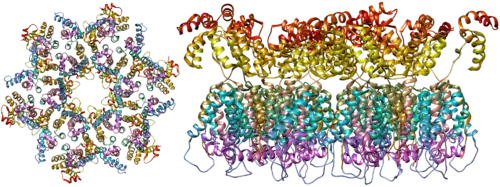
Como as únicas proteínas na superfície do vírus, as glicoproteínas do envelope (gp120 e gp41) são os principais alvos para os esforços de vacina contra o HIV.[17] Mais da metade da massa do espinho do envelope trímero é composta por glicanos N-ligados. A densidade é alta, pois os glicanos protegem a proteína viral subjacente da neutralização por anticorpos. Esta é uma das moléculas mais densamente glicosiladas conhecidas e a densidade é suficientemente alta para impedir o processo normal de maturação dos glicanos durante a biogênese no retículo endoplasmático e no complexo de Golgi.[18][19] A maioria dos glicanos, portanto, permanece como glicanos imaturos "altamente manose", não normalmente presentes em glicoproteínas humanas secretadas ou na superfície celular.[20] O processamento incomum e a alta densidade fazem com que quase todos os anticorpos amplamente neutralizantes identificados até agora (de um subconjunto de pacientes infectados por muitos meses a anos) se liguem ou sejam adaptados para lidar com esses glicanos do envelope.[21]
A estrutura molecular do espinho viral foi determinada por cristalografia de raios-X[22] e por microscopia crioeletrônica.[23] Esses avanços em biologia estrutural foram possibilitados pelo desenvolvimento de formas recombinantes estáveis do espinho viral, por meio da introdução de uma ligação dissulfeto intersubunidade e de uma mutação de isoleucina para prolina em gp41.[24] Os chamados trímeros SOSIP não apenas reproduzem as propriedades antigênicas do espinho viral nativo, mas também exibem o mesmo grau de glicanos imaturos apresentados no vírus nativo.[25] Espinhos virais trímeros recombinantes são candidatos promissores para vacinas, pois exibem menos epítopos não neutralizantes do que o gp120 monomérico recombinante, o qual atua para suprimir a resposta imune aos epítopos-alvo.[26]
Organização do genoma
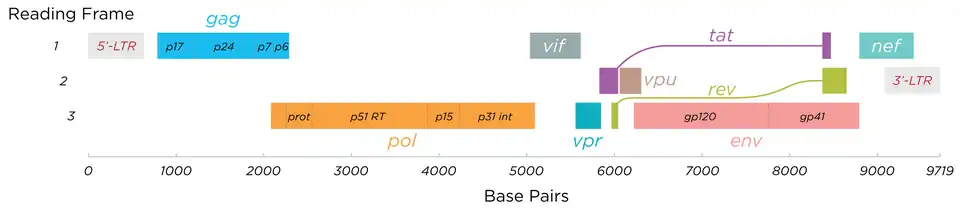
O HIV possui vários genes principais que codificam proteínas estruturais encontradas em todos os retrovírus, bem como vários genes não estruturais (acessórios) exclusivos do HIV.[27] O genoma do HIV contém nove genes que codificam quinze proteínas virais.[28] Estes genes são sintetizados como poliproteínas que produzem proteínas para o interior do vírion, denominadas Gag (antígeno de grupo específico); as enzimas virais (Pol, polimerase) ou as glicoproteínas do vírion env (envelope).[29] Além destes, o HIV também codifica proteínas que possuem funções regulatórias e auxiliares.[29] O HIV-1 possui dois elementos regulatórios importantes: Tat e Rev, e algumas proteínas acessórias importantes, como Nef, Vpr, Vif e Vpu, que não são essenciais para a replicação em certos tecidos.[29] O gene gag fornece a infraestrutura física básica do vírus, enquanto o gene pol fornece o mecanismo fundamental pelo qual os retrovírus se reproduzem, enquanto os demais auxiliam o HIV a penetrar na célula hospedeira e potencializam sua reprodução. Embora possam ser alterados por mutação, todos esses genes, exceto o tev, existem em todas as variantes conhecidas do HIV; ver Variabilidade genética do HIV.[carece de fontes]
O HIV emprega um sofisticado sistema de splicing de RNA diferencial para obter nove produtos gênicos diferentes a partir de um genoma com menos de 10 kb.[30] O HIV possui uma transcrição genômica não empalhada de 9,2 kb que codifica os precursores de gag e pol; uma transcrição empalhada única de 4,5 kb que codifica env, Vif, Vpr e Vpu; e um mRNA multiplemente empalhado de 2 kb que codifica Tat, Rev e Nef.[30]
| Classe | Nome do gene | Produtos proteicos primários | Produtos proteicos processados |
|---|---|---|---|
| Proteínas estruturais virais | gag | Poliproteína Gag | MA, CA, SP1, NC, SP2, P6 |
| pol | Poliproteína Pol | RT, RNase H, IN, PR | |
| env | gp160 | gp120, gp41 | |
| Elementos regulatórios essenciais | tat | Tat | |
| rev | Rev | ||
| Proteínas regulatórias acessórias | nef | Nef | |
| vpr | Vpr | ||
| vif | Vif | ||
| vpu | Vpu |
Proteínas estruturais virais
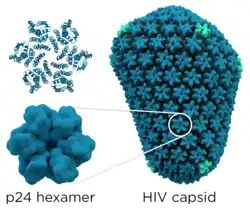
- gag (antígeno de grupo específico) codifica a poliproteína precursora do gag, que é processada pela protease viral durante a maturação em MA (proteína de matriz retroviral, p17); CA (proteína do cápside, p24); SP1 (peptídeo espaçador 1, p2); NC (proteína do nucleocapsídeo, p7); SP2 (peptídeo espaçador 2, p1) e a proteína P6.[31]
- pol codifica as enzimas virais transcriptase reversa (RT) e RNase H, integrase (IN) e protease do HIV (PR).[29]
A protease do HIV é necessária para clivar a poliproteína precursora Gag para produzir proteínas estruturais, a RT é responsável por transcrever DNA a partir de um molde de RNA, e a IN é essencial para integrar o DNA viral de fita dupla ao genoma do hospedeiro.[27]
- env (de "envelope") codifica o gp160, que é clivado por uma protease hospedeira, a furina, no retículo endoplasmático da célula hospedeira. O processamento pós-traducional resulta em uma glicoproteína de superfície, gp120 ou SU, que se liga aos receptores CD4 presentes nos linfócitos, e em gp41 ou TM, que se incorpora ao envelope viral para permitir que o vírus se ligue e fundir com as células-alvo.[27][31]
Elementos regulatórios essenciais
- tat (transativador do HIV) desempenha um papel importante na regulação da transcrição reversa do RNA do genoma viral, assegurando a síntese eficiente de mRNAs virais e regulando a liberação de vírions por células infectadas.[29]
O Tat é expresso tanto como um Tat de um exon com 72 aminoácidos quanto como um Tat de dois exons com 86–101 aminoácidos, desempenhando papel fundamental no início da infecção pelo HIV. O Tat (14–15 kDa) se liga à estrutura secundária em stem-loop do RNA genômico, próxima à região 5' do LTR, formando o elemento de resposta de transativação (TAR).[9][29]
- rev (regulador da expressão de proteínas do vírion): A proteína Rev se liga ao genoma viral por meio de um motivo de ligação a RNA rico em arginina, que também atua como sinal de localização nuclear (NLS), sendo necessário para o transporte do Rev do citosol para o núcleo durante a replicação viral.[29]
O Rev reconhece uma estrutura complexa em stem-loop do mRNA env, localizada no íntron que separa os exons codificadores do Tat e do Rev, conhecida como elemento de resposta do Rev do HIV (RRE).[9][29] O Rev é crucial para a síntese das principais proteínas virais e, portanto, essencial para a replicação viral.[carece de fontes]
Proteínas regulatórias acessórias
- vpr (proteína R dos lentivírus): O Vpr é uma proteína regulatória associada ao vírion, que realiza transporte nucleocitoplasmático.[29] Acredita-se que desempenhe um papel importante na replicação do vírus, especificamente na importação nuclear do complexo de pré-integração. O Vpr também parece induzir a parada do ciclo celular das células hospedeiras na fase G2, o que ativa o maquinário de reparo do DNA, possibilitando a integração do DNA viral.[9]
HIV-2 e SIV codificam uma proteína adicional relacionada ao Vpr, chamada Vpx, que atua em conjunto com o Vpr.[29]
- vif – O Vif é uma sequência conservada altamente conservada, uma fosfoproteína de 23 kDa, importante para a infectividade dos vírions do HIV-1 em função do tipo celular.[9] Estudos demonstraram que o HIV-1 necessita do Vif para sintetizar vírus infecciosos em linfócitos, macrófagos e em determinadas linhas celulares humanas, mas não aparenta necessitar dele em células HeLa ou COS, entre outras.[29]
- nef – O Nef, fator negativo, é uma fosfoproteína associada à membrana, myristoilada no terminal N, envolvida em múltiplas funções durante o ciclo replicativo do vírus. Acredita-se que desempenhe papel importante na apoptose celular e no aumento da infectividade viral.[29]
- vpu (proteína U do vírus) – O Vpu é específico do HIV-1. Trata-se de uma fosfoproteína de membrana integral oligomérica de classe I, com diversas funções biológicas. O Vpu participa da degradação do CD4 por meio da via do ubiquitina e do proteassoma, além de facilitar a liberação bem-sucedida de vírions por células infectadas.[9][29]
- tev: Este gene está presente apenas em alguns isolados de HIV-1. É uma fusão de partes dos genes tat, env e rev, e codifica uma proteína que apresenta algumas propriedades do tat, mas poucas ou nenhumas das propriedades do rev.[32]
Estrutura secundária do RNA
Vários elementos conservados de estrutura secundária foram identificados no genoma de RNA do HIV. As estruturas do RNA viral do HIV regulam o andamento da transcrição reversa.[33] A estrutura da UTR 5' consiste em uma série de estruturas stem-loop conectadas por pequenos conectores.[10] Esses stem-loops (do 5' para o 3') incluem o elemento de transativação (TAR), o sinal de poliadenilação 5' [poly(A)], o PBS, o DIS, o principal SD e a estrutura em forma de ψ (elemento de empacotamento psi) localizada na extremidade 5' do genoma, bem como o elemento de resposta do Rev do HIV (RRE) presente no gene env.[10][34][35] Outra estrutura de RNA identificada é o stem-loop 3 do gag (GSL3), que se acredita estar envolvida no empacotamento viral.[36][37] Estruturas secundárias de RNA foram propostas para afetar o ciclo de vida do HIV ao alterar a função da protease do HIV-1 e da transcriptase reversa, embora nem todos os elementos identificados tenham função definida.[carece de fontes]
Uma estrutura secundária de RNA, determinada por análise SHAPE, demonstrou conter três stem-loops e está localizada entre os genes da protease do HIV e da transcriptase reversa. Este RNA regulatório cis mostrou-se conservado em toda a família do HIV e acredita-se que influencie o ciclo de vida viral.[38]
Loop V3
O terceiro loop variável ou loop V3 é uma parte ou região do Vírus da Imunodeficiência Humana. O loop V3 da glicoproteína do envelope do vírion, gp120, permite que o vírus infecte células do sistema imune humano ao se ligar a um receptor de citocina na célula-alvo, como uma célula CCR5 ou CXCR4, dependendo da cepa do HIV.[39] A glicoproteína do envelope (Env) gp120/41 é essencial para a entrada do HIV-1 nas células. O Env serve como alvo molecular para medicamentos que tratam indivíduos com infecção por HIV-1 e como fonte de imunógeno para o desenvolvimento de vacinas contra a AIDS. Contudo, a estrutura do trímero funcional do Env continua evasiva.[40]
Referências
- ↑ Barré-Sinoussi F, Chermann JC, Rey F, Nugeyre MT, Chamaret S, Gruest J, Dauguet C, Axler-Blin C, Vézinet-Brun F, Rouzioux C, Rozenbaum W, Montagnier L (maio de 1983). «Isolamento de um retrovírus T-limfotrópico de um paciente em risco para síndrome da imunodeficiência adquirida (AIDS)». Science. 220 (4599): 868–71. Bibcode:1983Sci...220..868B. PMID 6189183. doi:10.1126/science.6189183
- ↑ Gallo RC, Sarin PS, Gelmann EP, Robert-Guroff M, Richardson E, Kalyanaraman VS, Mann D, Sidhu GD, Stahl RE, Zolla-Pazner S, Leibowitch J, Popovic M (maio de 1983). «Isolamento do vírus da leucemia de células T humanas na síndrome da imunodeficiência adquirida (AIDS)». Science. 220 (4599): 865–7. Bibcode:1983Sci...220..865G. PMID 6601823. doi:10.1126/science.6601823
- ↑ Churi C, Ross MW (2015). «Hiv/Aids». In: Whelehan P, Bolin A. The international encyclopedia of human sexuality. Wiley. ISBN 9781405190060. OCLC 949701914
- ↑ Centers for Disease Control (junho de 1981). «Pneumocystis pneumonia--Los Angeles». MMWR. Morbidity and Mortality Weekly Report. 30 (21): 250–2. PMID 6265753
- ↑ Centers for Disease Control (CDC) (julho de 1981). «Sarcoma de Kaposi e pneumonia por Pneumocystis entre homens homossexuais – Nova York e Califórnia» (PDF). MMWR. Morbidity and Mortality Weekly Report. 30 (25): 305–8. PMID 6789108. Consultado em 15 de setembro de 2017. Arquivado do original em 22 de outubro de 2012
- ↑ Watts JM, Dang KK, Gorelick RJ, Leonard CW, Bess JW, Swanstrom R, Burch CL, Weeks KM (agosto de 2009). «Arquitetura e estrutura secundária de um genoma completo de RNA do HIV-1». Nature. 460 (7256): 711–6. Bibcode:2009Natur.460..711W. PMC 2724670
 . PMID 19661910. doi:10.1038/nature08237
. PMID 19661910. doi:10.1038/nature08237
- ↑ a b Li G, De Clercq E (setembro de 2016). «Associações de proteínas em todo o genoma do HIV: uma revisão de 30 anos de pesquisa». Microbiology and Molecular Biology Reviews. 80 (3): 679–731. PMC 4981665
 . PMID 27357278. doi:10.1128/MMBR.00065-15
. PMID 27357278. doi:10.1128/MMBR.00065-15
- ↑ Singleton P, Sainsbury D, eds. (2006). «Hiv». Dictionary of microbiology & molecular biology 3rd ed. Hoboken, NJ: Wiley. ISBN 9780470035450. OCLC 71223221
- ↑ a b c d e f g Montagnier L (1999). «Human Immunodeficiency Viruses (Retroviridae)». Encyclopedia of Virology 2nd ed. pp. 763–774
- ↑ a b c Lu K, Heng X, Summers MF (julho de 2011). «Determinantes estruturais e mecanismo de empacotamento do genoma do HIV-1». Journal of Molecular Biology. 410 (4): 609–33. PMC 3139105
 . PMID 21762803. doi:10.1016/j.jmb.2011.04.029
. PMID 21762803. doi:10.1016/j.jmb.2011.04.029
- ↑ a b c d Moore, Michael D.; Hu, Wei Shau (2009). «HIV-1 RNA dimerization: It takes two to tango». AIDS Reviews. 11 (2): 91–102. ISSN 1139-6121. PMC 3056336
 . PMID 19529749
. PMID 19529749
- ↑ Hwang CK, Svarovskaia ES, Pathak VK (outubro de 2001). «Dynamic copy choice: steady state between murine leukemia virus polymerase and polymerase-dependent RNase H activity determines frequency of in vivo template switching». Proceedings of the National Academy of Sciences of the United States of America. 98 (21): 12209–14. Bibcode:2001PNAS...9812209H. PMC 59793
 . PMID 11593039. doi:10.1073/pnas.221289898
. PMID 11593039. doi:10.1073/pnas.221289898
- ↑ Wain-Hobson S, Sonigo P, Danos O, Cole S, Alizon M (janeiro de 1985). «Nucleotide sequence of the AIDS virus, LAV». Cell. 40 (1): 9–17. PMID 2981635. doi:10.1016/0092-8674(85)90303-4
- ↑ Ratner L, Haseltine W, Patarca R, Livak KJ, Starcich B, Josephs SF, Doran ER, Rafalski JA, Whitehorn EA, Baumeister K (1985). «Complete nucleotide sequence of the AIDS virus, HTLV-III». Nature. 313 (6000): 277–84. Bibcode:1985Natur.313..277R. PMID 2578615. doi:10.1038/313277a0
- ↑ a b Castelli JC, Levy A (2002). «HIV (Human Immunodeficiency Virus)». Encyclopedia of Cancer. 2 2nd ed. pp. 407–415
- ↑ Checkly MA, Freed EO (22 de julho de 2011). «HIV-1 envelope glycoprotein biosynthesis, trafficking, and incorporation». Journal of Molecular Biology (em inglês). 410 (4): 582–608. PMC 3139147
 . PMID 21762802. doi:10.1016/j.jmb.2011.04.042
. PMID 21762802. doi:10.1016/j.jmb.2011.04.042
- ↑ National Institute of Health (17 de junho de 1998). «Crystal structure of key HIV protein reveals new prevention, treatment targets» (Nota de imprensa). Consultado em 14 de setembro de 2006. Cópia arquivada em 19 de fevereiro de 2006
- ↑ Behrens AJ, Vasiljevic S, Pritchard LK, Harvey DJ, Andev RS, Krumm SA, Struwe WB, Cupo A, Kumar A, Zitzmann N, Seabright GE, Kramer HB, Spencer DI, Royle L, Lee JH, Klasse PJ, Burton DR, Wilson IA, Ward AB, Sanders RW, Moore JP, Doores KJ, Crispin M (março de 2016). «Composition and Antigenic Effects of Individual Glycan Sites of a Trimeric HIV-1 Envelope Glycoprotein». Cell Reports (em inglês). 14 (11): 2695–706. PMC 4805854
 . PMID 26972002. doi:10.1016/j.celrep.2016.02.058
. PMID 26972002. doi:10.1016/j.celrep.2016.02.058
- ↑ Pritchard LK, Spencer DI, Royle L, Bonomelli C, Seabright GE, Behrens AJ, Kulp DW, Menis S, Krumm SA, Dunlop DC, Crispin DJ, Bowden TA, Scanlan CN, Ward AB, Schief WR, Doores KJ, Crispin M (junho de 2015). «Agrupamento de glicanos estabiliza a mancha de manose do HIV-1 e preserva a vulnerabilidade a anticorpos amplamente neutralizantes». Nature Communications. 6. 7479 páginas. Bibcode:2015NatCo...6.7479P. PMC 4500839
 . PMID 26105115. doi:10.1038/ncomms8479
. PMID 26105115. doi:10.1038/ncomms8479
- ↑ Pritchard LK, Harvey DJ, Bonomelli C, Crispin M, Doores KJ (setembro de 2015). «Glicosilação dirigida pela célula e pela proteína do envelope nativo clivado do HIV-1». Journal of Virology. 89 (17): 8932–44. PMC 4524065
 . PMID 26085151. doi:10.1128/JVI.01190-15
. PMID 26085151. doi:10.1128/JVI.01190-15
- ↑ Crispin M, Doores KJ (abril de 2015). «Targeting host-derived glycans on enveloped viruses for antibody-based vaccine design». Current Opinion in Virology. Viral pathogenesis • Preventive and therapeutic vaccines. 11: 63–9. PMC 4827424
 . PMID 25747313. doi:10.1016/j.coviro.2015.02.002
. PMID 25747313. doi:10.1016/j.coviro.2015.02.002
- ↑ Julien JP, Cupo A, Sok D, Stanfield RL, Lyumkis D, Deller MC, Klasse PJ, Burton DR, Sanders RW, Moore JP, Ward AB, Wilson IA (dezembro de 2013). «Estrutura cristalina de um trímero do envelope do HIV-1 solúvel e clivado». Science. 342 (6165): 1477–83. Bibcode:2013Sci...342.1477J. PMC 3886632
 . PMID 24179159. doi:10.1126/science.1245625
. PMID 24179159. doi:10.1126/science.1245625
- ↑ Lyumkis D, Julien JP, de Val N, Cupo A, Potter CS, Klasse PJ, Burton DR, Sanders RW, Moore JP, Carragher B, Wilson IA, Ward AB (dezembro de 2013). «Estrutura por Crio-EM de um trímero do envelope do HIV-1 solúvel, clivado e completamente glicosilado». Science. 342 (6165): 1484–90. Bibcode:2013Sci...342.1484L. PMC 3954647
 . PMID 24179160. doi:10.1126/science.1245627
. PMID 24179160. doi:10.1126/science.1245627
- ↑ Sanders RW, Derking R, Cupo A, Julien JP, Yasmeen A, de Val N, Kim HJ, Blattner C, de la Peña AT, Korzun J, Golabek M, de Los Reyes K, Ketas TJ, van Gils MJ, King CR, Wilson IA, Ward AB, Klasse PJ, Moore JP (setembro de 2013). «Um trímero do envelope do HIV-1 clivado, solúvel e de nova geração, BG505 SOSIP.664 gp140, expressa múltiplos epítopos para anticorpos amplamente neutralizantes, mas não para anticorpos não neutralizantes». PLOS Pathogens. 9 (9): e1003618. PMC 3777863
 . PMID 24068931. doi:10.1371/journal.ppat.1003618
. PMID 24068931. doi:10.1371/journal.ppat.1003618
- ↑ Pritchard LK, Vasiljevic S, Ozorowski G, Seabright GE, Cupo A, Ringe R, Kim HJ, Sanders RW, Doores KJ, Burton DR, Wilson IA, Ward AB, Moore JP, Crispin M (junho de 2015). «Restrições estruturais determinam a glicosilação dos trímeros do envelope do HIV-1». Cell Reports. 11 (10): 1604–13. PMC 4555872
 . PMID 26051934. doi:10.1016/j.celrep.2015.05.017
. PMID 26051934. doi:10.1016/j.celrep.2015.05.017
- ↑ de Taeye SW, Ozorowski G, Torrents de la Peña A, Guttman M, Julien JP, van den Kerkhof TL, Burger JA, Pritchard LK, Pugach P, Yasmeen A, Crampton J, Hu J, Bontjer I, Torres JL, Arendt H, DeStefano J, Koff WC, Schuitemaker H, Eggink D, Berkhout B, Dean H, LaBranche C, Crotty S, Crispin M, Montefiori DC, Klasse PJ, Lee KK, Moore JP, Wilson IA, Ward AB, Sanders RW (dezembro de 2015). «Imunogenicidade de trímeros do envelope do HIV-1 estabilizados com exposição reduzida de epítopos não neutralizantes». Cell. 163 (7): 1702–15. PMC 4732737
 . PMID 26687358. doi:10.1016/j.cell.2015.11.056
. PMID 26687358. doi:10.1016/j.cell.2015.11.056
- ↑ a b c Mushahwar IK (2007). «Human Immunodeficiency Viruses: Molecular Virology, pathogenesis, diagnosis and treatment». Perspectives in Medical Virology. 13: 75–87. ISBN 9780444520739. doi:10.1016/S0168-7069(06)13005-0
- ↑ Li G, Piampongsant S, Faria NR, Voet A, Pineda-Peña AC, Khouri R, Lemey P, Vandamme AM, Theys K (fevereiro de 2015). «Um mapa integrado da variação do genoma do HIV sob uma perspectiva populacional». Retrovirology (em inglês). 12 (1). 18 páginas. PMC 4358901
 . PMID 25808207. doi:10.1186/s12977-015-0148-6
. PMID 25808207. doi:10.1186/s12977-015-0148-6
- ↑ a b c d e f g h i j k l m Votteler J, Schubert U (2008). «Human Immunodeficiency Viruses: Molecular Biology». Encyclopedia of Virology 3rd ed. pp. 517–525
- ↑ a b Feinberg MB, Greene WC (1992). «Insights moleculares na patogênese do vírus da imunodeficiência humana tipo 1». Current Opinion in Immunology. 4 (4): 466–474. PMID 1356348. doi:10.1016/s0952-7915(06)80041-5
- ↑ a b King SR (1994). «HIV: Virology and Mechanisms of disease». Annals of Emergency Medicine. 24 (3): 443–449. PMID 7915889. doi:10.1016/s0196-0644(94)70181-4
- ↑ Benko DM, Schwartz S, Pavlakis GN, Felber BK (junho de 1990). «Uma nova proteína do vírus da imunodeficiência humana tipo 1, tev, compartilha sequências com as proteínas tat, env e rev». Journal of Virology. 64 (6): 2505–18. PMC 249426
 . PMID 2186172. doi:10.1128/JVI.64.6.2505-2518.1990
. PMID 2186172. doi:10.1128/JVI.64.6.2505-2518.1990
- ↑ Krupkin M, Jackson LN, Ha B, Puglisi EV (dezembro de 2020). «Avanços na compreensão da iniciação da transcrição reversa do HIV-1». Curr Opin Struct Biol. 65: 175–183. PMC 9973426
 . PMID 32916568. doi:10.1016/j.sbi.2020.07.005
. PMID 32916568. doi:10.1016/j.sbi.2020.07.005
- ↑ Berkhout B (janeiro de 1992). «Características estruturais no RNA TAR dos vírus da imunodeficiência humana e símios: uma análise filogenética». Nucleic Acids Research. 20 (1): 27–31. PMC 310321
 . PMID 1738599. doi:10.1093/nar/20.1.27
. PMID 1738599. doi:10.1093/nar/20.1.27
- ↑ Paillart JC, Skripkin E, Ehresmann B, Ehresmann C, Marquet R (fevereiro de 2002). «Evidência in vitro para um pseudonódo de longo alcance nas regiões não traduzidas e de codificação de matriz do RNA genômico do HIV-1». The Journal of Biological Chemistry. 277 (8): 5995–6004. PMID 11744696. doi:10.1074/jbc.M108972200

- ↑ Damgaard CK, Andersen ES, Knudsen B, Gorodkin J, Kjems J (fevereiro de 2004). «Interações de RNA na região 5' do genoma do HIV-1». Journal of Molecular Biology. 336 (2): 369–79. PMID 14757051. doi:10.1016/j.jmb.2003.12.010
- ↑ Rong L, Russell RS, Hu J, Laughrea M, Wainberg MA, Liang C (setembro de 2003). «Exclusão do stem-loop 3 é compensada por mutações de segundo sítio na proteína Gag do vírus da imunodeficiência humana tipo 1». Virology. 314 (1): 221–8. PMID 14517075. doi:10.1016/S0042-6822(03)00405-7
- ↑ Wang Q, Barr I, Guo F, Lee C (dezembro de 2008). «Evidência de uma nova estrutura secundária de RNA na região codificadora do gene pol do HIV-1». RNA. 14 (12): 2478–88. PMC 2590956
 . PMID 18974280. doi:10.1261/rna.1252608
. PMID 18974280. doi:10.1261/rna.1252608
- ↑ «The interactions of the gp120 V3 loop of different HIV-1 strains with the potent anti-HIV human monoclonal antibody 447-52D». Weizmann Institute of Science: Department of Structural Biology. Consultado em 18 de abril de 2017. Arquivado do original em 18 de julho de 2007
- ↑ Takeda S, Takizawa M, Miyauchi K, Urano E, Fujino M, Murakami T, Murakami T, Komano J (junho de 2016). «Propriedades conformacionais do terceiro loop variável da glicoproteína do envelope do HIV-1AD8 em condições ligadas». Biochemical and Biophysical Research Communications. 475 (1): 113–8. PMID 27178216. doi:10.1016/j.bbrc.2016.05.051
Ligações externas
- Entrada no Rfam para o loop haste-alça do HIV pol-1
- Modelo 3D do vírion completo do HIV-1
- Liu J, Wright ER, Winkler H (2010). «Visualização 3D de Vírions de HIV por Tomografia Crioeletrônica». Crio-EM, Parte C: Análises, Interpretação e Estudos de Caso. Col: Methods in Enzymology. 483. [S.l.: s.n.] pp. 267–90. ISBN 9780123849939. PMC 3056484
 . PMID 20888479. doi:10.1016/S0076-6879(10)83014-9
. PMID 20888479. doi:10.1016/S0076-6879(10)83014-9