Entecavir
Entecavir
| |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
 | |||||||||||||||||||
| Nomes | |||||||||||||||||||
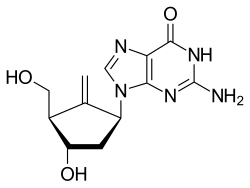
| Nome IUPAC | 2-Amino-9-[(1S,3R,4S)-4-hydroxy-3-(hydroxymethyl)-2-methylidenecyclopentyl]-1H-purin-6-one | ||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||
O entecavir (ETV), comercializado sob a marca Baraclude®, é um medicamento antiviral usado no tratamento da infecção pelo vírus da hepatite B (VHB).[3] Pessoas com HIV/AIDS e HBV, também devem utilizar medicação antirretroviral.[3] O entecavir é administrado via oral, em comprimidos ou solução.[3]
Dentre os efeitos colaterais comuns incluem dor de cabeça, náusea, aumento do açúcar no sangue e diminuição da função renal.[3] Dentre os efeitos colaterais graves incluem aumento do fígado, níveis elevados de lactato no sangue e inflamação do fígado, caso a medicação seja interrompida.[3] Este medicamento carece de estudos sobre o risco do uso durante a gravidez, embora não pareça ter apresentado riscos.[4] O entecavir pertence à família de medicamentos inibidores da transcriptase reversa nucleosídica (ITRN).[3][5] Ele impede a multiplicação do vírus da hepatite B bloqueando a transcriptase reversa.[3]
O entecavir foi aprovado para uso médico em 2005.[3] Consta na Lista de Medicamentos Essenciais da Organização Mundial da Saúde.[6] Nos Estados Unidos, desde 2015, não está disponível como medicamento genérico,[7] e o preço por atacado é cerca de US$ 392 dólares, custo mensal em 2016.[8]
Referências
- ↑ «Baraclude- entecavir tablet, film coated Baraclude- entecavir solution». DailyMed. Consultado em 24 de janeiro de 2021. Cópia arquivada em 8 de novembro de 2016
- ↑ Fung J, Cheung C, Chan SC, Yuen MF, Chok KS, Sharr W, Dai WC, Chan AC, Cheung TT, Tsang S, Lam B, Lai CL, Lo CM (outubro de 2011). «Entecavir monotherapy is effective in suppressing hepatitis B virus after liver transplantation». Gastroenterology. 141 (4): 1212–1219. PMID 21762659. doi:10.1053/j.gastro.2011.06.083

- ↑ a b c d e f g h «Entecavir». The American Society of Health-System Pharmacists. Consultado em 28 de novembro de 2016. Arquivado do original em 20 de dezembro de 2016
- ↑ «Entecavir (Baraclude) Use During Pregnancy». www.drugs.com. Consultado em 6 de dezembro de 2016. Arquivado do original em 7 de novembro de 2016
- ↑ Shetty, Kirti; Wu, George Y. (2009). Chronic Viral Hepatitis: Diagnosis and Therapeutics (em inglês). [S.l.]: Springer Science & Business Media. ISBN 9781597455657. Consultado em 25 de maio de 2018. Cópia arquivada em 28 de agosto de 2018
- ↑ World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. 2019. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO
- ↑ Hamilton, Richart (2015). Tarascon Pocket Pharmacopoeia 2015 Deluxe Lab-Coat Edition. [S.l.]: Jones & Bartlett Learning. ISBN 9781284057560
- ↑ «NADAC as of 2016-11-30 | Data.Medicaid.gov». Centers for Medicare and Medicaid Services. Consultado em 6 de dezembro de 2016. Arquivado do original em 30 de novembro de 2016