Distribuição disjunta
Em biogeografia, um taxon apresenta uma distribuição disjunta se tiver dois ou mais grupos relacionados e que sejam amplamente separados entre si, do ponto de vista geográfico.
Mais especificamente, a distribuição disjunta refere-se ao padrão em que espécies, populações ou linhagens evolutivamente relacionadas ocorrem em duas ou mais áreas geográficas separadas, sem continuidade atual da vegetação entre esses núcleos. Esse tipo de padrão decorre de eventos históricos que interromperam a conexão entre populações ancestrais, podendo refletir processos como vicariância, dispersão de longa distância ou extinções locais ao longo do tempo [1].
Importância da distribuição disjunta em plantas Neotropicais
A distribuição disjunta em plantas é importante porque revela processos históricos e ambientais que moldaram a flora da América do Sul, permitindo identificar eventos de vicariância, mudanças climáticas profundas e transgressões marinhas que separaram linhagens anteriormente contínuas.
Esses padrões também evidenciam conservadorismo de nicho, uma vez que muitas linhagens, por exemplo, permaneceram restritas a áreas que conservaram condições ambientais semelhantes às originais após períodos de aridificação. Além disso, distribuições disjuntas ajudam a interpretar a estrutura filogenética das espécies e suas relações evolutivas, integrando informações ecológicas e espaciais para compreender a evolução da flora Neotropical. Esses padrões também refletem de eventos maiores, como a expansão da diagonal de formações abertas (expansão das regiões sazonalmente secas - Caatinga-Cerrado-Chaco) a partir do soerguimento dos Andes no Oligoceno-Mioceno, criando uma barreira climática no interior da América do Sul e antigas conexões florísticas intercontinentais, revelando rotas de dispersão e isolamento que marcaram a história biogeográfica do continente [2].
Mecanismos que podem levar à ocorrência de distribuição disjunta
A vicariância é um processo evolutivo pelo qual populações ancestrais contínuas são separadas pela formação de barreiras físicas ou ecológicas, levando ao isolamento e posterior divergência genética.
Algumas principais causas de eventos de vicariância são:
- Oscilações climáticas do Pleistoceno: isolamento e reconexão altitudinal;
- Barreiras topográficas: vales profundos e relevo acidentado;
- Isolamento em “ilhas céu” (sky islands);
- Alterações paleogeográficas.
São eventos raros de dispersão biológica onde pode ocorrer a colonização de novas regiões, muito distantes da localização parental, superando barreiras geográficas e ecológicas. Ocorre principalmente de forma passiva nas plantas, onde sementes e outras unidades de dispersão são transportadas por vetores como corpos d'água, como rios e mares; vento e por animais.
Padrões de distribuição disjunta
Existem numerosos padrões de distribuição disjunta a escalas muito diferentes:
Relictos glaciares
Muitos gêneros têm espécies vicariantes como consequência da regressão glaciar. Tal ocorre com o gênero Abies, presente em numerosos maciços montanhosos onde vingaram após a retirada dos glaciares. As populações migraram para outras latitudes de forma paralela ao recuo dos gelos, mas algumas subiram as cordilheiras e produziu-se uma especiação alopátrica. Outro exemplo é o do género Cedrus presente não apenas nas montanhas do Magrebe (Cedrus atlantica), mas também nas do Líbano (Cedrus libani), Chipre (Cedrus brevifolia) e Himalaia (Cedrus deodara).
Disjunção Irano-Turaniana
A espécie Stipa tenacissima tem distribuição disjunta entre a região entre o mar Negro e o mar Cáspio e o Mediterrâneo Ocidental. Provavelmente estas espécies chegaram com a crise salina do Messiniense durante a qual o Mediterrâneo praticamente ficou seco.
Disjunção Europa-África meridional
O género Erica está distribuído entre a África meridional (mais de 600 espécies) e a Europa (cerca de 70 espécies), com um grande vazio em quase todo o continente africano.
Espécies relictas no Sahara
Alguns géneros como o Olea apresentam distribuição disjunta entre o Mediterrâneo (Olea europaea) e as montanhas centrais do Saara (Olea laperrini). O crocodilo-do-nilo (Crocodilus niloticus) subsiste também em algumas gueltas saarianas e nos maciços montanhosos como o Hoggar. Várias espécies de vertebrados têm esta mesma distribuição disjunta entre o norte e o sul do Saara em consequência da sua desertificação: Psammophis schokari, Bitis arietans, Gazella dorcas. Algumas distribuições disjuntas, como o elefante, o leopardo ou o leão-do-atlas, desapareceram em tempos históricos.
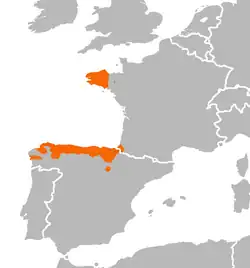
Distribuição lusitânica
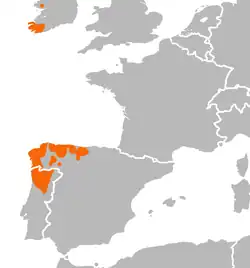
Várias espécies têm uma distribuição denominada lusitânica aparecendo na Península Ibérica e na Irlanda, sem passar pela Grã-Bretanha. Entre as espécies que têm esta distribuição estão alguns gastrópodes como Geomalacus maculosus ou Semilimax pyrenaicus e várias plantas, como algumas ericáceas tais como Daboecia cantabrica ou Arbutus unedo.
As teorias sobre a origem desta distribuição admitem a existência de uma ponte terrestre livre de gelo que teria permitido a existência de um refúgio quaternário. Esta hipótese está descartada na atualidade. Com o uso de marcadores genéticos pôde-se desenvolver uma nova teoria. Mascheretti et al. (2003)[5] examinaram os genótipos de Sorex minutus e comprovaram que as populações irlandesas estavam mais próximas da ibéricas que de outras populações europeias e a estrutura genética da população sugeria um único efeito fundador. Os autores concluem que existiria um contacto Paleolítico ou Mesolítico desde o sudoeste da Europa. Algo semelhante ocorre com a espécie Microtus arvalis nas Órcades[6][7] e con otros micromamíferos que surgem nas ilhas britânicas como Microtus epiroticus ou Clethrionomys glareolus[8][9][10]
Estes resultados coincidem com os trabalhos em genética humana[11][12] que afirmam haver uma forte semelhança entre as populações humanas ibéricas e do sul da Irlanda.
Disjunção Gondwânica [13]
A disjunção gondwânica refere-se ao padrão biogeográfico resultante da fragmentação do supercontinente Gondwana, que unia as massas continentais da América do Sul, África, Antártica, Austrália, Madagascar e Índia. A separação progressiva desses blocos, iniciada no Cretáceo Inferior (aprox. 130–125 milhões de anos atrás), provocou o isolamento gradual das biotas anteriormente contínuas, dando origem a linhagens disjuntas com afinidades evolutivas comuns.
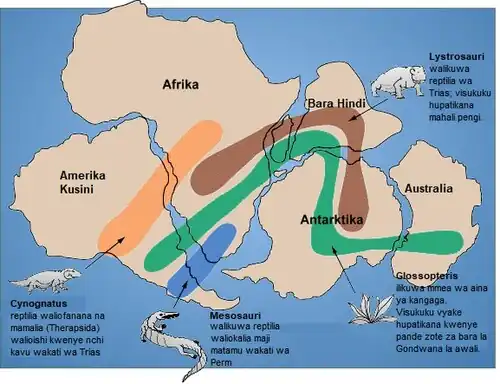
Durante o Cretáceo Médio, a América do Sul permanecia ligada à África e, por meio da Antártica, a Madagascar, Índia e Austrália. Esse arranjo permitiu amplas trocas faunísticas e florísticas entre as regiões austrais. A subsequente abertura do Atlântico Sul, completada há cerca de 90 milhões de anos, interrompeu esses fluxos e consolidou a separação entre as biotas afro-sul-americanas. Vestígios dessa conexão são observados na ocorrência de táxons hoje restritos ao Hemisfério Sul, como Nothofagus e várias famílias de angiospermas (Proteaceae, Myrtaceae, Arecaceae), que apresentam distribuições descontínuas entre América do Sul, Austrália e Nova Zelândia.
Assim, a disjunção gondwânica constitui evidência de vicariância associada à deriva continental, explicando afinidades biogeográficas entre organismos dos atuais continentes do sul. O conceito representa um marco na biogeografia histórica, ao integrar dados paleontológicos, tectônicos e filogenéticos na interpretação da distribuição global das espécies.
Distribuição disjunta sob uma perspectiva Neotropical
Amazônia - Mata Atlântica[14]
O padrão de disjunção Amazônia–Mata Atlântica é um dos mais expressivos exemplos de distribuição disjunta na flora brasileira. Diversas espécies e gêneros de angiospermas ocorrem simultaneamente nos dois biomas, hoje separados por formações abertas e secas — o “arco das formações abertas”, composto principalmente por Cerrado e Caatinga.
Evidências paleoclimáticas e florísticas indicam que, em períodos mais úmidos do Cenozoico e do Pleistoceno, houve conexões florestais contínuas entre esses domínios, possibilitando o intercâmbio florístico.
A presença atual de táxons idênticos ou aparentados, como Philodendron ornatum (Araceae), Eschweilera ovata (Lecythidaceae), Pouteria venosa (Sapotaceae) e gêneros como Macrolobium, Parkia, Lacmellea, Adelobotrys e Pagamea, reflete essas antigas ligações florísticas.
Três rotas principais são propostas para explicar o intercâmbio entre os biomas:
- Meridional, pela bacia do rio Paraná;
- Central, por florestas de galeria no Cerrado;
- Nordestina, atravessando a Caatinga — considerada a mais fortemente apoiada por dados florísticos e biogeográficos.
A disjunção Amazônia–Mata Atlântica representa, assim, um registro das mudanças paleoclimáticas e paleovegetacionais que moldaram a história da flora neotropical, envolvendo tanto eventos de vicariância (antigas conexões interrompidas) quanto de dispersão secundária (colonizações mais recentes).
Brejos de Altitude no Domínio da Caatinga
O Domínio Fitogeográfico da Caatinga constitui a maior província semiárida da América do Sul, ocupando grande parte do Nordeste brasileiro. Caracteriza-se por clima fortemente sazonal, precipitação anual geralmente inferior a 1.000 mm, elevada evapotranspiração e marcada estacionalidade hídrica. Essas condições determinam uma biota adaptada ao déficit de água e estruturam um mosaico de paisagens formado por caatingas cristalinas e sedimentares, inselbergs, florestas ribeirinhas e extensos ecótonos com o Cerrado e a Mata Atlântica .
Inseridos nesse contexto árido, os brejos de altitude destacam-se como enclaves úmidos associados a relevos mais elevados que interceptam massas de ar úmidas vindas do Atlântico. O efeito orográfico gera microclimas subúmidos com maior pluviosidade, solos mais profundos e temperaturas mais amenas, contrastando fortemente com a matriz semiárida ao redor[15] .
Esses brejos configuram padrões clássicos de distribuição disjunta, por abrigarem espécies típicas de formações ombrófilas atlânticas isoladas em meio ao domínio semiárido [16]. Tal configuração está relacionada à teoria dos refúgios, segundo a qual áreas de estabilidade ambiental durante o Quaternário atuaram como refúgios de biodiversidade, preservando linhagens vegetais sob condições climáticas flutuantes [17].
A presença de espécies de ocorrência em diferentes brejos de altitude, que não ocorrem na matriz circundante, como Vismia guianensis (Aubl.) Choisy, Copaifera langsdorffii Desv, Piptadenia stipulacea (Benth.) Ducke, Byrsonima sericea DC., Guarea macrophylla Vahl, Talisia esculenta(Cambess.) Radlk., Simarouba amara Aubl. são evidências de distribuição disjunta dessa vegetação [18].
Exemplos de distribuição disjunta
- Género Coriaria, que tem distribuição disjunta no Mediterrâneo e do Paquistão ao Japão, Nova Guiné, Nova Zelândia e sul da América do Sul.[19]
- Género Cyanopica, comprovado recentemente que inclui duas espécies,[20] com distribuição disjunta entre a Península Ibérica (Cyanopica cookii) e a Ásia Oriental (Cyanopica cyanus).
Referências
- ↑ Rull, Valentí; Carnaval, Ana Carolina, eds. (2020). «Neotropical Diversification: Patterns and Processes». Fascinating Life Sciences (em inglês). ISSN 2509-6745. doi:10.1007/978-3-030-31167-4. Consultado em 7 de novembro de 2025
- ↑ «Biogeografia e Diversidade da Flora Sul-Americana | PDF | Biodiversidade | América do Sul». Scribd. Consultado em 7 de novembro de 2025
- ↑ Henry Nicholas Ridley (1930). The Dispersal Of Plants Throughout The World. [S.l.: s.n.] Consultado em 7 de novembro de 2025
- ↑ Nathan, Ran (11 de agosto de 2006). «Long-Distance Dispersal of Plants». Science (em inglês) (5788): 786–788. ISSN 0036-8075. doi:10.1126/science.1124975. Consultado em 7 de novembro de 2025
- ↑ Masheretti S., Rogatcheva M. B., Gündüz I., Fredga K. & Searle J. B. 2003. How did pygmy shrews colonize Ireland? Clues from a phylogenetic analysis of mitochondrial cytochrome b sequences Arquivado em 2012-06-29 na Archive.today. Proc. Roy. Soc. B 270: 1593-1599.
- ↑ Haynes, S., M. Jaarola & J.B. Searle. 2003. Phylogeography of the common vole (Microtus arvalis) with particular emphasis on the colonization of the Orkney archipelago. Molecular Ecology 12 (4): 951-956.
- ↑ Haynes, S., M. Jaarola, J. Searle & K. Dobney. 2004. The origin of the Orkney vole: a proxy for reconstructing human movements, in: R. Housley and G. Coles (eds.). Atlantic connections and adaptations: Economies, environments and subsistence in the north Atlantic realm. Oxford: Oxbow books.
- ↑ Corbet, G. B. 1961. Origin of the British insular races of small mammals and of the 'Lusitanian' fauna. Nature 191, 1037-1040.
- ↑ Fredga, K., Jaarola, M., Ims, R. A., Steen, H. & Yoccoz, N. G. 1990. The 'common vole' in Svalbard identified as Microtus epiroticus by chromosome analysis. Polar Research 8, 283-290.
- ↑ Smal, C. M. & Fairley, J. S. 1984. The spread of the Bank vole Clethrionomys glareolus in Ireland . Mammal Review 14, 71-78.
- ↑ Hill E. W., Jobling M. A. & Bradley D. G. 2000. Y chromosome variation and Irish origins. Nature 404: 351.
- ↑ McEvoy B., Richards M., Forster P. & Bradley D. G. 2004. The longue durée of genetic ancestry: multiple genetic marker systems and Celtic origins on the Atlantic facade of Europe. Am. J. Hum. Genet. 75: 693-702.
- ↑ Raven, Peter H.; Axelrod, Daniel I. (1975). «History of the Flora and Fauna of Latin America: The theory of plate tectonics provides a basis for reinterpreting the origins and distribution of the biota». American Scientist (4): 420–429. ISSN 0003-0996. Consultado em 7 de novembro de 2025
- ↑ Fiaschi, Pedro; Pirani, José R. (setembro de 2009). «Review of plant biogeographic studies in Brazil». Journal of Systematics and Evolution (em inglês) (5): 477–496. ISSN 1674-4918. doi:10.1111/j.1759-6831.2009.00046.x. Consultado em 7 de novembro de 2025
- ↑ Gois, Laís Susana de Souza; Corrêa, Antônio Carlos de Barros; Monteiro, Kleython de Araújo (17 de dezembro de 2019). «Análise Integrada dos Brejos de Altitude do Nordeste do Brasil a partir de Atributos Fisiográficos / Integrated Analysis of Highland Humid Brejos in Northeast Brazil Based on Physiographic Attributes». Espaço Aberto (2): 77–98. ISSN 2237-3071. doi:10.36403/espacoaberto.2019.28357. Consultado em 7 de novembro de 2025
- ↑ «Establishing a secure connection ...». www.scielo.br. doi:10.1590/s0103-40141999000200003. Consultado em 7 de novembro de 2025
- ↑ Werneck, Fernanda P. (1 de junho de 2011). «The diversification of eastern South American open vegetation biomes: Historical biogeography and perspectives». Quaternary Science Reviews (13): 1630–1648. ISSN 0277-3791. doi:10.1016/j.quascirev.2011.03.009. Consultado em 7 de novembro de 2025
- ↑ Araujo, Thallyta Guimarães; Queiroz, Augusto Barbosa de; Lopes, Sérgio de Faria (30 de junho de 2019). «Fitossociologia de um brejo de altitude no semiárido brasileiro: variação das espécies dominantes ao longo do gradiente altitudinal». Ciência Florestal (2): 779–794. ISSN 1980-5098. doi:10.5902/1980509821231. Consultado em 7 de novembro de 2025
- ↑ Royal Botanic Gardens: World Checklist of Selected Plant Families. «Coriaria L., Sp. Pl.: 1037 (1753).». Consultado em 12 de janeiro de 2010
- ↑ Kyukov et al., Synchronic east–west divergence in azure-winged magpies (Cyanopica cyanus) and magpies (Pica pica)[ligação inativa], Journal of Zoological Systematics and Evolutionary Research 42(4): 342-351 (2004)