Difluoreto de criptônio
Difluoreto de criptônio
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
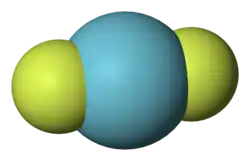 | |||||||||||||
| Nomes | |||||||||||||
| Nome IUPAC | Fluoreto de criptônio II | ||||||||||||
| Outros nomes | Difluoreto de criptônio | ||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| Página de dados suplementares | |||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||
O difluoreto de criptônio é um composto de criptônio de fórmula química KrF2,[2] formado pela reação do gás Kr com F2 em condições especiais, tais como descargas elétricas de uma mistura dos dois gases em baixa temperatura (-150º C) , irradiação ultravioleta de uma mistura de flúor com Kr sólido, etc.. É a única molécula neutra e estável contendo criptônio; as demais são instáveis, carregadas ou transientes. É um sólido branco, poderoso agente oxidante e de fluoração, que reage vigorosamente com várias substâncias liberando criptônio gasoso e compostos de flúor. Embora seja uma molécula estável, o KrF2 se decompõe espontaneamente nos elementos constituintes à temperatura normal. Ele é capaz de oxidar diretamente o xenônio gasoso a XeF6:
3KrF2 + Xe --> XeF6 + 3Kr
KrF2 oxida o pentafluoreto de bromo a´compostos com o íon extremamente reativo [BrF6]+ (que contem Br com nox +7), além de reagir com o ouro oxidando-o até o estado de oxidação +5, extremamente raro para o elemento:
7 KrF2 (g) + 2 Au (s) --> 2 KrF+AuF6- + 5 Kr (g)
O composto formado se decompõe a 60°C gerando pentafluoreto de ouro (AuF5) e liberando Kr gasoso:
KrF+AuF6- --> AuF5 + Kr + F2