Dideoxinucleotídeo
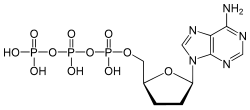
Didesoxinucleotídeos são inibidores da elongação de cadeia da DNA polimerase, utilizados no método de Sanger para sequenciamento de DNA.[1] Também são conhecidos como 2',3' porque tanto as posições 2' quanto 3' da ribose não possuem grupo hidroxila, e são abreviados como ddNTPs (ddGTP, ddATP, ddTTP e ddCTP).[2]
Papel no método de Sanger
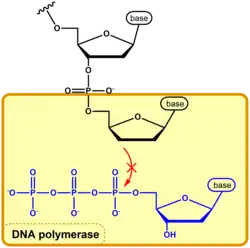
O método de Sanger é utilizado para amplificar um segmento-alvo de DNA, de forma que a sequência do DNA possa ser determinada com precisão. A incorporação de ddNTPs na reação serve para interromper a síntese de uma cadeia de DNA em crescimento, resultando em fragmentos de DNA parcialmente replicados. Isso ocorre porque a DNA polimerase requer o grupo OH 3' da cadeia em crescimento e o grupo fosfato 5' do dNTP que entra para formar uma ligação fosfodiéster.[2]
Às vezes, a DNA polimerase incorpora um ddNTP, e a ausência do grupo OH 3' interrompe a reação de condensação entre o fosfato 5' (após a clivagem do pirofosfato) do nucleotídeo que entra com o grupo hidroxila 3' do nucleotídeo anterior da cadeia em crescimento. Essa reação de condensação normalmente ocorreria com a incorporação de um dNTP não modificado pela DNA polimerase. Em termos simples, o ataque nucleofílico do grupo OH 3' leva à adição de um nucleotídeo a uma cadeia em crescimento. A ausência do grupo hidroxila 3' impede esse ataque nucleofílico de ocorrer, impossibilitando que a DNA polimerase continue sua função.[2]
Essa descoberta levou ao nome apropriado de "nucleotídeos terminadores de cadeia".[2] Os didesoxirribonucleotídeos não possuem o grupo hidroxila 3', portanto nenhuma elongação adicional da cadeia pode ocorrer uma vez que esse didesoxinucleotídeo esteja incorporado. Isso pode levar à interrupção da sequência de DNA. Assim, essas moléculas constituem a base do método de terminação em cadeia por didesoxi de sequenciamento de DNA, que foi descrito por Frederick Sanger e sua equipe em 1977[3] como uma extensão de trabalhos anteriores.[4]
A abordagem de Sanger foi descrita em 2001 como um dos dois métodos fundamentais para o sequenciamento de fragmentos de DNA[1] (o outro sendo o método de Maxam–Gilbert[5]), mas o método de Sanger é tanto "o mais amplamente utilizado quanto o método utilizado pela maioria dos sequenciadores de DNA automatizados."[1] Sanger recebeu seu segundo Prêmio Nobel de Química em 1980, compartilhando-o com Walter Gilbert ("por suas contribuições relativas à determinação das sequências de bases nos ácidos nucleicos") e com Paul Berg ("por seus estudos fundamentais da bioquímica dos ácidos nucleicos, especialmente no que diz respeito ao DNA recombinante"),[6] e discutiu o uso de didesoxinucleotídeos em sua palestra do Nobel.[7]
Sequenciamento de DNA
Didesoxinucleotídeos são úteis no sequenciamento de DNA em combinação com eletroforese. Uma amostra de DNA que passa por PCR (reação em cadeia da polimerase) em uma mistura contendo os quatro desoxinucleotídeos e um didesoxinucleotídeo produzirá cadeias com comprimento igual à posição de cada base do tipo complementar ao tipo que contém o didesoxinucleotídeo. A Taq polimerase usada na PCR favorece o ddGTP, um padrão observado em diversas pesquisas.[8] Ou seja, cada base de nucleotídeo daquele tipo tem uma chance de se ligar a um didesoxinucleotídeo em vez de um desoxinucleotídeo, o que termina a elongação da cadeia. Portanto, se a amostra passar por eletroforese, haverá uma faixa presente para cada comprimento em que o complementar do didesoxinucleotídeo está presente. Hoje é comum o uso de didesoxinucleotídeos fluorescentes, de modo que cada um dos quatro apresenta uma fluorescência diferente que pode ser detectada por um sequenciador; assim, apenas uma reação é necessária.
Produção
Em um método patenteado, utilizou-se tetraidrofurano em um solvente contendo 50 g (0,205 mols) de uridina (ou, presumivelmente, qualquer nucleosídeo não protegido), 112 ml (1,03 mols) de ortoformato de metila e 10 g (52,6 mmols) de ácido p-toluenossulfônico à temperatura ambiente com agitação. Após 24 horas, a mistura foi despejada em uma solução aquosa de bicarbonato de sódio, seguida de extração com clorofórmio 5 vezes. O extrato foi seco com sulfato de sódio e concentrado, obtendo-se 49,5 g (0,173 mols) de 2',3'-O-metoximetilidenouridina (rendimento de 84,5%). Em seguida, o produto de uridina é dissolvido em 50 ml de anidrido acético à temperatura ambiente com agitação. A solução foi aquecida a 140 °C e mantida nessa temperatura por 5 horas sob refluxo. Após resfriamento, o solvente foi removido por destilação sob pressão reduzida, adicionaram-se 50 ml de água, e a mistura foi extraída 3 vezes com 100 ml de clorofórmio. O extrato foi concentrado sob pressão reduzida, obtendo-se um rendimento de 82,3% de 2',3'-didesoxi-2',3'-dideidouridina. Este produto foi então hidratado para remoção da dupla ligação, dissolvendo-o em 10 ml de metanol contendo um catalisador (5% de paládio em carbono úmido) (400 mg) sob atmosfera de hidrogênio por 1 h, obtendo-se o didesoxinucleosídeo resultante (neste caso, 2',3'-didesoxiuridina).[6] O nucleotídeo com corante a ser usado provavelmente será obtido por tratamento com enzima de fosforilação e biotinilação, seguido de reação com o corante. É possível que a reação imediata com o corante também ocorra, mas a extensão do braço é apontada como mais eficiente no caso de uso de forma mutante da DNA polimerase.[5]
Referências
Referências
- ↑ a b c Meis, RJ; Raghavachari R (2001). Aplicações de Infravermelho Próximo na Biotecnologia. [S.l.]: CRC Press. pp. 133–150. ISBN 9781420030242
- ↑ a b c d Watson, JD; Baker TA; Bell SP; Gann A; Levine M; Losick R (2014). Biologia molecular do gene 7ª ed. Cold Spring Harbor, NY: Pearson. pp. 160–161. ISBN 978-0-321-76243-6
- ↑ Sanger, F (dezembro de 1977). «DNA sequencing with chain-terminating inhibitors». Proceedings of the National Academy of Sciences of the United States of America. 74 (12): 5463–7. Bibcode:1977PNAS...74.5463S. PMC 431765
 . PMID 271968. doi:10.1073/pnas.74.12.5463
. PMID 271968. doi:10.1073/pnas.74.12.5463
- ↑ Sanger, F (maio de 1975). «A rapid method for determining sequences in DNA by primed synthesis with DNA polymerase». Journal of Molecular Biology. 94 (3): 441–8. PMID 1100841. doi:10.1016/0022-2836(75)90213-2
- ↑ a b Maxam, AM (fevereiro de 1977). «A new method for sequencing DNA». Proceedings of the National Academy of Sciences of the United States of America. 74 (2): 560–4. Bibcode:1977PNAS...74..560M. PMC 392330
 . PMID 265521. doi:10.1073/pnas.74.2.560
. PMID 265521. doi:10.1073/pnas.74.2.560
- ↑ a b Kungliga Vetenskapsakademien (Academia Real das Ciências da Suécia) (14 de outubro de 1980). «O Prêmio Nobel de Química de 1980». nobelprize.org (Nota de imprensa). Nobel Media. Consultado em 14 de dezembro de 2019 [ligação inativa]
- ↑ Sanger, F (8 de dezembro de 1980). «Determination of Nucleotide Sequences in DNA (Palestra do Nobel)» (PDF). nobelprize.org. Nobel Media. Consultado em 14 de dezembro de 2019 [ligação inativa]
- ↑ Li, Y; Mitaxov V; Waksman G (agosto de 1999). «Structure-based design of Taq DNA polymerases with improved properties of dideoxynucleotide incorporation». Proceedings of the National Academy of Sciences of the United States of America. 96 (17): 9491–6. Bibcode:1999PNAS...96.9491L. PMC 22236
 . PMID 10449720. doi:10.1073/pnas.96.17.9491
. PMID 10449720. doi:10.1073/pnas.96.17.9491
Ligações externas
