Dibenzoilmetano
Dibenzoilmetano
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
| Nomes | |||||||||||||
| Outros nomes | 2-Benzoilacetofenona | ||||||||||||
| |||||||||||||
| |||||||||||||
| Página de dados suplementares | |||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||
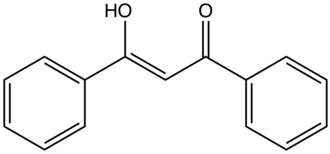
Dibenzoilmetano (DBM) é um composto orgânico de fórmula química (C6H5C(O))2CH2. O DBM é uma 1,3-dicetona, mas o composto existe principalmente em estrutura dienólica (tautomerismo enol-enol).[1]
Devido às propriedades de absorção de radiação UV, derivados de DBM, a exemplo da avobenzona, também são utilizados em produtos de proteção solar.[2]
Síntese
A síntese do DBM ocorre pela condensação de benzoato de etila com acetofenona.[3]
Ocorrência e propriedades medicinais
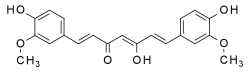
O dibenzoilmetano (DBM) é um componente secundário presente no extrato da raiz de alcaçuz (Glycyrrhiza glabra, da família Leguminosae) e também é encontrado na curcumina.[4] Sua ocorrência nessas fontes naturais levou a pesquisas sobre as propriedades medicinais dessa classe de compostos.[5][6]
Estudos indicam que o DBM (e a trazodona) retardam a progressão de doenças neurodegenerativas, prevenindo a interrupção da síntese proteica nos neurônios.[7]
Ver também
Referências
- ↑ Thomas, L. H.; Florence, A. J.; Wilson, C. C. (2009). «Hydrogen atom behaviour imaged in a short intramolecular hydrogen bond using the combined approach of X-ray and neutron diffraction». New Journal of Chemistry. 33 (12): 2486–2490. doi:10.1039/B908915B
- ↑ Freire, Thamires Batello (17 de janeiro de 2022). «Influência de antioxidantes na fotoestabilização da avobenzona (filtro UVA) e do p-metoxicinamato de octila (filtro UVB) em fotoprotetores». São Paulo. doi:10.11606/t.9.2022.tde-19052022-110821. Consultado em 16 de março de 2025
- ↑ Magnani, Arthur; McElvain, S. M. (1940). «Dibenzoylmethane». Org. Synth. 20. 32 páginas. doi:10.15227/orgsyn.020.0032
- ↑ Jackson, Kimberly M.; Deleon, Marisela; Verret, C.Reynold; Harris, Wayne B. (2002). «Dibenzoylmethane Induces Cell Cycle Deregulation in Human Prostate Cancer Cells». Cancer Letters. 178 (2): 161–165. PMID 11867200. doi:10.1016/S0304-3835(01)00844-8
- ↑ Shishu; Singla, A.K.; Kaur, I.P. (2003). «Inhibitory Effect of Dibenzoylmethane on Mutagenicity of Food-Derived Heterocyclic Amine Mutagens». Phytomedicine. 10 (6–7): 575–582. PMID 13678246. doi:10.1078/094471103322331575
- ↑ Pan, Min-Hsiung; Huang, Mei-Chen; Wang, Ying-Jan; Lin, Jen-Kun; Lin, Chao-Hsien (2003). «Induction of Apoptosis by Hydroxydibenzoylmethane through Coordinative Modulation of Cyclin D3, BCL-XL, and Bax, Release of Cytochrome c, and Sequential Activation of Caspases in Human Colorectal Carcinoma Cells». Journal of Agricultural and Food Chemistry. 51 (14): 3977–3984. PMID 12822933. doi:10.1021/jf034094i
- ↑ Halliday, Mark; Radford, Helois; Zents, Karlijn A. M.; Molloy, Collin; Moreno, Julie A.; Verity, Nicholas C.; Smith, Ewan; Ortori, Catharine A.; Barrett, David A. (2017). «Repurposed Drugs Targeting eIF2α-P-Mediated Translational Repression Prevent Neurodegeneration in Mice». Brain. 140 (6): 1768–1783. PMC 5445255
 . PMID 28430857. doi:10.1093/brain/awx074
. PMID 28430857. doi:10.1093/brain/awx074