Cobra marinha
Cobra marinha
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ocorrência: Oligoceno – Recente[1] | |||||||||||||
| Classificação científica | |||||||||||||
| |||||||||||||
| Distribuição geográfica | |||||||||||||
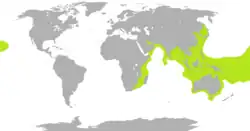 Distribuição das cobras marinhas mostrado em verde-limão, exceto a cobra-do-mar-pelágio, pelágica e amplamente distribuída.
| |||||||||||||
As cobras marinhas, serpentes marinhas ou cobras de recifes de coral, são serpentes da família Elapidae que habitam ambientes marinhos durante a maior parte ou toda a sua vida. Elas pertencem a duas subfamílias, Hydrophiinae e Laticaudinae [en]. Hydrophiinae também inclui serpentes terrestres australianas, enquanto Laticaudinae inclui apenas as serpentes-marítimas (Laticauda), das quais três espécies são encontradas exclusivamente em água doce. Se essas três espécies de água doce forem excluídas, há 69 espécies de cobras marinhas divididas entre sete gêneros.[2]
A maioria das cobras marinhas é venenosa, exceto o gênero Emydocephalus [en], que se alimenta quase exclusivamente de ovos de peixe.[3] As cobras marinhas são amplamente adaptadas a uma vida totalmente aquática e são incapazes de se mover em terra, exceto as serpentes-marítimas, que têm movimento limitado em terra. Elas são encontradas em águas costeiras quentes do Oceano Índico ao Pacífico e são estreitamente relacionadas às serpentes terrestres venenosas da Austrália.[4]
Todas as cobras marinhas têm caudas em forma de remo e muitas possuem corpos lateralmente comprimidos, o que lhes confere uma aparência semelhante a uma enguia. Diferentemente dos peixes, elas não possuem brânquias e devem emergir regularmente para respirar. Junto com os cetáceos, estão entre os vertebrados mais completamente aquáticos existentes que respiram ar.[5] Entre esse grupo estão espécies com alguns dos venenos mais potentes entre todas as cobras. Algumas têm disposições gentis e mordem apenas quando provocadas, enquanto outras são muito mais agressivas.
Descrição
A maioria das espécies de cobras marinhas adultas cresce entre 120 e 150 cm de comprimento,[6] com a maior, Hydrophis spiralis [en], alcançando um máximo de 3 m.[7] Seus olhos são relativamente pequenos com uma pupila redonda[8] e a maioria tem narinas localizadas dorsalmente.[9] Os crânios não diferem significativamente dos de elapídeos terrestres, embora sua dentição seja relativamente primitiva com presas curtas e (com exceção de Emydocephalus) até 18 dentes menores atrás delas no maxilar.[5]
.jpg)
A maioria das cobras marinhas é completamente aquática e adaptou-se aos ambientes marinhos de várias maneiras, sendo a mais característica a cauda em forma de remo que melhorou sua capacidade de natação.[10] Em graus variados, os corpos de muitas espécies são lateralmente comprimidos, especialmente nas espécies pelágicas. Isso frequentemente causou a redução do tamanho das escamas ventrais, sendo até difícil distingui-las das escamas adjacentes. A falta de escamas ventrais significa que elas se tornaram praticamente indefesas em terra, mas, como vivem todo o seu ciclo de vida no mar, não precisam sair da água.[6][9]
O único gênero que reteve as escamas ventrais alargadas é o das cobras-marítimas, Laticauda [en], com apenas cinco espécies. Essas cobras são consideradas mais primitivas, pois ainda passam muito tempo em terra, onde suas escamas ventrais lhes proporcionam a aderência necessária.[6][9] As espécies de Laticauda também são as únicas cobras marinhas com escamas internasais; ou seja, suas narinas não estão localizadas dorsalmente.[10]
Como a língua de uma cobra pode cumprir sua função olfativa mais facilmente sob a água, sua ação é curta em comparação com a de espécies de cobras terrestres. Apenas as pontas bifurcadas protrudem da boca através de uma fenda dividida no meio da escama rostral.[5] As narinas possuem válvulas constituídas por um tecido esponjoso especializado para excluir a água, e a traqueia pode ser elevada até onde a passagem nasal curta se abre no teto da boca. Essa é uma adaptação importante para um animal que deve emergir para respirar, mas pode ter a cabeça parcialmente submersa ao fazê-lo. O pulmão tornou-se muito grande e se estende por quase todo o comprimento do corpo, embora a porção traseira seja considerada como tendo se desenvolvido para auxiliar na flutuação, em vez de trocar gases. O pulmão estendido possivelmente também serve para armazenar ar para mergulhos.[6][9]
A maioria das espécies de cobras marinhas pode realizar respiração cutânea através do topo de sua pele. Isso é incomum para répteis, pois sua pele é espessa e escamosa, mas experimentos com a cobra-do-mar-pelágio, Hydrophis platurus (uma espécie pelágica), mostraram que essa espécie pode satisfazer cerca de 30% de suas necessidades de oxigênio dessa maneira, permitindo mergulhos prolongados.[11]

Como outros animais terrestres que se adaptaram à vida em um ambiente marinho, as cobras marinhas ingerem consideravelmente mais sal do que seus parentes terrestres por meio de suas dietas, quando a água do mar é engolida inadvertidamente. Por causa disso, é necessário um meio mais eficaz de regular a concentração de sal em seu sangue. Nas cobras marinhas, as glândulas sublinguais posteriores, localizadas sob e ao redor da bainha da língua, permitem-lhes expelir sal com a ação da língua.[5][9]
A escamação entre as cobras marinhas é altamente variável. Ao contrário das espécies de cobras terrestres que possuem escamas imbricadas para proteção contra abrasão, as escamas da maioria das cobras marinhas pelágicas não se sobrepõem. Espécies que habitam recifes, como Aipysurus [en], possuem escamas imbricadas para proteção contra o coral afiado. As escamas em si podem ser lisas, carenadas, espinhosas ou granulares, estas últimas frequentemente parecendo verrugas. Pelamis tem escamas corporais em forma de "pino", enquanto as de sua cauda são placas hexagonais justapostas.[9]
Habilidades sensoriais
Visão, quimiorrecepção (com o movimento da língua) e audição são sentidos importantes para cobras terrestres, mas esses estímulos se tornam distorcidos na água.[12][13] A pouca visibilidade, diluição química e limitação de vibrações transmitidas pelo solo na água sugerem que as cobras marinhas e as cobras-marítimas podem ter habilidades sensoriais únicas para compensar a relativa falta de outros sinais sensoriais.[14]
Relativamente pouco se sabe sobre a visão das cobras marinhas. Um estudo de fotorreceptores na retina de serpentes-marinhas-de-barriga-áspera, Hydrophis curtus, e da H. peronii, encontrou três classes de opsinas, todas de células cone.[15] Apesar da ausência de células bastonete nos olhos das cobras marinhas, Simões et al. encontraram a rodopsina (rh1), a opsina das bastonetes, ainda expressa no genoma,[16] sugerindo que em cobras marinhas alguns cones podem ser bastonetes transmutados. Observações comportamentais indicam que a visão tem um papel limitado na captura de presas e na seleção de parceiros, mas vibrações sonoras e quimiorrecepção podem ser importantes.[17][18] Um estudo identificou pequenos órgãos sensoriais na cabeça de H. curtus[19] semelhantes aos mecanorreceptores em jacarés e cobras aquáticas Acrochodus que são usados para detectar o movimento de peixes que são presas.[20]
Westhoff et al. registraram respostas cerebrais auditivas a vibrações subaquáticas em H. curtus,[21] que são sensíveis o suficiente para detectar movimentos em presas, mas não tão sensíveis quanto os sistemas de linha lateral de peixes. Da mesma forma, a visão parece ter importância limitada para encontrar parceiros. Shine experimentou aplicando secreções cutâneas (feromônios) a objetos semelhantes a cobras para ver se machos de serpentes-marinhas-cabeça-de-tartaruga, Emydocephalus annulatus, são atraídos por feromônios femininos. Shine descobriu que, embora a visão possa ser útil a curtas distâncias (menos de 1 m), os feromônios são mais importantes uma vez que o macho entra em contato físico com um objeto.[22]
A serpente-marinha-oliva, Aipysurus laevis [en], foi encontrada com fotorreceptores na pele de sua cauda, permitindo-lhe detectar luz e, presumivelmente, garantir que esteja completamente escondida, incluindo sua cauda, dentro de buracos de coral durante o dia. Embora outras espécies não tenham sido testadas, A. laevis possivelmente não é única entre as cobras marinhas nesse aspecto.[23] Outros sentidos únicos, como recepção eletromagnética e detecção de pressão,[24] foram propostos para cobras marinhas, mas estudos científicos ainda não foram realizados para testar esses sentidos.[14]
Distribuição e habitat
As cobras marinhas estão majoritariamente confinadas às águas tropicais quentes do Oceano Índico e do oeste do Oceano Pacífico,[6] com algumas espécies encontradas bem ao largo da Oceania.[25] A distribuição geográfica de uma espécie, a cobra-do-mar-pelágio, P. platura, é mais ampla do que a de qualquer outra espécie de réptil, exceto por algumas espécies de tartarugas marinhas.[5] Ela se estende desde a costa leste da África, de Djibuti ao norte até Cidade do Cabo ao sul,[26] através do Oceano Índico, do Pacífico, ao sul até a costa norte da Nova Zelândia,[25][27] até a costa oeste das Américas, onde ocorre do norte do Peru ao sul (incluindo as Ilhas Galápagos) até o Golfo da Califórnia ao norte. Espécimes isolados foram encontrados tão ao norte quanto San Diego e Oxnard nos Estados Unidos.[28]
As cobras marinhas não ocorrem no Oceano Atlântico.[9] Pelamis possivelmente estaria presente lá se não fosse pelas correntes frias ao largo da Namíbia e oeste da África do Sul que a impedem de cruzar para o Atlântico Sul oriental, ou ao sul da latitude de 5°S ao longo da costa oeste da América do Sul. As cobras marinhas também não ocorrem no Mar Vermelho, acredita-se que devido à sua salinidade aumentada, então não há perigo de que cruzem pelo canal de Suez. A falta de salinidade também é considerada a razão pela qual Pelamis não cruzou para o Caribe pelo canal do Panamá.[5]
Apesar de suas adaptações marinhas, a maioria das serpentes marinhas prefere águas rasas próximas à terra, ao redor de ilhas, e especialmente águas um pouco abrigadas, bem como próximas a estuários.[6][10] Elas podem nadar rio acima e foram relatadas a até 160 km do mar.[10] Outras, como P. platurus, são pelágicas e são encontradas em linhas de deriva, acúmulos de detritos flutuantes reunidos por correntes de superfície.[29] Algumas cobras marinhas habitam pântanos de mangue e habitats de água salobra semelhantes, e duas formas de água doce isoladas em terra são encontradas: H. semperi [en] ocorre no lago Taal nas Filipinas, e L. crockeri [en] no lago Tegano de Rennell nas Ilhas Salomão.[9]
Comportamento
As cobras marinhas são geralmente relutantes em morder,[6][7] e são usualmente consideradas de temperamento suave, embora haja variação entre espécies e indivíduos.[25] Algumas espécies, como P. platurus, que se alimentam simplesmente engolindo suas presas, são mais propensas a morder quando provocadas porque parecem usar seu veneno mais para defesa. Outras, como as espécies de Laticauda, usam seu veneno para imobilizar presas. As cobras marinhas são frequentemente manuseadas sem preocupação por pescadores locais que as desenrolam e jogam de volta na água com as mãos nuas, geralmente sem serem mordidos, quando as cobras frequentemente ficam presas em redes de pesca.[6][9] Espécies relatadas como muito mais agressivas incluem Aipysurus laevis, Astrotia stokesii, H. schistosus, H. zweifeli e H. ornatus.[10]

Em terra, seus movimentos tornam-se muito erráticos. Elas rastejam desajeitadamente nessas situações e podem se tornar bastante agressivas, atacando selvagemente qualquer coisa que se mova, embora sejam incapazes de se enrolar e atacar da maneira de cobras terrestres.[7][8]
As cobras marinhas parecem ser ativas tanto de dia quanto de noite. Pela manhã, e às vezes no final da tarde, elas podem ser vistas na superfície tomando sol, e mergulham quando perturbadas.[6] Foram relatadas nadando a profundidades superiores a 90 m, e podem permanecer submersas por até algumas horas, possivelmente dependendo da temperatura e do grau de atividade.[7][25]
As cobras marinhas foram avistadas em grandes números. Por exemplo, em 1932, um navio a vapor no estreito de Malaca, ao largo da costa da Malásia, relatou ter avistado "milhões" de indivíduos de Astrotia stokesii, uma parente de Pelamis; estas formaram uma linha de cobras com 3 m de largura e 100 km de comprimento.[29] A causa desse fenômeno é desconhecida, embora provavelmente esteja relacionada à reprodução.[5] Elas podem às vezes ser vistas nadando em grupos de várias centenas, e muitos espécimes mortos foram encontrados em praias após tufões.[8]
Ecologia
Elas se alimentam de peixes pequenos e ocasionalmente de polvos jovens. Frequentemente estão associadas à craca Platylepas ophiophila, que se fixa à sua pele.[30]
Reprodução
Exceto por um único gênero, todas as cobras marinhas são ovovivíparas; os filhotes nascem na água, onde vivem toda a sua vida.[9] Em algumas espécies, os filhotes são bastante grandes, chegando a até metade do comprimento da mãe.[7] A única exceção é o gênero Laticauda, que é ovíparo; e suas cinco espécies depositam seus ovos em terra.[9]
Veneno
Como seus parentes na família Elapidae, a maioria das cobras marinhas é altamente venenosa. Elas raramente injetam seu veneno ao morder, então mordidas venenosas em humanos são raras.[10] Por exemplo, P. platura tem um veneno mais potente do que qualquer espécie de cobra terrestre na Costa Rica com base na DL50, mas apesar de sua abundância nas águas ao largo de sua costa oeste, poucas fatalidades humanas foram relatadas.[11] A morte de um pescador de arrasto em águas australianas em 2018 foi relatada como a primeira fatalidade por cobra marinha na região desde a morte de um mergulhador em 1935.[31]
Mordidas nas quais ocorre envenenamento são geralmente indolores e podem nem ser percebidas quando o contato é feito. Os dentes podem permanecer na ferida. Geralmente, ocorre pouco ou nenhum inchaço, e raramente os linfonodos próximos são afetados. Os sintomas mais importantes são rabdomiólise (degradação rápida do tecido muscular esquelético) e paralisia. Os sintomas iniciais incluem dor de cabeça, sensação de língua espessa, sede, sudorese e vômito. O veneno age muito lentamente e os sintomas que ocorrem de 30 minutos a várias horas após a mordida incluem dores generalizadas, rigidez e sensibilidade muscular em todo o corpo. O alongamento passivo dos músculos também é doloroso, e trismo, que é semelhante ao tétano, é comum. Isso é seguido mais tarde por sintomas típicos de outros envenenamentos por elapídeos, uma paralisia flácida progressiva, começando com ptose e paralisia dos músculos voluntários. A paralisia dos músculos envolvidos na deglutição e respiração pode ser fatal.[32]
Vick et al (1975) estimaram que a DL50 de três venenos de cobras marinhas (H. platurus, L. semifasciata e L. laticaudata) para um humano de 70 kg varia de 7,7 a 21 mg. Dados do único veneno de cobra marinha testado em macacos na época sugeriram que primatas eram ligeiramente mais resistentes aos efeitos do veneno com base na resposta à dose do que camundongos. Ishikawa et al (1985) indicaram uma afinidade de ligação substancialmente menor entre a neurotoxina de cobra marinha e AChR's humanos e de chimpanzés em comparação com outros animais. Em humanos, os alvos do veneno parecem ser principalmente as paredes celulares dos músculos voluntários (esqueléticos) e porções tubulares distais do rim, incluindo a alça de Henle, o túbulo contorcido distal e os túbulos coletores. Sitprija et al (1973) encontraram evidências de necrose tubular em todas as porções dos túbulos renais em dois pacientes gravemente envenenados por cobras marinhas. Os venenos de cobras marinhas em humanos são, portanto, mais frequentemente miotóxicos e/ou nefrotóxicos do que neurotóxicos.[33]
Taxonomia
As cobras marinhas foram inicialmente consideradas uma família unificada e distinta, os Hydrophiidae, que mais tarde passaram a compreender duas subfamílias: os Hydrophiinae, ou cobras marinhas verdadeiras/aquáticas (atualmente com 6 gêneros e 64 espécies), e os mais primitivos Laticaudinae, ou cobras-marítimas (um gênero, Laticauda, com oito espécies). Eventualmente, à medida que ficou claro o quão estreitamente relacionadas as cobras marinhas são aos elapídeos, a situação taxonômica tornou-se menos definida. Alguns taxonomistas responderam movendo as cobras marinhas para a família Elapidae. A maioria dos taxonomistas agora coloca as cobras marinhas nas subfamílias elapídeas Hydrophiinae e Laticaudinae, embora esta última possa ser omitida se Laticauda for incluída nos Hydrophiinae. Diferentemente dos Hydrophiinae tradicionais, os Hydrophiinae como atualmente vistos também incluem elapídeos terrestres australasianos.[34][2][8][9][4]
| Gênero[2] | Autoridade taxonômica[34] | Espécies[2] | Subesp.[34][a] | Distribuição geográfica[35] |
|---|---|---|---|---|
| Aipysurus [en] | Lacépède, 1804 | 9 | 1 | Mar de Timor, mar do sul da China, golfo da Tailândia e costas da Austrália (Território do Norte, Queensland, Austrália Ocidental), Nova Caledônia, Ilhas Lealdade, sul da Nova Guiné, Indonésia, oeste da Malásia e Vietnã. |
| Emydocephalus [en] | Krefft, 1869 | 3 | 0 | Costas de Timor (mar da Indonésia), Nova Caledônia, Austrália (Território do Norte, Queensland, Austrália Ocidental) e no mar do Sudeste Asiático ao longo das costas da China, Taiwan, Japão e Ilhas Ryukyu. |
| Ephalophis | M.A. Smith, 1931 | 1 | 0 | Noroeste da Austrália. |
| Hydrelaps | Boulenger, 1896 | 1 | 0 | Norte da Austrália, sul da Nova Guiné. |
| Hydrophis [en] | Latreille in Sonnini & Latreille, 1801 | 49 | 3 | Águas indo-australianas e do Sudeste Asiático.[36] |
| Laticauda | Laurenti, 1768 | 8 | 0 | Águas do Sudeste Asiático e indo-australianas. |
| Parahydrophis | Burger & Natsuno, 1974 | 1 | 0 | Norte da Austrália, sul da Nova Guiné. |
- ↑ Sem contar a subespécie nominada
Estudos moleculares
Estudos de dados moleculares sugerem que os três gêneros monotípicos semiaquáticos (Ephalophis, Parahydrophis e Hydrelaps) são linhagens divergentes iniciais.[37]
Cativeiro
Na melhor das hipóteses, as cobras marinhas são cativas difíceis. Ditmars descreveu-as como cativas nervosas e delicadas que geralmente se recusam a comer, preferindo apenas se esconder no canto mais escuro do tanque.[8] Mais de 50 anos depois, Mehrtens escreveu que, embora raramente fossem exibidas em parques zoológicos ocidentais, algumas espécies estavam regularmente em exibição em aquários japoneses. O suprimento de alimentos disponível limita o número de espécies que podem ser mantidas em cativeiro, já que algumas têm dietas muito especializadas. Além disso, algumas espécies parecem intolerantes ao manuseio, ou mesmo à remoção da água. Quanto aos seus requisitos em cativeiro, as espécies de Laticauda precisam poder sair da água em algum lugar a cerca de 29 ºC, juntamente com um abrigo submerso. Espécies que se saíram relativamente bem em cativeiro incluem a serpente-marinha-nipônica, H. cyanocinctus [en], que se alimenta de peixes e enguias em particular. H. platurus tem se saído especialmente bem em cativeiro, aceitando peixes pequenos, incluindo peixinhos-dourados. Hospedá-las em tanques redondos, ou em tanques retangulares com cantos bem arredondados, impede que as cobras danifiquem seus focinhos nas laterais.[9]
Estado de conservação
A maioria das cobras marinhas não está nas listas de proteção do CITES.[10][38] Uma espécie, L. crockeri, é classificada como vulnerável. Várias espécies de Aipysurus estão listadas com status de conservação de maior preocupação, a espécie de Timor A. fuscus é conhecida por estar ameaçada, e outras duas encontradas em mares ao norte da Austrália, a de escamas folhosas A. foliosquama e a de nariz curto A. apraefrontalis [en], são classificadas como criticamente em perigo de acordo com a Lista Vermelha de Espécies Ameaçadas da IUCN.[39]
Ver também
- Mordida de cobra
- Serpente marinha - mitologia
Referências
- ↑ Dudgeon, Christine L.; White, William T. (2012). «First record of potential Batesian mimicry in an elasmobranch: juvenile zebra sharks mimic banded sea snakes?». Marine and Freshwater Research (em inglês). 63 (6). 545 páginas. Bibcode:2012MFRes..63..545D. ISSN 1323-1650. doi:10.1071/MF11211
- ↑ a b c d Uetz, P.; Freed, P.; Aguilar, R.; Hošek, J., eds. (2022). «Elapidae». The Reptile Database. Consultado em 9 de maio de 2022
- ↑ Minton, S. A. (1983). «Lethal toxicity of venoms of snakes from the Coral Sea». Toxicon. 21 (6): 901–902. Bibcode:1983Txcn...21..901M. PMID 6658813. doi:10.1016/0041-0101(83)90082-x
- ↑ a b Hutchings, Pat (2008). The Great Barrier Reef: Biology, Environment and Management. [S.l.]: Csiro Publishing. p. 345. ISBN 9780643099975.
Sea snakes are true reptiles closely related to Australian venomous terrestrial snakes. Indeed, both groups are included in a single subfamily, Hydrophiinae, by most modern herpetologists.
- ↑ a b c d e f g Parker HW, Grandison AGC. 1977. Snakes – a natural history. Second Edition. British Museum (Natural History) and Cornell University Press. 108 pp. 16 plates. LCCCN 76-54625. ISBN 0-8014-1095-9 (cloth), ISBN 0-8014-9164-9 (paper).
- ↑ a b c d e f g h i Stidworthy J. 1974. Snakes of the World. Grosset & Dunlap Inc. 160 pp. ISBN 0-448-11856-4.
- ↑ a b c d e Fichter GS. 1982. Poisonous Snakes. A First Book. Franklin Watts. 66 pp. ISBN 0-531-04349-5.
- ↑ a b c d e Ditmars RL. 1933. Reptiles of the World. Revised Edition. The MacMillan Company. 329 pp. 89 plates.
- ↑ a b c d e f g h i j k l m Mehrtens JM. 1987. Living Snakes of the World in Color. New York: Sterling Publishers. 480 pp. ISBN 0-8069-6460-X.
- ↑ a b c d e f g Rasmussen, A.R. (2001). «Sea snakes». In: Kent E. Carpenter; Volker H. Niem. The living marine resources of the Western Central Pacific. Col: FAO species identification guide for fishery purposes. Roma: Food and Agriculture Organization of the United Nations. pp. 3987–4008. Consultado em 7 de agosto de 2007. Arquivado do original (PDF) em 6 de fevereiro de 2019
- ↑ a b Campbell JA, Lamar WW. 2004. The Venomous Reptiles of the Western Hemisphere. Comstock Publishing Associates, Ithaca and London. 870 pp. 1500 plates. ISBN 0-8014-4141-2.
- ↑ Shine, R.; Phillips, B.; Waye, H.; LeMaster, M.; Mason, R. T. (14 de maio de 2003). «Chemosensory cues allow courting male garter snakes to assess body length and body condition of potential mates». Behavioral Ecology and Sociobiology (em inglês). 54 (2): 162–166. Bibcode:2003BEcoS..54..162S. ISSN 0340-5443. doi:10.1007/s00265-003-0620-5
- ↑ Young, Bruce A. (1 de setembro de 2003). «Snake bioacoustics: toward a richer understanding of the behavioral ecology of snakes». The Quarterly Review of Biology. 78 (3): 303–325. ISSN 0033-5770. PMID 14528622. doi:10.1086/377052
- ↑ a b Sensory Evolution on the Threshold: Adaptations in Secondarily Aquatic Vertebrates (em inglês) 1 ed. [S.l.]: University of California Press. 4 de fevereiro de 2008. ISBN 9780520252783
- ↑ Hart, Nathan S.; Coimbra, João Paulo; Collin, Shaun P.; Westhoff, Guido (15 de abril de 2012). «Photoreceptor types, visual pigments, and topographic specializations in the retinas of hydrophiid sea snakes». The Journal of Comparative Neurology. 520 (6): 1246–1261. ISSN 1096-9861. PMID 22020556. doi:10.1002/cne.22784
- ↑ Simões, Bruno F.; Sampaio, Filipa L.; Loew, Ellis R.; Sanders, Kate L.; Fisher, Robert N.; Hart, Nathan S.; Hunt, David M.; Partridge, Julian C.; Gower, David J. (27 de janeiro de 2016). «Multiple rod–cone and cone–rod photoreceptor transmutations in snakes: evidence from visual opsin gene expression». Proc. R. Soc. B (em inglês). 283 (1823). 20152624 páginas. Bibcode:2016RSPSB.28352624S. ISSN 0962-8452. PMC 4795032
 . PMID 26817768. doi:10.1098/rspb.2015.2624
. PMID 26817768. doi:10.1098/rspb.2015.2624
- ↑ Heatwole, H; Cogger, H (1993). Fauna of Australia (PDF). Canberra, Austrália: AGPS. 16 páginas
- ↑ Heatwole, Harold (1 de janeiro de 1999). Sea Snakes (em inglês). [S.l.]: UNSW Press. ISBN 9780868407760
- ↑ Van Der Kooij, Jeroen; Povel, David (1996). «Scale Sensillae of the File Snake (Serpentes: Acrochordidae) and Some Other Aquatic and Burrowing Snakes». Netherlands Journal of Zoology. 47 (4): 443–456. doi:10.1163/156854297X00111. Consultado em 2 de abril de 2016
- ↑ Soares, Daphne (16 de maio de 2002). «Neurology: An ancient sensory organ in crocodilians». Nature (em inglês). 417 (6886): 241–242. Bibcode:2002Natur.417..241S. ISSN 0028-0836. PMID 12015589. doi:10.1038/417241a
- ↑ Westhoff, Guido; Fry, Bryan G.; Bleckmann, Horst (1 de janeiro de 2005). «Sea snakes (Lapemis curtus) are sensitive to low-amplitude water motions». Zoology. 108 (3): 195–200. Bibcode:2005Zool..108..195W. ISSN 0944-2006. PMID 16351967. doi:10.1016/j.zool.2005.07.001
- ↑ Shine, R. (13 de janeiro de 2005). «All at sea: aquatic life modifies mate-recognition modalities in sea snakes (Emydocephalus annulatus, Hydrophiidae)». Behavioral Ecology and Sociobiology (em inglês). 57 (6): 591–598. Bibcode:2005BEcoS..57..591S. ISSN 0340-5443. doi:10.1007/s00265-004-0897-z
- ↑ Zimmerman, K; Heatwole, H (1990). «Cutaneous Photoreception: A New Sensory Mechanism for Reptiles». Copeia. 1990 (3): 860–862. JSTOR 1446454. doi:10.2307/1446454
- ↑ Liu, Y.-L.; Lillywhite, H. B.; Tu, M.-C. (3 de julho de 2010). «Sea snakes anticipate tropical cyclone». Marine Biology (em inglês). 157 (11): 2369–2373. Bibcode:2010MarBi.157.2369L. ISSN 0025-3162. doi:10.1007/s00227-010-1501-x
- ↑ a b c d U.S. Navy. 1991. Poisonous Snakes of the World. US Govt. New York: Dover Publications Inc. 203 pp. ISBN 0-486-26629-X.
- ↑ Spawls S, Branch B. 1995. The Dangerous Snakes of Africa. Ralph Curtis Books. Dubai: Oriental Press. 192 pp. ISBN 0-88359-029-8.
- ↑ Slaughter RJ, Beasley DM, Lambie BS, Schep LJ (2009). «New Zealand's venomous creatures». New Zealand Medical Journal. 122 (1290): 83–97. PMID 19319171
- ↑ «Venomous Yellow-Bellied Sea Snake Washes Up on Coronado Beach». 12 de janeiro de 2016
- ↑ a b The sea snakes are coming at NewScientist. Accessed 13 January 2009.
- ↑ Vernberg, F. John (2014). Behavior and Ecology. [S.l.]: Elsevier Science. p. 186. ISBN 978-0-323-16269-2
- ↑ Smith, Emily (8 de outubro de 2018). «Fisherman's deadly encounter with sea snake incredibly rare». ABC News (em inglês)
- ↑ Warrell DA. 2004. Snakebites in Central and South America: Epidemiology, Clinical Features, and Clinical Management. In Campbell JA, Lamar WW. 2004. The Venomous Reptiles of the Western Hemisphere. Comstock Publishing Associates, Ithaca and London. 870 pp. 1500 plates. ISBN 0-8014-4141-2.
- ↑ Gopalakrishnakone, P. (1994). Sea Snake Toxinology (em inglês). [S.l.]: NUS Press. ISBN 978-9971-69-193-6
- ↑ a b c «Elapidae» (em inglês). ITIS (www.itis.gov). Consultado em 7 de agosto de 2007
- ↑ Elapidae Arquivado em 2008-10-11 no Wayback Machine at the New Reptile Database. Accessed 12 August 2007.
- ↑ The Hydrophiidae at Cyberlizard's home pages. Accessed 12 August 2007.
- ↑ Sanders, KL; Lee; Mumpuni, Bertozzi T; Rasmussen, AR (2012). «Multilocus phylogeny and recent rapid radiation of the viviparous sea snakes (Elapidae: Hydrophiinae)». Molecular Phylogenetics and Evolution. 66 (3): 575–591. PMID 23026811. doi:10.1016/j.ympev.2012.09.021
- ↑ Serpentes Arquivado em 2020-05-30 no Wayback Machine at CITES. Accessed 11 August 2007.
- ↑ «Red list search». IUCN Red List (em inglês). Consultado em 16 de junho de 2023. Cópia arquivada em 6 de novembro de 2009
Literatura adicional
- Rasmussen AR. 1997. Systematics of sea snakes; a critical review. Symp. Zool. Soc. London 70, 15-30.
- Smith MA. 1926. Monograph of the sea snakes (Hydrophiidae). British Museum of Natural History, London.
- Voris HK. 1977. A phylogeny of the sea snakes (Hydrophiidae). Fieldiana Zool. 70, 79-169.
- Whitaker R. 1978. Common Indian Snakes: A Field Guide. Macmillan India Limited.
Ligações externas
- Cobras marinhas na Australia
- Cobras marinhas em Scubadoc's Diving Medicine Online
- Mergulho no Gunung Api: Vulcão das cobras marinhas - Relato em primeira mão de mergulhadores interagindo com cobras marinhas no vulcão indonésio Gunung Api, junho de 2009.
