Cloreto de vanádio(IV)
Vanadium tetrachloride
| |||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||
| Nomes | |||||||||||||||||||||||
| Nome IUPAC | Tetracloreto de vanádio Cloreto de vanádio(IV) | ||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| |||||||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||||||
Cloreto de vanádio(IV) ou tetracloreto de vanádio é um composto inorgânico de fórmula VCl4. Em condições normais de temperatura e pressão, apresenta-se como um líquido de coloração vermelho-escura, volátil e sensível à umidade. É utilizado como reagente na preparação de outros compostos de vanádio e como catalisador em síntese orgânica e processos de polimerização.
Síntese e propriedades
O cloreto de vanádio(IV) é preparado industrialmente pela cloração direta de vanádio metálico ou de óxidos de vanádio a elevada temperatura, em presença de cloro gasoso:[1]
- V + 2 Cl2 → VCl4
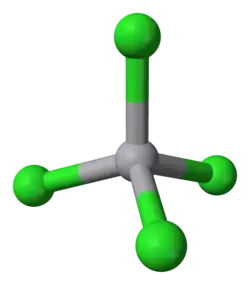
O composto contém vanádio no estado de oxidação +4 e apresenta geometria aproximadamente tetraédrica na fase gasosa e líquida. Possui um elétron desemparelhado em relação ao TiCl4, que é diamagnético, o que torna o VCl4 um líquido paramagnético em condições ambientais. É um dos poucos líquidos moleculares simples que exibem paramagnetismo nas CNTP.
Na presença de água, VCl4 sofre intensa hidrólise, formando ácido clorídrico e espécies oxocloradas de vanádio (por exemplo, VOCl3), o que explica o odor irritante e o caráter corrosivo do composto.
Aplicações
VCl4 é utilizado como catalisador na polimerização de alcenos, em especial na produção de certas borrachas sintéticas e polímeros relacionados. Nesses sistemas, o tetracloreto de vanádio atua em conjunto com co-catalisadores organometálicos (como trietilalumínio), de forma análoga aos sistemas de Ziegler–Natta, formando intermediários alquilvanádio ativos na inserção de monómeros.
Síntese orgânica
Na síntese orgânica, VCl4 é empregado como agente oxidante em reações de acoplamento de fenols, promovendo a formação de biarilfenóis. Um exemplo é a conversão do fenol em 4,4'-bisfenol, com redução concomitante do vanádio de +4 para +3:[1]
- 2 C6H5OH + 2 VCl4 → HOC6H4–C6H4OH + 2 VCl3 + 2 HCl
Esta reação ilustra a capacidade do cloreto de vanádio(IV) de atuar como oxidante em meio clorídrico, gerando cloreto de vanádio(III) como produto de redução.
Segurança
VCl4 é um líquido volátil, corrosivo e oxidante, que hidrolisa rapidamente em contato com a umidade do ar ou com água, liberando grandes quantidades de ácido clorídrico gasoso. A inalação de vapores ou o contato com a pele e olhos pode causar queimaduras químicas severas. O manuseio deve ser realizado em capela de exaustão, com uso de equipamentos de proteção individual adequados (luvas resistentes a produtos químicos, proteção ocular e máscara apropriada), e armazenamento em recipientes hermeticamente fechados, ao abrigo de umidade e fontes de calor.
Referências
- ↑ a b Calderazzo, F.; Maichle-Mössmer, C.; Pampaloni, G.; Strähle, J. (1993). «Low-temperature Syntheses of Vanadium(III) and Molybdenum(IV) Bromides by Halide Exchange». Dalton Transactions: 655–658. doi:10.1039/DT9930000655
