Cloreto de titânio(II)
Cloreto de titânio(II)
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| Página de dados suplementares | |||||||||||||||||
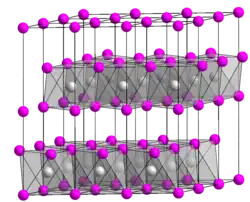
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||
Cloreto de titânio (II) é o composto químico com a fórmula química TiCl2. Apresenta-se como um sólido preto e tem sido estudado apena moderadamente, provavelmente por causa de sua alta reatividade.[3] Ti(II) é um forte agente redutor: tem uma alta afinidade por oxigênio e reage irreversivelmente com água para produzir H2. A preparação usual é a desprotonação térmica de TiCl3 a 500 °C. O equilíbrio é "conduzido" pela perda do volátil TiCl4:
- 2 TiCl3 → TiCl2 + TiCl4
Referências
- ↑ a b c Registo de CAS RN 10049-06-6 na Base de Dados de Substâncias GESTIS do IFA
- ↑ Datenblatt bei WebElements (englisch)
- ↑ Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.