Cloreto de tálio(I)
Cloreto de tálio(I)
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||
| Nomes | |||||||||||||||
| Nome IUPAC | Cloreto de tálio(I) | ||||||||||||||
| Outros nomes | Monocloreto de tálio | ||||||||||||||
| Entalpia padrão de formação ΔfH |
-204 kJ/mol[1] | ||||||||||||||
| PubChem | |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
O cloreto de tálio(I) é um sal inorgânico branco de fórmula mínima TlCl. Ele pode ser obtido mediante adição de cloreto a uma solução acidificada de sais solúveis de Tl(I), como perclorato de tálio(I), sulfato de tálio(I) ou nitrato de tálio(I)[1]. O raro mineral lafossaite, de fórmula Tl(Cl,Br), é uma forma na qual o cloreto de tálio(I) pode ser encontrado naturalmente[2].
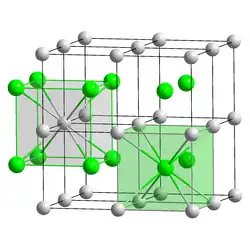
A estrutura cristalina do cloreto de tálio(I) é similar à do cloreto de césio (CsCl), isto é, apresenta célula unitária de geometria cúbica de corpo centrado (CCC), visto a presença do cátion volumoso Tl+. Assim como o cloreto de prata, o TlCl é fotossensível e, portanto, se decompõe quando exposto a luminosidade[1].
Diferentemente dos outros elementos do grupo 13 da Tabela Periódica (B, Al, Ga e In), o Tl apresenta número de oxidação +1 como mais estável, o que lhe confere a particularidade de ser o único, dentre os metais de seu grupo, que pode se apresentar associado estavelmente a qualquer um dos halogenetos (F-, Cl-, Br- e I-), tanto na forma sólida, quanto em meio aquoso[3].
Sob condições normais de pressão, o TlCl apresenta condutividade elétrica desprezível e band gab da ordem de 3 eV (~300 kJ.mol-1), assim sendo, é um excelente material isolante. No entanto, sob altas pressões, a medida que os íons são forçados a se aproximar, torna-se um condutor metálico[1].
1. Livro: Perry,Dale L,Philips,Sidney L.(1995) Handbook of Inorganic Compounds, CRC Press pág.406, ISBN 0-8493-8671-3
- Esta categoria reúne artigos sobre Tálio.
- ↑ a b c d e f g h i GREENWOOD, N. N.; EARNSHAW, A. (1997). Chemistry of the Elements 2. ed. Oxford: Elsevier. p. 241. 1342 páginas
- ↑ HIM, Hudson Institute of Mineralogy (9 de junho de 2021). «Lafossaite». Mindat. Consultado em 1 de julho de 2021
- ↑ SHRIVER, D. F.; ATKINS; OVERTON; ROURKE; WELLER; ARMSTRONG (2008). Química Inorgânica 4. ed. Porto Alegre: Bookman. p. 332. 848 páginas
-chloride-3D-SF-C.png)