Cloreto de gálio(III)
Cloreto de gálio(III)
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||
| Nomes | |||||||||||||||||
| Outros nomes | Gallium(III) chloride, Trichlorogallium, Trichlorogallane | ||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| Página de dados suplementares | |||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||
Cloreto de gálio(III) é um composto químico inorgânico com a fórmula que forma um mono hidrato, . O cloreto de gálio(III) sólido é um cristal incolor deliquescente e existe como um dímero com a fórmula . É incolor e solúvel em praticamente todos os solventes, até mesmo alcanos , o que é incomum para um haleto metálico. É o principal precursor da maioria dos derivados de gálio e um reagente em síntese orgânica .
Como um ácido de Lewis, o é mais suave que o cloreto de alumínio . Também é mais fácil de reduzir do que o cloreto de alumínio. A química de coordenação do Ga(III) e do Fe(III) é semelhante, portanto, o cloreto de gálio(III) tem sido usado como um análogo diamagnético do cloreto férrico .
Preparação
O cloreto de gálio (III) pode ser preparado a partir dos elementos aquecendo o metal gálio em uma corrente de cloro a 200 °C e purificando o produto por sublimação sob vácuo.
- 2 Ga + 3 Cl 2 → 2 GaCl 3
Também pode ser preparado aquecendo óxido de gálio com cloreto de tionila :
- Ga 2 O 3 + 3 SOCl 2 → 2 GaCl 3 + 3 SO 2
O metal gálio reage lentamente com o ácido clorídrico , produzindo gás hidrogênio . A evaporação desta solução produz o monohidrato.
Estrutura
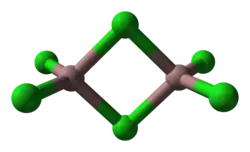
[ editar fonte ] Como um sólido, ele adota uma estrutura bitédrica com dois cloretos em ponte. Sua estrutura se assemelha à do tribrometo de alumínio . Em contraste, AlCl3 e InCl3 contêm 6 centros metálicos coordenados. Como consequência de sua natureza molecular e baixa energia de rede associada, o cloreto de gálio (III) tem um ponto de fusão mais baixo em comparação aos haletos de alumínio e índio (III) . A fórmula de Ga2Cl6 é frequentemente escrita como Ga2 ( μ-Cl ) 2Cl4 .
Na fase gasosa, o dimérico ( Ga 2 Cl 6 ) e o monomérico trigonal planar ( GaCl 3 ) estão em um equilíbrio dependente da temperatura, com temperaturas mais altas favorecendo a forma monomérica. A 870 K, todas as moléculas da fase gasosa estão efetivamente na forma monomérica.
No monohidrato, o gálio é coordenado tetraedricamente com três moléculas de cloro e uma molécula de água.
Propriedades
[ editar fonte ]
Físico
[ editar fonte ] O cloreto de gálio(III) é um sólido incolor , diamagnético e deliquescente , que funde a 77,9 °C e entra em ebulição a 201 °C sem se decompor em elementos. Este baixo ponto de fusão resulta do fato de formar moléculas discretas de Ga2Cl6 no estado sólido. O cloreto de gálio(III) dissolve-se em água com liberação de calor, formando uma solução incolor que, ao evaporar, produz um monoidrato incolor, que funde a 44,4 °C.
Químico
[ editar fonte ] O gálio é o membro mais leve do Grupo 13 a ter uma camada d completa , (o gálio tem a configuração eletrônica [ Ar ] 3 d 10 4 s 2 4 p 1 ) abaixo dos elétrons de valência que poderiam participar da ligação π da camada d com ligantes . O baixo estado de oxidação do Ga em Ga(III)Cl 3 , juntamente com a baixa eletronegatividade e a alta polarizabilidade , permitem que o GaCl 3 se comporte como um "ácido macio" em termos da teoria HSAB . A força das ligações entre haletos de gálio e ligantes foi extensivamente estudada. O que emerge é:
- GaCl3 é um ácido de Lewis mais fraco que AlCl3 em relação aos doadores de N e O , por exemplo, piridina
- GaCl3 é um ácido de Lewis mais forte que AlCl3 em relação aos tioéteres , por exemplo, sulfeto de dimetila , ( CH3 ) 2S
Com um íon cloreto como ligante, o íon tetraclorogalato(III) tetraédrico [GaCl 4 ] − é produzido, a coordenada 6 [GaCl 6 ] 3− não pode ser feita. Compostos como K[Ga 2 Cl 7 ] que têm um ânion cloreto em ponte são conhecidos. Em uma mistura fundida de KCl e GaCl 3 , existe o seguinte equilíbrio:
- 2 [GaCl 4 ] − ⇌ [Ga 2 Cl 7 ] − + Cl −
Quando dissolvido em água, o cloreto de gálio(III) dissocia-se nos íons octaédricos [Ga(H 2 O) 6 ] 3+ e Cl − formando uma solução ácida, devido à hidrólise do íon hexaaquogálio(III):
- [Ga(H2O ) 6 ] 3+ → [Ga(H2O ) 5OH ] 2+ + H + ( pKa = 3,0)
Em solução básica, ele se hidrolisa em hidróxido de gálio (III) , que se dissolve novamente com a adição de mais hidróxido , possivelmente para formar [Ga (OH) 4 ] − .
Usos
[ editar fonte ]
Síntese orgânica
[ editar fonte ] O cloreto de gálio(III) é um catalisador ácido de Lewis , como na reação de Friedel-Crafts , capaz de substituir ácidos de Lewis mais comuns, como o cloreto férrico . O gálio forma complexos fortes com doadores π, especialmente sililetinos , produzindo um complexo fortemente eletrofílico. Esses complexos são usados como agentes alquilantes para hidrocarbonetos aromáticos.
Também é usado em reações de carbogalação de compostos com ligação tripla carbono-carbono. Também é usado como catalisador em muitas reações orgânicas.
Compostos organogálios
[ editar fonte ] É um precursor de reagentes organogálio . Por exemplo, o trimetilgálio , um composto organogálio usado em MOCVD para produzir vários semicondutores contendo gálio , é produzido pela reação do cloreto de gálio (III) com vários agentes alquilantes, como dimetilzinco , trimetilalumínio ou iodeto de metilmagnésio .
Purificação de gálio
[ editar fonte ] O cloreto de gálio (III) é um intermediário em vários processos de purificação de gálio, onde o cloreto de gálio (III) é destilado fracionadamente ou extraído de soluções ácidas.
Detecção de neutrinos solares
[ editar fonte ] 110 toneladas de solução aquosa de cloreto de gálio(III) foram utilizadas nos experimentos GALLEX e GNO realizados nos Laboratori Nazionali del Gran Sasso, na Itália, para detectar neutrinos solares . Nesses experimentos, o germânio -71 foi produzido por interações de neutrinos com o isótopo gálio-71 (que possui uma abundância natural de 40%), e os decaimentos beta subsequentes do germânio-71 foram medidos.
