Ceratioidei
| Ceratioidei | |
|---|---|

| |
| Diversidade de Ceratioidei.[a] | |
| Classificação científica | |
| Reino: | Animalia |
| Filo: | Chordata |
| Classe: | Actinopterygii |
| Ordem: | Lophiiformes |
| Subordem: | Ceratioidei Regan, 1912 |
| Famílias | |
|
ver texto | |
Ceratioidei, os peixes-pescadores pelágicos ou peixes-pescadores de águas profundas,[b] é uma subordem de peixes com nadadeiras raiadas, uma das cinco subordens da ordem Lophiiformes, os peixes-pescadores. Esses peixes são encontrados em mares tropicais e temperados de todo o mundo, vivendo acima do fundo do oceano profundo, na zona pelágica.
Os peixes-pescadores de águas profundas apresentam dimorfismo sexual extremo: os machos são muitas vezes menores que as fêmeas. Para se reproduzir, o macho procura uma fêmea e utiliza seus dentículos afiados, semelhantes a dentes, para se prender a ela. Os detalhes desse parasitismo sexual variam entre as espécies; em várias delas, o macho passa a fazer parte permanente da fêmea, com seus tecidos fundindo-se aos dela. Esse é o único exemplo natural conhecido de um processo chamado parabiose. A esca, característica definidora de todos os grupos de peixes-pescadores, é bioluminescente nos peixes-pescadores de águas profundas, atraindo presas na imensa escuridão da zona batipelágica que eles habitam.
Etimologia
Ceratioidei recebe seu nome do gênero Ceratias, o gênero tipo da família Ceratiidae e da subordem. Ceratias significa "portador de chifre", uma alusão à esca que se projeta do focinho, comparada a um chifre.[1]
Taxonomia
Ceratioidei foi proposto pela primeira vez como um agrupamento em 1912 pelo ictiólogo inglês Charles Tate Regan, como a divisão Ceratiformes dentro da subordem Lophoidea da ordem Pediculati, a qual incluía a família Batrachoididae.[2] Atualmente, os Batrachoididae não são mais considerados intimamente relacionados aos peixes-pescadores, que hoje são incluídos na ordem Lophiiformes; dentro desse clado, os Ceratioidei pertencem ao mesmo clado que os Chaunacoidei, tendo os Antennarioidei e os Ogcocephaloidei como grupos irmãos desse clado.[3] A 5.ª edição de Fishes of the World trata esse agrupamento como uma subordem dentro de Lophiiformes.[4]
A classificação dessa subordem baseia-se principalmente em características específicas das fêmeas, como a morfologia da esca, embora algumas características osteológicas e merísticas sejam compartilhadas entre os sexos. Os machos de peixes-pescadores podem ser identificados até o nível de gênero por meio das características dos dentículos em forma de "dentes"[c] e da morfologia das narinas, mas a identificação em nível de espécie não foi possível, mesmo ao examinar machos parasitas.[6][7][5]:194
Ceratioidei inclui as seguintes famílias:[4][8]
- Ceratiidae Gill, 1861
- Himantolophidae Gill, 1861
- Melanocetidae Gill, 1878
- Oneirodidae Gill, 1878
- Caulophrynidae Goode & Bean, 1896
- Gigantactinidae Boulenger, 1904
- Thaumatichthyidae Smith & Radcliffe, 1912
- Linophrynidae Regan, 1925
- Neoceratiidae Regan, 1926
- Diceratiidae Regan & Trewavas, 1932
- Centrophrynidae Bertelsen, 1951
Evolução
Presume-se que os Ceratioidei derivem de um ancestral semelhante aos Chaunacoides modernos (sapos marinhos de águas profundas) ou Ogcocefalóides (peixes-morcego), que viviam em habitats bentônicos ou litorâneos, e que eventualmente mantiveram os habitats pelágicos da larva Lophiiforme até a adolescência. A monofilia é sustentada neste grupo através das características compartilhadas de extremo dimorfismo sexual, perda das nadadeiras pélvicas ambulatórias encontradas em outros peixes-pescadores, realocação das nadadeiras peitorais e uma redução geral na densidade através da perda de partes ósseas, diminuição da ossificação e da massa muscular e infusão de lipídios por todo o corpo.[7]:230
.jpg)

Um estudo de 2024 descobriu que, embora os Ceratioidei provavelmente tenham divergido dos Chaunacidae durante o Paleoceno, a diversificação em suas várias famílias existentes só ocorreu ao longo do Eoceno, após o Máximo térmico do Paleoceno-Eoceno. Isso provavelmente também coincide com sua colonização de habitats de águas profundas. Antes dessas radiações, os Ceratioidei ancestrais desenvolveram dimorfismo sexual extremo de tamanho e perderam independentemente genes imunológicos adaptativos, como o aicda, que permitia que os machos do peixe-pescador se fundissem com as fêmeas, levando, em última análise, à evolução de seu parasitismo sexual.[9][10][11]
Uma explicação para a evolução do parasitismo sexual é que a densidade relativamente baixa de fêmeas em ambientes de águas profundas deixa pouca oportunidade para a escolha de parceiros entre os peixes-pescadores. As fêmeas permaneceram relativamente grandes para melhorar a fecundidade: uma fêmea maior seria capaz de ter ovários e óvulos volumetricamente maiores. Espera-se que os machos diminuam de tamanho para reduzir os custos metabólicos em ambientes com poucos recursos e desenvolvam habilidades altamente especializadas para encontrar fêmeas. Se um macho é capaz de encontrar parceiras e se associar permanentemente a elas (eventualmente levando ao desenvolvimento da fusão), então é mais provável que ele melhore seu sucesso reprodutivo ao longo da vida em relação aos machos de vida livre, particularmente quando a perspectiva de encontrar futuras parceiras é baixa; como um macho associado está sempre disponível para a fêmea para acasalamento, ele pode potencialmente participar de múltiplos eventos de fertilização, garantindo a paternidade para cada evento em que estiver associado. Por outro lado, maiores probabilidades de encontros entre machos e fêmeas em um habitat podem estar correlacionadas com espécies que demonstram parasitismo facultativo ou um acasalamento por contato temporário mais tradicional.[12][11]
Devido aos ambientes extremos que habitam, os restos fósseis de peixes-pescadores de águas profundas são muito raros no registro geológico. Apenas algumas formações em todo o mundo os preservam, as quais tendem a ter sido depositadas em regiões tectonicamente ativas, onde sedimentos de águas profundas puderam ser erguidos para a superfície. Estas incluem a Formação Puente da Califórnia, Estados Unidos, e a Formação Kurasi da Ilha Sakhalin, Rússia. Estas formações datam do Mioceno Médio-tardio, e os espécimes recuperados delas são atribuídos a gêneros existentes.[13][14][15][16]
Parasitismo sexual
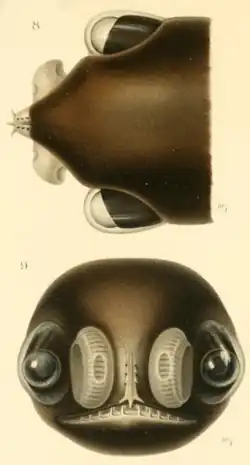
O parasitismo sexual é um modo de reprodução sexual exclusivo dos Ceratioidei, facilitado pelo seu extremo dimorfismo sexual. O cerne desse comportamento é a fixação física dos machos ao corpo da fêmea para a reprodução, que se divide em três categorias: parasitismo obrigatório, em que os machos precisam se fixar permanentemente às fêmeas e fundir seus tecidos; fixação temporária não parasitária, em que os machos conseguem viver independentemente; e parasitismo facultativo, em que ocorrem tanto a fixação parasitária quanto machos independentes. O termo "parasitismo sexual" é usado porque os machos das espécies parasitas obrigatórias são incapazes de se alimentar após a metamorfose e precisam se fixar à fêmea para obter nutrição, de forma semelhante a um ectoparasita. Se não encontrarem uma parceira, presume-se que os machos morram. Além disso, a maturação sexual nessas espécies é desencadeada pela fixação do macho à fêmea. Esse comportamento evoluiu múltiplas vezes dentro do grupo, tendo se desenvolvido independentemente de três a cinco vezes. A diversidade na natureza e localização da fixação dos machos são evidência de evolução independente.[7][6][17][10][11]
Geralmente, os machos localizam suas parceiras por meio de uma combinação de meios visuais e olfativos, embora se acredite que algumas espécies se especializem em um sentido em detrimento do outro: algumas dependem exclusivamente da visão, possuindo um campo de visão binocular excepcionalmente amplo para detectar carúnculas bioluminescentes no dorso das fêmeas (Ceratiidae), ou estruturas olfativas excepcionalmente desenvolvidas em suas narinas para detectar feromônios femininos (Gigantactinidae). Em algumas famílias, como Centrophrynidae e Neoceratiidae, os métodos que os machos usam para localizar as fêmeas permanecem obscuros.[7]:229, 232
Em espécies parasitas obrigatórias, o macho morde a pele da fêmea usando o "aparelho denticular",[c] iniciando o processo de fusão e eventualmente recebendo nutrientes através de seus sistemas circulatórios conectados,[11] embora ele retenha brânquias funcionais e providencie suas próprias necessidades de oxigênio; o ponto de fixação do macho, uma protuberância do tecido da fêmea semelhante a um mamilo ou um pedúnculo, frequentemente deixa uma abertura por onde a água pode fluir através de sua boca e sair pelas brânquias. No Neoceratias spinifer, onde os machos foram observados se fixando tão completamente que frequentemente não apresentavam nenhuma abertura oral remanescente, acredita-se que a respiração ocorra através do bombeamento de água para dentro e para fora das aberturas operculares, já que as brânquias permanecem bem desenvolvidas.[7]:225 Após a fusão, os machos aumentam de volume e frequentemente se tornam muito maiores em relação aos machos de vida livre da espécie, e quanto mais tempo um macho permanece fixado, mais atrofiado seu corpo se torna. Embora órgãos sensoriais como os olhos e as narinas degenerem, os corações, as brânquias e os raios das barbatanas dos machos são retidos.[7]:226[d]
.jpg)
Esse parasitismo se desenvolveu a tal ponto que, pelo menos em Ceratiidae e alguns Linophrynidae, ambos os sexos nunca amadurecem (suas gônadas não amadurecem) antes da fusão ocorrer.[7]:229 Após a fusão, eles vivem e permanecem reprodutivamente funcionais enquanto a fêmea estiver viva, podendo participar de múltiplos eventos de desova; essa união da fêmea e do macho tem sido chamada de um único organismo hermafrodita.[18][19] Vários machos podem ser incorporados em uma única fêmea, com até oito machos se fixando em quase qualquer lugar do corpo do Cryptopsaras couesii, embora alguns táxons pareçam ter uma regra estrita de um macho por fêmea, como Linophryne spp., onde os machos quase sempre se fixam na linha média ventral, em frente à abertura genital da fêmea.[7] Este método garante que, quando a fêmea estiver pronta para desovar, ela tenha um parceiro imediatamente disponível,[20] o que foi conjecturado por Charles Tate Regan:
A razão pela qual os ceratóides, os únicos entre os vertebrados, possuem machos desse tipo é evidente. Eles são necessariamente poucos em número em comparação com os peixes mais ativos dos quais se alimentam, e levam uma vida solitária, flutuando na escuridão das profundezas do oceano. Nessas circunstâncias, seria muito difícil para um peixe adulto encontrar uma parceira, mas essa dificuldade parece ter sido, em certa medida, superada pelos machos, logo após a eclosão, quando são relativamente numerosos, fixando-se às fêmeas, se tiverem a sorte de encontrá-las, e permanecendo assim por toda a vida. Com toda a probabilidade, os machos são incapazes de desenvolvimento livre, e é provável que a grande maioria deles não encontre uma fêmea e pereça, embora outra possibilidade tenha sido sugerida, a saber, que os peixes pós-larvais que encontram e se fixam às fêmeas se desenvolvam em machos, e aqueles que não encontram, em fêmeas.
Charles Tate Regan, 1926, Os peixes pediculados da subordem Ceratioidea[21][7]
Estudos subsequentes descobriram que o sexo até mesmo das larvas menores (2-3 mm de comprimento total) pode ser determinado através do desenvolvimento inicial do ilício, que aparece como uma pequena papila indiferenciada no focinho das larvas fêmeas;[22] portanto, a ideia de que o sexo é determinado pela fixação e não fixação é infundada.[7]
Em espécies não parasitárias, incluindo até agora os peixe-pescador-das-profundezas, os peixes-futebol, os Diceratiidae, Gigantactinidae e a maioria dos gêneros de Oneirodidae; ambos os sexos amadurecem independentemente, sem necessidade de fusão, com os machos se fixando temporariamente. De fato, não há evidências de parasitismo sexual e, onde machos de peixe-pescador-das-profundezas foram observados firmemente fixados às suas parceiras, não houve evidência de fusão. O aparelho denticular nesses machos permite que eles se fixem às fêmeas e, presumivelmente, capturem também presas, já que alimento foi encontrado em alguns machos dessas espécies,[e] e eles continuam a crescer após a metamorfose[f] mesmo depois de esgotarem as reservas de energia em seus fígados. É provável que esses machos só se fixem às fêmeas quando estiverem prontos para desovar.[7]:230[5]:195, 291, 305-306[11]
O parasitismo facultativo é conhecido em Caulophrynidae, Leptacanthichthys gracilispinis e Bertella, sendo este último par pertencente à família Oneirodidae. Este método é intermediário entre o não parasitismo e o parasitismo obrigatório; ambos os sexos amadurecem independentemente, mas os machos se fixam independentemente da maturidade da fêmea. Se ambos estiverem sexualmente maduros, desovam, ocorre a fertilização e o macho presumivelmente se desprende para se recuperar, alimentar-se e procurar outra parceira. Se algum dos parceiros não estiver pronto para desovar, o macho se fixa até que estejam prontos; quanto mais tempo ele permanecer fixado, maiores serão as chances de ele se fundir e se tornar um parasita sexual.[7]:230[5]:91, 130, 195, 305-306[11]
A perda efetiva de certos aspectos dos sistemas imunológicos dos Ceratioidei, como o sistema imunológico adaptativo, é um fator chave para permitir a fusão entre os sexos.[23][24][25][11] Presume-se que eles desenvolveram novas estratégias imunológicas que compensam a perda das funções dos linfócitos B e T encontradas em animais com um sistema imunológico adaptativo.[26]
Filogenia
A árvore filogenética abaixo é baseada em Pietsch & Orr (2007);[27]
| Lophiiformes |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Notas
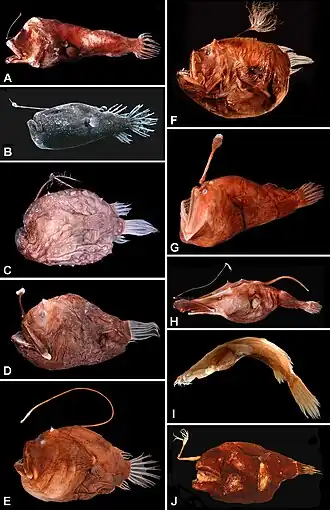
- ↑ As espécies representadas são (Barras de escala = 10 mm):
- A. Ceratias uranoscopus
- B. Himantolophus sp
- C. Melanocetus johnsonii
- D. Thaumatichthys sp.
- E. Chaenophryne draco
- F. Chaenophryne ramifera
- G. Dolopichthys sp.
- H. Oneirodes anisacanthus
- I. Oneirodes carlsbergi
- J. Caulophryne sp.
- ↑ Embora membros das famílias Chaunacidae e Lophiidae também possam viver em águas profundas, este é um nome comum mais ambíguo.
- ↑ a b Não são dentes verdadeiros, sendo formados pela fusão de espículas dérmicas modificadas anteriores (para a frente) das pré-maxilas e dentários, que são os ossos que suportam os dentes verdadeiros em todos os peixes ósseos.[5]:190, 279
- ↑ Mesmo no já mencionado Neoceratias spinifer, onde os machos em estágio avançado de fusão parecem estar "incorporados ou absorvidos pela fêmea", esses órgãos são retidos, sugerindo que ele não depende da parceira para respirar.[5]:279, 298
- ↑ As presas são quetognatos e pequenos crustáceos, embora em algumas espécies estes possam permanecer de alimentações anteriores à metamorfose completa.[5]:263, 291
- ↑ Os machos aumentam em comprimento em 6,5–12 milímetros (0,26–0,47 polegadas), significativo quando os maiores indivíduos desses machos têm 16,5–39 milímetros (0,65–1,54 polegadas) de comprimento.[5]:68, 291, 295, 333, 337
- ↑
- (A) Centrophrynidae: Centrophryne spinulosa;
- (B) Ceratiidae: Cryptopsaras couesii;
- (C) Himantolophidae: Himantolophus appelii;
- (D) Diceratiidae: Diceratias trilobus;
- (E) Diceratiidae: Bufoceratias wedli;
- (F) Diceratiidae: Bufoceratias shaoi;
- (G) Melanocetidae: Melanocetus eustalus;
- (H) Thaumatichthyidae: Lasiognathus amphirhamphus;
- (I) Thaumatichthyidae: Thaumatichthys binghami;
- (J) Oneirodidae: Chaenophryne quasiramifera.
Referências
- ↑ Christopher Scharpf (18 de outubro de 2022). «Order LOPHIIFORMES (part 2): Families CAULOPHRYNIDAE, NEOCERATIIDAE, MELANOCETIDAE, HIMANTOLOPHIDAE, DICERATIIDAE, ONEIRODIDAE, THAUMATICHTHYIDAE, CENTROPHRYNIDAE, CERATIIDAE, GIGANTACTINIDAE and LINOPHRYNIDAE». The ETYFish Project Fish Name Etymology Database. Christopher Scharpf. Consultado em 1 de maio de 2024
- ↑ Regan, C.T. (1912). «The classification of the teleostean fishes of the order Pediculati». Annals and Magazine of Natural History. Series 8. 9 (51): 277–289. doi:10.1080/00222931208693132
- ↑ Arnold, Rachel J. (2014). Evolutionary Relationships of the Enigmatic Anglerfishes (Teleostei: Lophiiformes): Can Nuclear DNA Provide Resolution for Conflicting Morphological and Mitochondrial Phylogenies? (Tese de PhD). University of Washington
- ↑ a b Nelson, J.S.; Grande, T.C.; Wilson, M.V.H. (2016). Fishes of the World 5th ed. Hoboken, NJ: John Wiley & Sons. pp. 508–518. ISBN 978-1-118-34233-6. LCCN 2015037522. OCLC 951899884. OL 25909650M. doi:10.1002/9781119174844
- ↑ a b c d e f g Pietsch, Theodore W. (2009). Oceanic anglerfishes: extraordinary diversity in the deep sea. Berkeley: University of California Press. ISBN 978-0-520-94255-4. OCLC 1298208235
- ↑ a b Bertelsen, E (1984). Ceratioidei: development and relationships. In: Moser HG, Richards WJ, Cohen DM, Fahay MP, Kendall AW Jr, Richardson SL (eds) Ontogeny and systematics of fishes. Lawrence, KS: American Society of Ichthyologists and Herpetologists. pp. 325–334
- ↑ a b c d e f g h i j k l Pietsch, Theodore W. (agosto de 2005). «Dimorphism, parasitism, and sex revisited: modes of reproduction among deep-sea ceratioid anglerfishes (Teleostei: Lophiiformes)»
 . Ichthyological Research. 52 (3): 207–236. Bibcode:2005IchtR..52..207P. ISSN 1341-8998. doi:10.1007/s10228-005-0286-2. Consultado em 1 de março de 2025
. Ichthyological Research. 52 (3): 207–236. Bibcode:2005IchtR..52..207P. ISSN 1341-8998. doi:10.1007/s10228-005-0286-2. Consultado em 1 de março de 2025
- ↑ Richard van der Laan; William N. Eschmeyer; Ronald Fricke (2014). «Family-group names of recent fishes». Zootaxa. 3882 (2): 1–230. PMID 25543675. doi:10.11646/zootaxa.3882.1.1

- ↑ Brownstein, Chase D.; Zapfe, Katerina L.; Lott, Spencer; Harrington, Richard; Ghezelayagh, Ava; Dornburg, Alex; Near, Thomas J. (2024). «Synergistic innovations enabled the radiation of anglerfishes in the deep open ocean». Current Biology. 34 (11): 2541–2550.e4. Bibcode:2024CBio...34.2541B. ISSN 0960-9822. PMID 38788708. doi:10.1016/j.cub.2024.04.066

- ↑ a b Thorsberg, Christian. «Bizarre Sex Helped Anglerfish Diversify and Dominate the Deep Sea, Study Suggests». smithsonianmag.com. Smithsonian Magazine. Consultado em 24 de março de 2025
- ↑ a b c d e f g Cummings, Mike. «Sea of love: Behind the unusual sexual parasitism of deep-water anglerfish». news.yale.edu. Yale University. Consultado em 24 de março de 2025
- ↑ Miya, Masaki; Pietsch, Theodore W; Orr, James W; Arnold, Rachel J; Satoh, Takashi P; Shedlock, Andrew M; Ho, Hsuan-Ching; Shimazaki, Mitsuomi; Yabe, Mamoru; Nishida, Mutsumi (1 de janeiro de 2010). «Evolutionary history of anglerfishes (Teleostei: Lophiiformes): a mitogenomic perspective». BMC Evolutionary Biology. 10 (1). 58 páginas. Bibcode:2010BMCEE..10...58M. PMC 2836326
 . PMID 20178642. doi:10.1186/1471-2148-10-58
. PMID 20178642. doi:10.1186/1471-2148-10-58
- ↑ «PBDB Taxon». paleobiodb.org. Consultado em 29 de novembro de 2024
- ↑ Carnevale, Giorgio; Pietsch, Theodore W.; Takeuchi, Gary T.; Huddleston, Richard W. (2008). «Fossil ceratioid anglerfishes (Teleostei: Lophiiformes) from the Miocene of the Los Angeles Basin, California»
 . Journal of Paleontology (em inglês). 82 (5): 996–1008. Bibcode:2008JPal...82..996C. ISSN 0022-3360. doi:10.1666/07-113.1
. Journal of Paleontology (em inglês). 82 (5): 996–1008. Bibcode:2008JPal...82..996C. ISSN 0022-3360. doi:10.1666/07-113.1
- ↑ Carnevale, Giorgio; Pietsch, Theodore W. (12 de junho de 2009). «The deep-sea anglerfish genus Acentrophryne (Teleostei, Ceratioidei, Linophrynidae) in the Miocene of California»
 . Journal of Vertebrate Paleontology. 29 (2): 372–378. Bibcode:2009JVPal..29..372C. ISSN 0272-4634. doi:10.1671/039.029.0232
. Journal of Vertebrate Paleontology. 29 (2): 372–378. Bibcode:2009JVPal..29..372C. ISSN 0272-4634. doi:10.1671/039.029.0232
- ↑ Nazarkin, Mikhail V.; Pietsch, Theodore W. (2020). «A fossil dreamer of the genus Oneirodes (Lophiiformes: Ceratioidei) from the Miocene of Sakhalin Island, Russia»
 . Geological Magazine (em inglês). 157 (8): 1378–1382. Bibcode:2020GeoM..157.1378N. ISSN 0016-7568. doi:10.1017/S0016756820000588
. Geological Magazine (em inglês). 157 (8): 1378–1382. Bibcode:2020GeoM..157.1378N. ISSN 0016-7568. doi:10.1017/S0016756820000588
- ↑ «16.4: Parasitism». bio.libretexts.org. LibreTexts Biology. Consultado em 24 de março de 2025
- ↑ «Animal Sex: How Anglerfish Do It». www.livescience.com. LiveScience. 6 de janeiro de 2015. Consultado em 6 de março de 2025
- ↑ «Small tale: Parasitic anglerfish takes size prize, prof says». www.washington.edu. University of Washington. Consultado em 6 de março de 2025
- ↑ Theodore W. Pietsch (julho 1975). «Precocious sexual parasitism in the deep sea ceratioid anglerfish, Cryptopsaras couesi Gill». Nature. 256 (5512): 38–40. Bibcode:1975Natur.256...38P. doi:10.1038/256038a0
- ↑ Regan, CT (1926). «The pediculate fishes of the suborder Ceratioidea». Dana Oceanogr Rep. 2. 14 páginas
- ↑ Bertelsen, E (1951). «The ceratioid fishes. Ontogeny, taxonomy, distribution and biology.». Dana Rep. 39: 1–276
- ↑ Swann, Jeremy B.; Holland, Stephen J.; Petersen, Malte; Pietsch, Theodore W.; Boehm, Thomas (30 de julho de 2020). «The immunogenetics of sexual parasitism»
 . Science. 369 (6511): 1608–1615. Bibcode:2020Sci...369.1608S. PMID 32732279. doi:10.1126/science.aaz9445. Consultado em 5 de março de 2025
. Science. 369 (6511): 1608–1615. Bibcode:2020Sci...369.1608S. PMID 32732279. doi:10.1126/science.aaz9445. Consultado em 5 de março de 2025
- ↑ Bordon, Yvonne (18 de agosto de 2020). «Loss of immunity lets a sexual parasite hold on tight»
 . Nature Reviews Immunology. 20 (10): 590–591. PMID 32811995. doi:10.1038/s41577-020-00435-5. Consultado em 5 de março de 2025
. Nature Reviews Immunology. 20 (10): 590–591. PMID 32811995. doi:10.1038/s41577-020-00435-5. Consultado em 5 de março de 2025
- ↑ Swann, Jeremy B (30 de julho de 2020). «The immunogenetics of sexual parasitism»
 . Science. 369 (6511): 1608–1615. Bibcode:2020Sci...369.1608S. PMID 32732279. doi:10.1126/science.aaz9445. hdl:21.11116/0000-0006-CE67-F
. Science. 369 (6511): 1608–1615. Bibcode:2020Sci...369.1608S. PMID 32732279. doi:10.1126/science.aaz9445. hdl:21.11116/0000-0006-CE67-F
- ↑ Isakov, Noah (2022). «Histocompatibility and Reproduction: Lessons from the Anglerfish». Life (em inglês). 12 (1). 113 páginas. Bibcode:2022Life...12..113I. ISSN 2075-1729. PMC 8780861
 . PMID 35054506. doi:10.3390/life12010113
. PMID 35054506. doi:10.3390/life12010113
- ↑ Pietsch, Theodore W.; Orr, James (28 de fevereiro de 2007). «Phylogenetic Relationships of Deep-sea Anglerfishes of the Suborder Ceratioidei (Teleostei: Lophiiformes) Based on Morphology». Copeia. 1: 1–34. doi:10.1643/0045-8511(2007)7[1:PRODAO]2.0.CO;2. Consultado em 19 de março de 2025
- Este artigo foi inicialmente traduzido, total ou parcialmente, do artigo da Wikipédia em inglês cujo título é «Ceratioidei», especificamente desta versão.