Carbono inorgânico particulado
_map_2014.png)
Carbono inorgânico particulado (PIC) pode ser contrastado com o carbono inorgânico dissolvido [en] (DIC), a outra forma de carbono inorgânico [en] encontrada no oceano. Essas distinções são fundamentais em oceanografia química. O carbono inorgânico particulado é às vezes chamado de carbono inorgânico suspenso. Em termos operacionais, é definido como o carbono inorgânico em forma particulada que é grande demais para passar pelo filtro usado para separar o carbono inorgânico dissolvido.
A maior parte do PIC é carbonato de cálcio, CaCO3, especialmente na forma de calcita, mas também como aragonita. O carbonato de cálcio compõe as conchas de muitos organismos marinhos. Ele também se forma durante eventos de branqueamento e é excretado por peixes marinhos durante a osmorregulação.
Visão geral
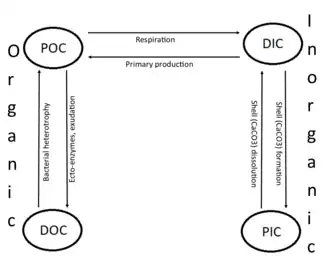
Os compostos de carbono podem ser classificados como orgânicos ou inorgânicos, e dissolvidos ou particulados, dependendo de sua composição. O carbono orgânico forma a base de componentes essenciais de compostos orgânicos, como proteínas, lipídeos, carboidratos e ácidos nucleicos. O carbono inorgânico é encontrado principalmente em compostos simples, como dióxido de carbono, ácido carbônico, bicarbonato e carbonato (CO2, H2CO3, HCO3−, CO32−, respectivamente).
O carbono marinho é ainda separado em uma fase particulada e outra dissolvida. Esses reservatórios são definidos operacionalmente por separação física – o carbono dissolvido passa por um filtro de 0,2 μm, enquanto o carbono particulado fica retido.
Existem dois tipos principais de carbono inorgânico nos oceanos. O carbono inorgânico dissolvido [en] (DIC) é composto por bicarbonato (HCO3−), carbonato (CO32−) e dióxido de carbono (incluindo CO2 dissolvido e ácido carbônico H2CO3). O DIC pode ser convertido em carbono inorgânico particulado (PIC) por meio da precipitação de CaCO3 (biológica ou abiótica). O DIC também pode ser transformado em carbono orgânico particulado (POC) por meio de fotossíntese e quimioautotrofia (ou seja, produção primária). O DIC aumenta com a profundidade à medida que partículas de carbono orgânico afundam e são respiradas. O oxigênio livre diminui à medida que o DIC aumenta, pois o oxigênio é consumido durante a respiração aeróbica.
O carbono inorgânico particulado (PIC) é a outra forma de carbono inorgânico encontrada no oceano. A maior parte do PIC é o CaCO3 que compõe as conchas de vários organismos marinhos, mas também pode se formar em eventos de branqueamento. Peixes marinhos também excretam carbonato de cálcio durante a osmorregulação.[4]

Algumas espécies de carbono inorgânico no oceano, como bicarbonato e carbonato, são grandes contribuintes para a alcalinidade, um tampão natural do oceano que previne mudanças drásticas na acidez (ou pH). O ciclo do carbono marinho também afeta as taxas de reação e dissolução de alguns compostos químicos, regula a quantidade de dióxido de carbono na atmosfera e a temperatura da Terra.[6]
Carbonato de cálcio
O carbono inorgânico particulado (PIC) geralmente assume a forma de carbonato de cálcio (CaCO3) e desempenha um papel fundamental no ciclo do carbono oceânico.[7] Esse carbono fixado biologicamente é usado como revestimento protetor para muitas espécies planctônicas (cocolitóforos, foraminíferos) e organismos marinhos maiores (conchas de moluscos). O carbonato de cálcio também é excretado em altas taxas durante a osmorregulação por peixes e pode se formar em eventos de branqueamento.[8] Embora essa forma de carbono não seja diretamente retirada do orçamento atmosférico, ela é formada a partir de formas dissolvidas de carbonato que estão em equilíbrio com o CO2 e, posteriormente, responsáveis pela remoção desse carbono por meio de sequestro.[9]
- CO2 + H2O → H2CO3 → H+ + HCO3−
- Ca2+ + 2HCO3− → CaCO3 + CO2 + H2O
Embora esse processo consiga fixar uma grande quantidade de carbono, duas unidades de alcalinidade são sequestradas para cada unidade de carbono.[10][11] A formação e o afundamento de CaCO3 geram, portanto, um gradiente de alcalinidade da superfície para o fundo, que eleva o pH das águas superficiais, alterando a especiação do carbono dissolvido para aumentar a pressão parcial de CO2 dissolvido nas águas superficiais, o que, por fim, acaba elevando os níveis atmosféricos. Além disso, o depósito de CaCO3 nos sedimentos reduz a alcalinidade oceânica geral, tendendo a aumentar o pH e, consequentemente, os níveis de CO2 atmosférico, se não for contrabalançado pela nova entrada de alcalinidade por intemperismo.[10] A porção de carbono permanentemente enterrada no fundo do mar torna-se parte do registro geológico. O carbonato de cálcio frequentemente forma depósitos notáveis que podem ser elevados à terra por movimentos tectônicos, como no caso das Falésias Brancas de Dover no sul da Inglaterra. Essas falésias são compostas quase inteiramente por placas de cocolitóforos enterrados.[12]
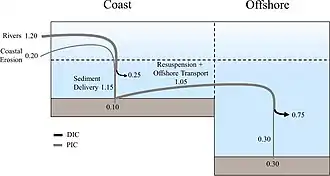
Bomba de carbonato
A bomba de carbonato, às vezes chamada de bomba contrária de carbonato, começa com organismos marinhos na superfície do oceano produzindo carbono inorgânico particulado (PIC) na forma de carbonato de cálcio (calcita ou aragonita, CaCO3). Esse CaCO3 forma partes duras do corpo, como conchas.[6] A formação dessas conchas aumenta o CO2 atmosférico devido à produção de CaCO3[14] na seguinte reação com estequiometria simplificada:[15]
.png)
- Ca2+ + 2HCO3− ⇌ CaCO3 + CO2 + H2O[16]
- Os cocolitóforos, um grupo quase ubíquo de fitoplâncton que produz conchas de carbonato de cálcio, são os principais contribuintes para a bomba de carbonato.[6] Devido à sua abundância, os cocolitóforos têm implicações significativas na química do carbonato, nas águas superficiais que habitam e no oceano abaixo: eles fornecem um importante mecanismo para o transporte descendente de CaCO3.[17] O fluxo de CO2 entre o ar e o mar induzido por uma comunidade biológica marinha pode ser determinado pela proporção de afundamento – a proporção de carbono de carbonato de cálcio em comparação com o carbono orgânico em material particulado que afunda para o fundo do oceano (PIC/POC).[16] A bomba de carbonato atua como uma retroalimentação negativa no CO2 absorvido pelo oceano pela bomba de solubilidade. Ela ocorre com menor magnitude do que a bomba de solubilidade.
A bomba de carbonato é às vezes referida como o componente de "tecido duro" da bomba biológica.[10] Alguns organismos marinhos de superfície, como cocolitóforos, produzem estruturas duras de carbonato de cálcio, uma forma de carbono inorgânico particulado, fixando bicarbonato.[18] Essa fixação de DIC é uma parte importante do ciclo do carbono oceânico.
- Ca2+ + 2 HCO3− → CaCO3 + CO2 + H2O
Enquanto a bomba de carbono biológica fixa carbono inorgânico (CO2) em carbono orgânico particulado [en] na forma de açúcar (C6H12O6), a bomba de carbonato fixa bicarbonato inorgânico e causa uma liberação líquida de CO2.[18] Dessa forma, a bomba de carbonato pode ser chamada de bomba contrária de carbonato. Ela trabalha contra a bomba biológica, contrabalançando o seu fluxo de CO2.[14]
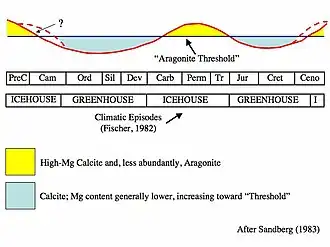
Mares de calcita e aragonita
Um mar de aragonita [en] contém aragonita e calcita com alto teor de magnésio como os principais precipitados de carbonato de cálcio inorgânico. As condições químicas da água do mar devem ter um teor de magnésio notavelmente alto em relação ao cálcio (alta razão Mg/Ca) para que um mar de aragonita se forme. Isso contrasta com um mar de calcita [en], no qual a água do mar com baixo teor de magnésio em relação ao cálcio (baixa razão Mg/Ca) favorece a formação de calcita com baixo teor de magnésio como o principal precipitado de carbonato de cálcio inorgânico marinho.
Os oceanos do início do Paleozoico e do meio ao final do Mesozoico eram predominantemente mares de calcita, enquanto os períodos do meio do Paleozoico ao início do Mesozoico e o Cenozoico (incluindo hoje) são caracterizados por mares de aragonita.[19][20][21][22][23][24][25][26]
Mares de aragonita ocorrem devido a vários fatores, sendo o mais óbvio uma alta razão Mg/Ca na água do mar (Mg/Ca > 2), que ocorre durante intervalos de baixa expansão do fundo oceânico.[22] No entanto, o nível do mar, a temperatura e o estado de saturação de carbonato de cálcio do sistema circundante também determinam qual polimorfo de carbonato de cálcio (aragonita, calcita com baixo teor de magnésio, calcita com alto teor de magnésio) será formado.[27][28]
Da mesma forma, a ocorrência de mares de calcita é controlada pelo mesmo conjunto de fatores que controlam os mares de aragonita, sendo o mais óbvio uma baixa razão Mg/Ca na água do mar (Mg/Ca < 2), que ocorre durante intervalos de rápida expansão do fundo oceânico.[22][26]
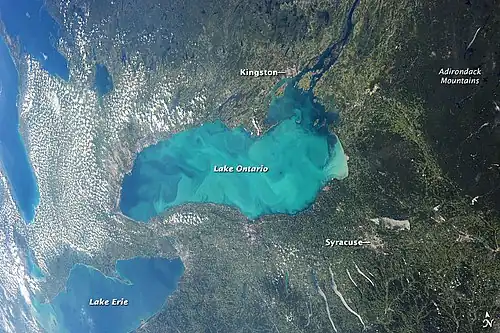
Eventos de branqueamento
Um evento de branqueamento é um fenômeno que ocorre quando uma nuvem suspensa de carbonato de cálcio em grãos finos precipita em corpos d'água, geralmente durante os meses de verão, como resultado da atividade microbiológica fotossintética ou perturbação do sedimento.[29][30][31] O fenômeno recebe seu nome pela cor branca e calcária que confere à água. Esses eventos ocorrem em águas temperadas e tropicais e podem se estender por centenas de metros.[31] Eles também podem ocorrer em ambientes marinhos e de água doce.[32] A origem dos eventos de branqueamento é debatida na comunidade científica, e não está claro se há uma causa única e específica. Geralmente, acredita-se que resultem da ressuspensão de sedimentos do fundo ou do aumento da atividade de certos microrganismos, como o fitoplâncton.[29][33][34] Como os eventos de branqueamento afetam a química aquática, as propriedades físicas e o ciclo do carbono, estudar os mecanismos por trás deles tem relevância científica em várias maneiras.[30][35][36][37][38]
Cinturão de Calcita do Sul
O Grande Cinturão de Calcita [en] (GCB) do Oceano Antártico é uma região com elevada concentração de calcita no oceano superior durante o verão, derivada de cocolitóforos, apesar da região ser conhecida pela predominância de diatomáceas. A sobreposição de dois grandes grupos de fitoplâncton, cocolitóforos e diatomáceas, nos sistemas frontais dinâmicos característicos dessa região fornece um ambiente ideal para estudar as influências ambientais na distribuição de diferentes espécies dentro desses grupos taxonômicos.[39]
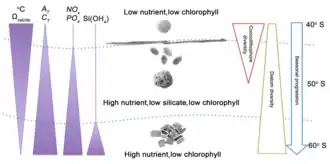
O Grande Cinturão de Calcita, definido como uma ocorrência de carbono inorgânico particulado (PIC) elevado que coincide com clorofila a sazonalmente elevada na primavera e no verão austral no Oceano Antártico,[40] desempenha um papel importante nas flutuações climáticas,[41][42] representando mais de 60% da área do Oceano Antártico (30–60° S).[43] A região entre 30° e 50° S tem a maior absorção de dióxido de carbono antropogênico (CO2) ao lado dos oceanos Atlântico Norte e Pacífico Norte.[44] O conhecimento sobre o impacto das influências ambientais interativas na distribuição de fitoplâncton no Oceano Antártico é limitado. Por exemplo, é necessário mais entendimento sobre como a disponibilidade de luz e ferro ou temperatura e pH interagem para controlar a biogeografia do fitoplâncton.[45][46][47] Portanto, se as parametrizações de modelos forem aprimoradas para fornecer previsões precisas de mudanças biogeoquímicas, é necessário um entendimento multivariado do conjunto completo de fatores ambientais.[39][48]

O Oceano Antártico tem sido frequentemente considerado como um sistema dominado por microplâncton (20–200 μm), com floração de fitoplâncton dominada por grandes diatomáceas e Phaeocystis [en] sp.[49][50][51] No entanto, desde a identificação do cinturão como um evento consistente[40][52] e o reconhecimento da importância do picoplâncton (< 2 μm) e nanoplâncton (2–20 μm) em águas de regiões de muitos nutrientes e baixa clorofila (ANBC),[53] a dinâmica de pequenos plânctons (bio)mineralizantes e sua produção precisam ser reconhecidas. Os dois grupos dominantes de fitoplâncton biomineralizantes no cinturão são cocolitóforos e diatomáceas. Cocolitóforos são geralmente encontrados ao norte da frente polar,[54] embora Emiliania huxleyi tenha sido observada tão ao sul quanto 58° S no Mar de Scotia,[55] a 61° S através da Passagem de Drake,[47] e a 65° S ao sul da Austrália.[39][56]
As diatomáceas estão presentes em todo o cinturão de calcita, com a frente polar marcando uma forte divisão entre diferentes frações de tamanho.[57] Ao norte da frente polar, espécies pequenas de diatomáceas, como Pseudo-nitzschia [en] spp. e Thalassiosira [en] spp., tendem a dominar numericamente, enquanto grandes diatomáceas com maiores demandas de ácido silícico (por exemplo, Fragilariopsis kerguelensis [en]) são geralmente mais abundantes ao sul do círculo polar.[57] Altas abundâncias de nanoplâncton (cocolitóforos, pequenas diatomáceas, crisófitas) também foram observadas na Plataforma Patagônica [en][50] e no Mar de Scotia.[58] Atualmente, poucos estudos incorporam pequenos fitoplânctons biomineralizantes ao nível de espécie.[49][50][57][58] Em vez disso, o foco tem sido frequentemente nas espécies maiores e não calcificantes no Oceano Antártico devido a problemas de preservação de amostras (ou seja, a solução de Lugol acidificada dissolve calcita, e a microscopia óptica restringe a identificação precisa a células maiores de 10 μm).[58] No contexto das mudanças climáticas e o funcionamento futuro do ecossistema, é importante conhecer a distribuição de fitoplâncton biomineralizante ao considerar as interações do fitoplâncton com a química do carbonato[59][60] e a biogeoquímica oceânica [en].[39][61][62][63]

com diferentes morfologias
B) e D) Partículas semelhantes aos carbonatos de Ca descritos como precipitados na superfície celular de bactérias marinhas [en] cultivadas.
E) e F) Partículas com uma superfície plana, sugerindo que são formadas em uma superfície ou interface.
G e H) Partículas com forma romboédrica.
I) e J) Partículas em forma de bastão semelhantes aos oóides das Bahamas.[64]
O Cinturão de Calcita abrange as principais fronteiras circumpolares do Oceano Antártico: a fronteira subantártica, a fronteira polar, a fronteira da Corrente Circumpolar Antártica do Sul e, ocasionalmente, o limite sul da Corrente Circumpolar Antártica.[65][66][67] A frente subtropical (a aproximadamente 10 °C) atua como o limite norte do cinturão e está associada a um forte aumento no PIC em direção ao sul.[43] Essas fronteiras dividem zonas ambientais e biogeoquímicas distintas, tornando o cinturão uma área de estudo ideal para examinar os fatores que influenciam as comunidades de fitoplâncton em mar aberto.[45][51] Uma alta concentração de PIC observada no cinturão (1 μmol PIC L−1) em comparação com a média global (0,2 μmol PIC L−1) e quantidades significativas de cocolitos destacados de E. huxleyi (em concentrações > 20 000 cocolitos mL−1)[43] marcam o cinturão. Ele é claramente observado em imagens de satélite[40] que se estendem desde a Plataforma Patagônica [en][68][69] através dos oceanos Atlântico, Índico e Pacífico, completando a circunavegação antártica via Passagem de Drake.[39]
Cocolitóforos

Desde a revolução industrial, 30% do CO2 antropogênico foi absorvido pelos oceanos,[70] resultando em acidificação oceânica,[71] que é uma ameaça às algas calcificantes.[72][73] Como resultado, houve um grande interesse nessas algas calcificantes, impulsionado pelo seu papel principal no ciclo global do carbono.[74][75][76][77][78] Globalmente, os cocolitóforos, particularmente Emiliania huxleyi, são considerados as algas calcificantes mais prevalentes, cujas eflorescências podem até ser vistas do espaço.[79] As algas calcificantes [en] criam um exoesqueleto a partir de placas de carbonato de cálcio (cocolitos [en]), fornecendo lastro que aumenta o fluxo de carbono orgânico e inorgânico para o fundo do mar.[74][80] O carbono orgânico é formado pela fotossíntese, onde o CO2 é fixado e convertido em moléculas orgânicas, causando a remoção de CO2 da água do mar. Ao contrário, a produção de cocolitos leva à liberação de CO2 na água do mar, devido à remoção de carbonato da água do mar, o que reduz a alcalinidade e causa acidificação oceânica.[81] Portanto, a razão entre carbono inorgânico particulado (PIC) e carbono orgânico particulado [en] (POC) é uma medida importante para determinar a liberação ou absorção líquida de CO2. Em resumo, a razão PIC/POC é uma característica chave necessária para entender e prever o impacto das mudanças climáticas no ciclo global do carbono nos oceanos.[71][76][78][82][83][84][85]
Referências
- ↑ «Particulate Inorganic Carbon (PIC)». NASA Ocean Color (em inglês). Consultado em 2 de outubro de 2025. Arquivado do original em 30 de janeiro de 2023
- ↑ Balch, W. M.; Gordon, Howard R.; Bowler, B. C.; Drapeau, D. T.; Booth, E. S. (julho de 2005). «Calcium carbonate measurements in the surface global ocean based on Moderate‐Resolution Imaging Spectroradiometer data». Journal of Geophysical Research: Oceans (em inglês). 110 (C7). ISSN 0148-0227. doi:10.1029/2004JC002560. Consultado em 2 de outubro de 2025
- ↑ Gordon, Howard R.; Boynton, G. Chris; Balch, William M.; Groom, Stephen B.; Harbour, Derek S.; Smyth, Tim J. (15 de abril de 2001). «Retrieval of coccolithophore calcite concentration from SeaWiFS Imagery». Geophysical Research Letters (em inglês). 28 (8): 1587–1590. ISSN 0094-8276. doi:10.1029/2000GL012025. Consultado em 2 de outubro de 2025
- ↑ Wilson, R. W.; Millero, F. J.; Taylor, J. R.; Walsh, P. J.; Christensen, V.; Jennings, S.; Grosell, M. (16 de janeiro de 2009). «Contribution of Fish to the Marine Inorganic Carbon Cycle». Science (em inglês). 323 (5912): 359–362. ISSN 0036-8075. doi:10.1126/science.1157972. Consultado em 2 de outubro de 2025
- ↑ Davies, Emlyn J.; Basedow, Sünnje L.; McKee, David (17 de fevereiro de 2021). «The hidden influence of large particles on ocean colour». Scientific Reports (em inglês). 11 (1). ISSN 2045-2322. PMC 7889869
 . PMID 33597642. doi:10.1038/s41598-021-83610-5. Consultado em 2 de outubro de 2025
. PMID 33597642. doi:10.1038/s41598-021-83610-5. Consultado em 2 de outubro de 2025
- ↑ a b c Emerson, Steven; Hedges, John (2008). Chemical oceanography and the marine carbon cycle (em inglês). Cambridge: Cambridge University Press. ISBN 978-0-521-83313-4
- ↑ Mitchell, C.; Hu, C.; Bowler, B.; Drapeau, D.; Balch, W. M. (novembro de 2017). «Estimating Particulate Inorganic Carbon Concentrations of the Global Ocean From Ocean Color Measurements Using a Reflectance Difference Approach». Journal of Geophysical Research: Oceans (em inglês). 122 (11): 8707–8720. ISSN 2169-9275. doi:10.1002/2017JC013146. Consultado em 2 de outubro de 2025
- ↑ Wilson, R. W.; Millero, F. J.; Taylor, J. R.; Walsh, P. J.; Christensen, V.; Jennings, S.; Grosell, M. (16 de janeiro de 2009). «Contribution of Fish to the Marine Inorganic Carbon Cycle». Science (em inglês). 323 (5912): 359–362. ISSN 0036-8075. doi:10.1126/science.1157972. Consultado em 2 de outubro de 2025
- ↑ Pilson, Michael E. Q. (2013). An introduction to the chemistry of the sea (em inglês) 2 ed. Cambridge: Cambridge university press. ISBN 978-0521887076
- ↑ a b c Hain, M.P.; Sigman, D.M.; Haug, G.H. (2014). «The Biological Pump in the Past». Elsevier. Treatise on Geochemistry (Second Edition) (em inglês). 8: 485–517. ISBN 978-0-08-098300-4. doi:10.1016/b978-0-08-095975-7.00618-5. Consultado em 2 de outubro de 2025
- ↑ Hain, Mathis P.; Sigman, Daniel M.; Haug, Gerald H. (dezembro de 2010). «Carbon dioxide effects of Antarctic stratification, North Atlantic Intermediate Water formation, and subantarctic nutrient drawdown during the last ice age: Diagnosis and synthesis in a geochemical box model». Global Biogeochemical Cycles (em inglês). 24 (4). ISSN 0886-6236. doi:10.1029/2010GB003790. Consultado em 2 de outubro de 2025
- ↑ Webb, Paul (2019). «Chapter 12: Ocean Sediments». Introduction to Oceanography (em inglês). [S.l.: s.n.]
- ↑ Capelle, David W.; Kuzyk, Zou Zou A.; Papakyriakou, Tim; Guéguen, Céline; Miller, Lisa A.; Macdonald, Robie W. (junho de 2020). «Effect of terrestrial organic matter on ocean acidification and CO2 flux in an Arctic shelf sea». Progress in Oceanography (em inglês). 185. 102319 páginas. doi:10.1016/j.pocean.2020.102319. Consultado em 2 de outubro de 2025
- ↑ a b Zeebe, Richard E. (fevereiro de 2016). «The calcium carbonate counter pump: Fundamentals, evolution through time, and future feedbacks». American Geophysical Union, Ocean Sciences Meeting (em inglês): B23A–08. Consultado em 2 de outubro de 2025
- ↑ Smith, Stephen V. (2013). Parsing the Oceanic Calcium Carbonate Cycle: A Net Atmospheric Carbon Dioxide Source, or a Sink? (em inglês). [S.l.]: ASLO. ISBN 978-0-9845591-2-1. Consultado em 2 de outubro de 2025. Arquivado do original em 7 de dezembro de 2017
- ↑ a b Smith, S. V.; Key, G. S. (maio de 1975). «Carbon dioxide and metabolism in marine environments1». Limnology and Oceanography (em inglês). 20 (3): 493–495. ISSN 0024-3590. doi:10.4319/lo.1975.20.3.0493. Consultado em 2 de outubro de 2025
- ↑ Rost, Björn; Riebesell, Ulf (2004). Thierstein, Hans R.; Young, Jeremy R., eds. «Coccolithophores and the biological pump: responses to environmental changes». Berlin, Heidelberg: Springer Berlin Heidelberg (em inglês): 99–125. ISBN 978-3-642-06016-8. doi:10.1007/978-3-662-06278-4_5. Consultado em 2 de outubro de 2025
- ↑ a b Thierstein, Hans R.; Young, Jeremy R., eds. (2004). Coccolithophores: from molecular processes to global impact (em inglês). Berlin; New York: Springer. ISBN 978-3-642-06016-8
- ↑ Bruce H. Wilkinson, Robert M. Owen, (1985). «Submarine Hydrothermal Weathering, Global Eustasy, and Carbonate Polymorphism in Phanerozoic Marine Oolites». SEPM Journal of Sedimentary Research (em inglês). 55. ISSN 1527-1404. doi:10.1306/212F8657-2B24-11D7-8648000102C1865D. Consultado em 2 de outubro de 2025
- ↑ Wilkinson, Bruce H.; Given, R. Kevin (maio de 1986). «Secular Variation in Abiotic Marine Carbonates: Constraints on Phanerozoic Atmospheric Carbon Dioxide Contents and Oceanic Mg/Ca Ratios». The Journal of Geology (em inglês). 94 (3): 321–333. ISSN 0022-1376. doi:10.1086/629032. Consultado em 2 de outubro de 2025
- ↑ «Chapter 1 The CO2-Carbonic Acid System and Solution Chemistry». Elsevier. Developments in Sedimentology (em inglês). 48: 1–38. 1990. ISBN 978-0-444-87391-0. doi:10.1016/s0070-4571(08)70330-3. Consultado em 2 de outubro de 2025
- ↑ a b c Hardie, Lawrence A. (1996). «Secular variation in seawater chemistry: An explanation for the coupled secular variation in the mineralogies of marine limestones and potash evaporites over the past 600 m.y.». Geology (em inglês). 24 (3). 279 páginas. ISSN 0091-7613. doi:10.1130/0091-7613(1996)024<0279:SVISCA>2.3.CO;2. Consultado em 2 de outubro de 2025
- ↑ Lowenstein, Tim K.; Timofeeff, Michael N.; Brennan, Sean T.; Hardie, Lawrence A.; Demicco, Robert V. (2 de novembro de 2001). «Oscillations in Phanerozoic Seawater Chemistry: Evidence from Fluid Inclusions». Science (em inglês). 294 (5544): 1086–1088. ISSN 0036-8075. doi:10.1126/science.1064280. Consultado em 2 de outubro de 2025
- ↑ Hardie, Lawrence A. (2003). «Secular variations in Precambrian seawater chemistry and the timing of Precambrian aragonite seas and calcite seas». Geology (em inglês). 31 (9). 785 páginas. ISSN 0091-7613. doi:10.1130/G19657.1. Consultado em 2 de outubro de 2025
- ↑ Palmer, Timothy J.; Wilson, Mark A. (dezembro de 2004). «Calcite precipitation and dissolution of biogenic aragonite in shallow Ordovician calcite seas». Lethaia (em inglês). 37 (4): 417–427. ISSN 0024-1164. doi:10.1080/00241160410002135. Consultado em 2 de outubro de 2025
- ↑ a b Ries, J. B. (21 de setembro de 2010). «Review: geological and experimental evidence for secular variation in seawater Mg/Ca (calcite-aragonite seas) and its effects on marine biological calcification». Biogeosciences (em inglês). 7 (9): 2795–2849. ISSN 1726-4189. doi:10.5194/bg-7-2795-2010. Consultado em 2 de outubro de 2025
- ↑ Adabi, Mohammad H. (setembro de 2004). «A re-evaluation of aragonite versus calcite seas». Carbonates and Evaporites (em inglês). 19 (2): 133–141. ISSN 0891-2556. doi:10.1007/BF03178476. Consultado em 2 de outubro de 2025
- ↑ Ries, Justin B. (julho de 2011). «Skeletal mineralogy in a high-CO2 world». Journal of Experimental Marine Biology and Ecology (em inglês). 403 (1-2): 54–64. doi:10.1016/j.jembe.2011.04.006. Consultado em 2 de outubro de 2025
- ↑ a b «Whiting Event, Lake Ontario». NASA Earth Observatory (em inglês). 2 de setembro de 2013. Consultado em 2 de outubro de 2025
- ↑ a b Larson, Erik B.; Mylroie, John E. (dezembro de 2014). «A review of whiting formation in the Bahamas and new models». Carbonates and Evaporites (em inglês). 29 (4): 337–347. ISSN 0891-2556. doi:10.1007/s13146-014-0212-7. Consultado em 2 de outubro de 2025
- ↑ a b Sondi, Ivan; Juračić, Mladen (janeiro de 2010). «Whiting events and the formation of aragonite in Mediterranean Karstic Marine Lakes: new evidence on its biologically induced inorganic origin». Sedimentology (em inglês). 57 (1): 85–95. doi:10.1111/j.1365-3091.2009.01090.x. Consultado em 2 de outubro de 2025
- ↑ Long, Jacqueline S.; Hu, Chuanmin; Robbins, Lisa L.; Byrne, Robert H.; Paul, John H.; Wolny, Jennifer L. (setembro de 2017). «Optical and biochemical properties of a southwest Florida whiting event». Estuarine, Coastal and Shelf Science (em inglês). 196: 258–268. doi:10.1016/j.ecss.2017.07.017. Consultado em 2 de outubro de 2025
- ↑ Schultze-Lam, Susanne; Schultze-Lam, Susanne; Beveridge, Terrance J.; Des Marais, David J. (janeiro de 1997). «Whiting events: Biogenic origin due to the photosynthetic activity of cyanobacterial picoplankton». Limnology and Oceanography (em inglês). 42 (1): 133–141. ISSN 0024-3590. doi:10.4319/lo.1997.42.1.0133. Consultado em 2 de outubro de 2025
- ↑ «Whiting in Lake Michigan». NASA Earth Observatory (em inglês). 18 de setembro de 2001. Consultado em 2 de outubro de 2025
- ↑ Dittrich, Maria; Obst, Martin (dezembro de 2004). «Are Picoplankton Responsible for Calcite Precipitation in Lakes?». AMBIO: A Journal of the Human Environment (em inglês). 33 (8): 559–564. ISSN 0044-7447. doi:10.1579/0044-7447-33.8.559. Consultado em 2 de outubro de 2025
- ↑ Shinn, Eugene A.; Kendall, Christopher G. St. C. (31 de dezembro de 2011). Day-Stirrat, Ruarri; Janson, Xavier; Wright, Wayne, eds. «Back to the Future». The Sedimentary Record. 9 (4): 4–9. doi:10.2110/sedred.2011.4.4. Consultado em 2 de outubro de 2025
- ↑ Yates, K. K.; Robbins, L. L. (2001). «Chapter 14 - Microbial Lime-Mud Production and Its Relation to Climate Change». AAPG Studies in Geology: Geological Perspectives of Global Climate Change (em inglês). 47: 266–283. Consultado em 2 de outubro de 2025
- ↑ Effler, Steven W.; Perkins, Mary Gail; Greer, Harry; Johnson, David L. (abril de 1987). «EFFECT OF "WHITING" ON OPTICAL PROPERTIES AND TURBIDITY IN OWASCO LAKE, NEW YORK 1». JAWRA Journal of the American Water Resources Association (em inglês). 23 (2): 189–196. ISSN 1093-474X. doi:10.1111/j.1752-1688.1987.tb00796.x. Consultado em 2 de outubro de 2025
- ↑ a b c d e f g Smith, Helen E. K.; Poulton, Alex J.; Garley, Rebecca; Hopkins, Jason; Lubelczyk, Laura C.; Drapeau, Dave T.; Rauschenberg, Sara; Twining, Ben S.; Bates, Nicholas R. (7 de novembro de 2017). «The influence of environmental variability on the biogeography of coccolithophores and diatoms in the Great Calcite Belt». Biogeosciences (em inglês). 14 (21): 4905–4925. ISSN 1726-4189. doi:10.5194/bg-14-4905-2017. Consultado em 2 de outubro de 2025
- ↑ a b c Balch, W. M.; Gordon, Howard R.; Bowler, B. C.; Drapeau, D. T.; Booth, E. S. (julho de 2005). «Calcium carbonate measurements in the surface global ocean based on Moderate‐Resolution Imaging Spectroradiometer data». Journal of Geophysical Research: Oceans (em inglês). 110 (C7). ISSN 0148-0227. doi:10.1029/2004JC002560. Consultado em 2 de outubro de 2025
- ↑ Sarmiento, Jorge L.; Hughes, Tertia M. C.; Stouffer, Ronald J.; Manabe, Syukuro (maio de 1998). «Simulated response of the ocean carbon cycle to anthropogenic climate warming». Nature (em inglês). 393 (6682): 245–249. ISSN 0028-0836. doi:10.1038/30455. Consultado em 2 de outubro de 2025
- ↑ Sarmiento, J. L.; Slater, R.; Barber, R.; Bopp, L.; Doney, S. C.; Hirst, A. C.; Kleypas, J.; Matear, R.; Mikolajewicz, U. (setembro de 2004). «Response of ocean ecosystems to climate warming». Global Biogeochemical Cycles (em inglês). 18 (3). ISSN 0886-6236. doi:10.1029/2003GB002134. Consultado em 2 de outubro de 2025
- ↑ a b c Balch, W. M.; Drapeau, D. T.; Bowler, B. C.; Lyczskowski, E.; Booth, E. S.; Alley, D. (4 de agosto de 2011). «The contribution of coccolithophores to the optical and inorganic carbon budgets during the Southern Ocean Gas Exchange Experiment: New evidence in support of the "Great Calcite Belt" hypothesis». Journal of Geophysical Research (em inglês). 116. ISSN 0148-0227. doi:10.1029/2011JC006941. Consultado em 2 de outubro de 2025
- ↑ Sabine, Christopher L.; Feely, Richard A.; Gruber, Nicolas; Key, Robert M.; Lee, Kitack; Bullister, John L.; Wanninkhof, Rik; Wong, C. S.; Wallace, Douglas W. R. (16 de julho de 2004). «The Oceanic Sink for Anthropogenic CO 2». Science (em inglês). 305 (5682): 367–371. ISSN 0036-8075. doi:10.1126/science.1097403. Consultado em 2 de outubro de 2025
- ↑ a b Boyd, Philip W.; Strzepek, Robert; Fu, Feixue; Hutchins, David A. (maio de 2010). «Environmental control of open‐ocean phytoplankton groups: Now and in the future». Limnology and Oceanography (em inglês). 55 (3): 1353–1376. ISSN 0024-3590. doi:10.4319/lo.2010.55.3.1353. Consultado em 2 de outubro de 2025
- ↑ Boyd, P. W.; Arrigo, K. R.; Strzepek, R.; van Dijken, G. L. (junho de 2012). «Mapping phytoplankton iron utilization: Insights into Southern Ocean supply mechanisms». Journal of Geophysical Research: Oceans (em inglês). 117 (C6). ISSN 0148-0227. doi:10.1029/2011JC007726. Consultado em 2 de outubro de 2025
- ↑ a b Charalampopoulou, Anastasia; Poulton, Alex J.; Bakker, Dorothee C. E.; Lucas, Mike I.; Stinchcombe, Mark C.; Tyrrell, Toby (1 de novembro de 2016). «Environmental drivers of coccolithophore abundance and calcification across Drake Passage (Southern Ocean)». Biogeosciences (em inglês). 13 (21): 5917–5935. ISSN 1726-4189. doi:10.5194/bg-13-5917-2016. Consultado em 2 de outubro de 2025
- ↑ Boyd, P.W.; Newton, P.P. (janeiro de 1999). «Does planktonic community structure determine downward particulate organic carbon flux in different oceanic provinces?». Deep Sea Research Part I: Oceanographic Research Papers (em inglês). 46 (1): 63–91. doi:10.1016/S0967-0637(98)00066-1. Consultado em 2 de outubro de 2025
- ↑ a b Bathmann, U.V.; Scharek, R.; Klaas, C.; Dubischar, C.D.; Smetacek, V. (janeiro de 1997). «Spring development of phytoplankton biomass and composition in major water masses of the Atlantic sector of the Southern Ocean». Deep Sea Research Part II: Topical Studies in Oceanography (em inglês). 44 (1-2): 51–67. doi:10.1016/S0967-0645(96)00063-X. Consultado em 2 de outubro de 2025
- ↑ a b c Poulton, Alex J.; Mark Moore, C.; Seeyave, Sophie; Lucas, Mike I.; Fielding, Sophie; Ward, Peter (setembro de 2007). «Phytoplankton community composition around the Crozet Plateau, with emphasis on diatoms and Phaeocystis». Deep Sea Research Part II: Topical Studies in Oceanography (em inglês). 54 (18-20): 2085–2105. doi:10.1016/j.dsr2.2007.06.005. Consultado em 2 de outubro de 2025
- ↑ a b Boyd, Philip W. (outubro de 2002). «ENVIRONMENTAL FACTORS CONTROLLING PHYTOPLANKTON PROCESSES IN THE SOUTHERN OCEAN 1». Journal of Phycology (em inglês). 38 (5): 844–861. ISSN 0022-3646. doi:10.1046/j.1529-8817.2002.t01-1-01203.x. Consultado em 2 de outubro de 2025
- ↑ Balch, William M.; Bates, Nicholas R.; Lam, Phoebe J.; Twining, Benjamin S.; Rosengard, Sarah Z.; Bowler, Bruce C.; Drapeau, Dave T.; Garley, Rebecca; Lubelczyk, Laura C. (agosto de 2016). «Factors regulating the Great Calcite Belt in the Southern Ocean and its biogeochemical significance». Global Biogeochemical Cycles (em inglês). 30 (8): 1124–1144. ISSN 0886-6236. doi:10.1002/2016GB005414. Consultado em 2 de outubro de 2025
- ↑ Barber, R. T.; Hiscock, M. R. (dezembro de 2006). «A rising tide lifts all phytoplankton: Growth response of other phytoplankton taxa in diatom‐dominated blooms». Global Biogeochemical Cycles (em inglês). 20 (4). ISSN 0886-6236. doi:10.1029/2006GB002726. Consultado em 2 de outubro de 2025
- ↑ Mohan, Rahul; Mergulhao, Lina P.; Guptha, M.V.S.; Rajakumar, A.; Thamban, M.; AnilKumar, N.; Sudhakar, M.; Ravindra, Rasik (abril de 2008). «Ecology of coccolithophores in the Indian sector of the Southern Ocean». Marine Micropaleontology (em inglês). 67 (1-2): 30–45. doi:10.1016/j.marmicro.2007.08.005. Consultado em 2 de outubro de 2025
- ↑ Holligan, P.M.; Charalampopoulou, A.; Hutson, R. (setembro de 2010). «Seasonal distributions of the coccolithophore, Emiliania huxleyi, and of particulate inorganic carbon in surface waters of the Scotia Sea». Journal of Marine Systems (em inglês). 82 (4): 195–205. doi:10.1016/j.jmarsys.2010.05.007. Consultado em 2 de outubro de 2025
- ↑ Cubillos, Jc; Wright, Sw; Nash, G; de Salas, Mf; Griffiths, B; Tilbrook, B; Poisson, A; Hallegraeff, Gm (25 de outubro de 2007). «Calcification morphotypes of the coccolithophorid Emiliania huxleyi in the Southern Ocean: changes in 2001 to 2006 compared to historical data». Marine Ecology Progress Series (em inglês). 348: 47–54. ISSN 0171-8630. doi:10.3354/meps07058. Consultado em 2 de outubro de 2025
- ↑ a b c Froneman, P.W.; McQuaid, C.D.; Perissinotto, R. (1995). «Biogeographic structure of the microphytoplankton assemblages of the south Atlantic and Southern Ocean during austral summer». Journal of Plankton Research (em inglês). 17 (9): 1791–1802. ISSN 0142-7873. doi:10.1093/plankt/17.9.1791. Consultado em 2 de outubro de 2025
- ↑ a b c Hinz, D.J.; Poulton, A.J.; Nielsdóttir, M.C.; Steigenberger, S.; Korb, R.E.; Achterberg, E.P.; Bibby, T.S. (janeiro de 2012). «Comparative seasonal biogeography of mineralising nannoplankton in the Scotia Sea: Emiliania huxleyi, Fragilariopsis spp. and Tetraparma pelagica». Deep Sea Research Part II: Topical Studies in Oceanography (em inglês): 57–66. doi:10.1016/j.dsr2.2011.09.002. Consultado em 3 de outubro de 2025
- ↑ Langer, Gerald; Geisen, Markus; Baumann, Karl‐Heinz; Kläs, Jessica; Riebesell, Ulf; Thoms, Silke; Young, Jeremy R. (setembro de 2006). «Species‐specific responses of calcifying algae to changing seawater carbonate chemistry». Geochemistry, Geophysics, Geosystems (em inglês). 7 (9). ISSN 1525-2027. doi:10.1029/2005GC001227. Consultado em 3 de outubro de 2025
- ↑ Tortell, Philippe D.; Payne, Christopher D.; Li, Yingyu; Trimborn, Scarlett; Rost, Björn; Smith, Walker O.; Riesselman, Christina; Dunbar, Robert B.; Sedwick, Pete (fevereiro de 2008). «CO 2 sensitivity of Southern Ocean phytoplankton». Geophysical Research Letters (em inglês). 35 (4). ISSN 0094-8276. doi:10.1029/2007GL032583. Consultado em 3 de outubro de 2025
- ↑ Baines, Stephen B.; Twining, Benjamin S.; Brzezinski, Mark A.; Nelson, David M.; Fisher, Nicholas S. (dezembro de 2010). «Causes and biogeochemical implications of regional differences in silicification of marine diatoms». Global Biogeochemical Cycles (em inglês). 24 (4). ISSN 0886-6236. doi:10.1029/2010GB003856. Consultado em 3 de outubro de 2025
- ↑ Assmy, Philipp; Smetacek, Victor; Montresor, Marina; Klaas, Christine; Henjes, Joachim; Strass, Volker H.; Arrieta, Jesús M.; Bathmann, Ulrich; Berg, Gry M. (17 de dezembro de 2013). «Thick-shelled, grazer-protected diatoms decouple ocean carbon and silicon cycles in the iron-limited Antarctic Circumpolar Current». Proceedings of the National Academy of Sciences (em inglês). 110 (51): 20633–20638. ISSN 0027-8424. PMC 3870680
 . PMID 24248337. doi:10.1073/pnas.1309345110. Consultado em 3 de outubro de 2025
. PMID 24248337. doi:10.1073/pnas.1309345110. Consultado em 3 de outubro de 2025
- ↑ Poulton, Alex J.; Painter, Stuart C.; Young, Jeremy R.; Bates, Nicholas R.; Bowler, Bruce; Drapeau, Dave; Lyczsckowski, Emily; Balch, William M. (dezembro de 2013). «The 2008 Emiliania huxleyi bloom along the Patagonian Shelf: Ecology, biogeochemistry, and cellular calcification». Global Biogeochemical Cycles (em inglês). 27 (4): 1023–1033. ISSN 0886-6236. doi:10.1002/2013GB004641. Consultado em 3 de outubro de 2025
- ↑ Heldal, Mikal; Norland, Svein; Erichsen, Egil S.; Thingstad, T. Frede; Bratbak, Gunnar (23 de outubro de 2012). Paranhos, Rodolfo, ed. «An Unaccounted Fraction of Marine Biogenic CaCO3 Particles». PLoS ONE (em inglês). 7 (10): e47887. ISSN 1932-6203. PMC 3479124
 . PMID 23110119. doi:10.1371/journal.pone.0047887. Consultado em 3 de outubro de 2025
. PMID 23110119. doi:10.1371/journal.pone.0047887. Consultado em 3 de outubro de 2025
- ↑ Tsuchiya, Mizuki; Talley, Lynne D.; McCartney, Michael S. (1 de janeiro de 1994). «Water-mass distributions in the western South Atlantic; A section from South Georgia Island (54S) northward across the equator». Journal of Marine Research (em inglês). 52 (1): 55–81. doi:10.1357/0022240943076759. Consultado em 3 de outubro de 2025
- ↑ Orsi, Alejandro H.; Whitworth, Thomas; Nowlin, Worth D. (maio de 1995). «On the meridional extent and fronts of the Antarctic Circumpolar Current». Deep Sea Research Part I: Oceanographic Research Papers (em inglês). 42 (5): 641–673. doi:10.1016/0967-0637(95)00021-W. Consultado em 3 de outubro de 2025
- ↑ Belkin, Igor M.; Gordon, Arnold L. (15 de fevereiro de 1996). «Southern Ocean fronts from the Greenwich meridian to Tasmania». Journal of Geophysical Research: Oceans (em inglês). 101 (C2): 3675–3696. ISSN 0148-0227. doi:10.1029/95JC02750. Consultado em 3 de outubro de 2025
- ↑ Signorini, Sergio R.; Garcia, Virginia M. T.; Piola, Alberto R.; Garcia, Carlos A. E.; Mata, Mauricio M.; McClain, Charles R. (agosto de 2006). «Seasonal and interannual variability of calcite in the vicinity of the Patagonian shelf break (38°S–52°S)». Geophysical Research Letters (em inglês). 33 (16). ISSN 0094-8276. doi:10.1029/2006GL026592. Consultado em 3 de outubro de 2025
- ↑ Painter, Stuart C.; Poulton, Alex J.; Allen, John T.; Pidcock, Rosalind; Balch, William M. (outubro de 2010). «The COPAS'08 expedition to the Patagonian Shelf: Physical and environmental conditions during the 2008 coccolithophore bloom». Continental Shelf Research (em inglês). 30 (18): 1907–1923. doi:10.1016/j.csr.2010.08.013. Consultado em 3 de outubro de 2025
- ↑ Sabine, Christopher L.; Feely, Richard A.; Gruber, Nicolas; Key, Robert M.; Lee, Kitack; Bullister, John L.; Wanninkhof, Rik; Wong, C. S.; Wallace, Douglas W. R. (16 de julho de 2004). «The Oceanic Sink for Anthropogenic CO 2». Science (em inglês). 305 (5682): 367–371. ISSN 0036-8075. doi:10.1126/science.1097403. Consultado em 3 de outubro de 2025
- ↑ a b Feely, Richard A.; Sabine, Christopher L.; Lee, Kitack; Berelson, Will; Kleypas, Joanie; Fabry, Victoria J.; Millero, Frank J. (16 de julho de 2004). «Impact of Anthropogenic CO 2 on the CaCO 3 System in the Oceans». Science (em inglês). 305 (5682): 362–366. ISSN 0036-8075. doi:10.1126/science.1097329. Consultado em 3 de outubro de 2025
- ↑ Meyer, J.; Riebesell, U. (16 de março de 2015). «Reviews and Syntheses: Responses of coccolithophores to ocean acidification: a meta-analysis». Biogeosciences (em inglês). 12 (6): 1671–1682. ISSN 1726-4189. doi:10.5194/bg-12-1671-2015. Consultado em 3 de outubro de 2025
- ↑ Riebesell, Ulf; Zondervan, Ingrid; Rost, Björn; Tortell, Philippe D.; Zeebe, Richard E.; Morel, François M. M. (setembro de 2000). «Reduced calcification of marine plankton in response to increased atmospheric CO2». Nature (em inglês). 407 (6802): 364–367. ISSN 0028-0836. doi:10.1038/35030078. Consultado em 3 de outubro de 2025
- ↑ a b Armstrong, Robert A.; Lee, Cindy; Hedges, John I.; Honjo, Susumu; Wakeham, Stuart G. (janeiro de 2001). «A new, mechanistic model for organic carbon fluxes in the ocean based on the quantitative association of POC with ballast minerals». Deep Sea Research Part II: Topical Studies in Oceanography (em inglês). 49 (1-3): 219–236. doi:10.1016/S0967-0645(01)00101-1. Consultado em 3 de outubro de 2025
- ↑ Bach, Lennart T.; Mackinder, Luke C. M.; Schulz, Kai G.; Wheeler, Glen; Schroeder, Declan C.; Brownlee, Colin; Riebesell, Ulf (julho de 2013). «Dissecting the impact of CO 2 and pH on the mechanisms of photosynthesis and calcification in the coccolithophore Emiliania huxleyi». New Phytologist (em inglês). 199 (1): 121–134. ISSN 0028-646X. doi:10.1111/nph.12225. Consultado em 3 de outubro de 2025
- ↑ a b Gafar, N. A.; Eyre, B. D.; Schulz, K. G. (junho de 2019). «Particulate inorganic to organic carbon production as a predictor for coccolithophorid sensitivity to ongoing ocean acidification». Limnology and Oceanography Letters (em inglês). 4 (3): 62–70. ISSN 2378-2242. doi:10.1002/lol2.10105. Consultado em 3 de outubro de 2025
- ↑ Monteiro, Fanny M.; Bach, Lennart T.; Brownlee, Colin; Bown, Paul; Rickaby, Rosalind E. M.; Poulton, Alex J.; Tyrrell, Toby; Beaufort, Luc; Dutkiewicz, Stephanie (julho de 2016). «Why marine phytoplankton calcify». Science Advances (em inglês). 2 (7). ISSN 2375-2548. PMC 4956192
 . PMID 27453937. doi:10.1126/sciadv.1501822. Consultado em 3 de outubro de 2025
. PMID 27453937. doi:10.1126/sciadv.1501822. Consultado em 3 de outubro de 2025
- ↑ a b Schlüter, Lothar; Lohbeck, Kai T.; Gutowska, Magdalena A.; Gröger, Joachim P.; Riebesell, Ulf; Reusch, Thorsten B. H. (novembro de 2014). «Adaptation of a globally important coccolithophore to ocean warming and acidification». Nature Climate Change (em inglês). 4 (11): 1024–1030. ISSN 1758-678X. doi:10.1038/nclimate2379. Consultado em 3 de outubro de 2025
- ↑ Paasche, E. (novembro de 2001). «A review of the coccolithophorid Emiliania huxleyi (Prymnesiophyceae), with particular reference to growth, coccolith formation, and calcification-photosynthesis interactions». Phycologia (em inglês). 40 (6): 503–529. ISSN 0031-8884. doi:10.2216/i0031-8884-40-6-503.1. Consultado em 3 de outubro de 2025
- ↑ Lombard, Fabien; Guidi, Lionel; Kiørboe, Thomas (25 de setembro de 2013). MacKenzie, Brian R., ed. «Effect of Type and Concentration of Ballasting Particles on Sinking Rate of Marine Snow Produced by the Appendicularian Oikopleura dioica». PLoS ONE (em inglês). 8 (9): e75676. ISSN 1932-6203. PMC 3783419
 . PMID 24086610. doi:10.1371/journal.pone.0075676. Consultado em 3 de outubro de 2025
. PMID 24086610. doi:10.1371/journal.pone.0075676. Consultado em 3 de outubro de 2025
- ↑ Rost, Björn; Riebesell, Ulf (2004). Thierstein, Hans R.; Young, Jeremy R., eds. «Coccolithophores and the biological pump: responses to environmental changes». Berlin, Heidelberg: Springer Berlin Heidelberg (em inglês): 99–125. ISBN 978-3-642-06016-8. doi:10.1007/978-3-662-06278-4_5. Consultado em 3 de outubro de 2025
- ↑ Beaufort, L.; Probert, I.; de Garidel-Thoron, T.; Bendif, E. M.; Ruiz-Pino, D.; Metzl, N.; Goyet, C.; Buchet, N.; Coupel, P. (agosto de 2011). «Sensitivity of coccolithophores to carbonate chemistry and ocean acidification». Nature (em inglês). 476 (7358): 80–83. ISSN 0028-0836. doi:10.1038/nature10295. Consultado em 3 de outubro de 2025
- ↑ Hutchins, David A. (agosto de 2011). «Forecasting the rain ratio». Nature (em inglês). 476 (7358): 41–42. ISSN 0028-0836. doi:10.1038/476041a. Consultado em 3 de outubro de 2025
- ↑ Iglesias-Rodriguez, M. Debora; Halloran, Paul R.; Rickaby, Rosalind E. M.; Hall, Ian R.; Colmenero-Hidalgo, Elena; Gittins, John R.; Green, Darryl R. H.; Tyrrell, Toby; Gibbs, Samantha J. (18 de abril de 2008). «Phytoplankton Calcification in a High-CO 2 World». Science (em inglês). 320 (5874): 336–340. ISSN 0036-8075. doi:10.1126/science.1154122. Consultado em 3 de outubro de 2025
- ↑ de Bruijn, Douwe S.; ter Braak, Paul M.; Van de Waal, Dedmer B.; Olthuis, Wouter; van den Berg, Albert (fevereiro de 2021). «Coccolithophore calcification studied by single-cell impedance cytometry: Towards single-cell PIC:POC measurements». Biosensors and Bioelectronics (em inglês). 173. 112808 páginas. doi:10.1016/j.bios.2020.112808. Consultado em 3 de outubro de 2025