Córion
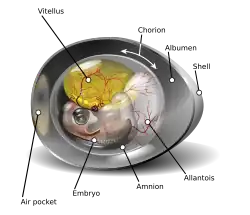
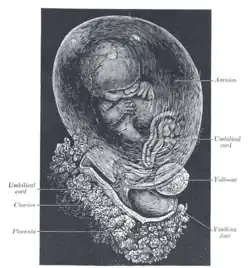
Córion ou Cório é uma membrana extra-embrionária que existe durante a gravidez e que forma a parede externa dos blastocisto em répteis, aves e mamíferos. Ele é formado pela mesoderme extra-embrionária e duas camadas de trofoblasto que envolvem o embrião e as outras membranas. As vilosidades coriónicas invadem o endométrio para permitir a transferência de nutrientes do sangue materno para o feto.[1]
Ele se desenvolve a partir de uma dobra externa na superfície do saco vitelino, que fica fora da zona pelúcida (em mamíferos), conhecida como membrana vitelina em outros animais. Nos insetos, ele é desenvolvido pelas células foliculares, enquanto o óvulo está no ovário.[2]
Une-se com o alantóide para formar o alantocório com função respiratória para aves e répteis, não em mamíferos.
Em aves e répteis o cório está localizado logo abaixo da casca; nos mamíferos o cório faz parte da placenta e também está envolvido com a remoção de resíduos. Durante a segunda semana de desenvolvimento embrionário humano, cório é a camada que reveste internamente o celoma extraembrionário e que é composto por trofoblasto e mesoderme extraembrionário. Surge durante a terceira semana de gestação, entre o o 15º dia e 17º dia de gravidez.
Tipos
- Liso
- Frondoso (formador da placenta, junto ao endométrio e o alantóide)
Funções
- Troca de gases (alantocórion)
- Formar a placenta (Córion frondoso - mamíferos)
Estrutura
Em humanos e outros mamíferos (excluindo os monotremados), o cório é uma das membranas fetais que se formam durante o período de gestação entre o feto em desenvolvimento e a mãe. O córion e o âmnio formam juntos o saco amniótico. Em humanos é formado pelo mesoderma extraembrionário e pelas duas camadas do trofoblasto que rodeia o embrião e outras membranas; as vilosidades coriónicas emergem do córion, invadem o endométrio e servem para a transferência de nutrientes do sangue materno para o fetal.
Camadas
O córion é composto por duas camadas: uma externa formada pelo trofoblasto e outra interna formada pelo mesoderma somático.
O trofoblasto é formado por uma camada interna de células cúbicas ou prismáticas, o citotrofoblasto ou camada de Langhans, e outra camada externa multinucleada (sincicial) chamada sinciciotrofoblasto.
Crescimento
O córion sofre uma rápida proliferação e forma numerosos processos, as vilosidades coriónicas, que invadem e destroem a decídua uterina, enquanto simultaneamente absorvem dela materiais nutritivos para o crescimento do embrião.
As vilosidades coriónicas são, no início, pequenas e não vasculares e consistem apenas em trofoblasto, mas aumentam o seu tamanho e ramificam-se, enquanto o mesoderma, que traz ramos dos vasos umbilicais, cresce nelas, e ficam vascularizadas.
O sangue chega às vilosidades pelas artérias umbilicais pares, que se ramificam originando as artérias coriónicas e entram nas vilosidades coriónicas como artérias dos cotilédones. Depois de circular através dos capilares das vilosidades, o sangue retorna ao embrião pela veia umbilical. Até aproximadamente o final do segundo mês de gravidez, as vilosidades cobrem todo o córion, e são quase uniformes em tamanho, mas, após esse momento, desenvolvem-se desigualmente.
Partes

A parte do cório que está em contacto com a decídua capsular atrofia, de modo que no quarto mês quase não restam vestígios das vilosidades. Esta parte do cório torna-se lisa,[3] e é denominada cório liso ou leve (do termo latino chorion laeve, que significa 'cório liso'). Como não participa na formação da placenta, também é chamada parte não placentária do cório. À medida que o cório cresce, o cório liso entra em contacto com a decidua parietal e estas camadas fundem-se.
As vilosidades no polo embrionário, que está em contacto com a decídua basal, aumentam muito em tamanho e complexidade e, portanto, esta parte é denominada cório frondoso.[3]
Assim, a placenta desenvolve-se a partir do cório frondoso e da decidua basal.
Gémeos Monocoriónicos
Os gémeos monocoriónicos são gémeos que partilham a mesma placenta. Isto ocorre em 0,3% das gestações,[4] e em 75% dos gémeos monozigóticos (idênticos), quando a separação ocorre no terceiro dia ou mais tarde após a fecundação.[5] Os restantes 25% de gémeos monozigóticos tornam-se diamnióticos dicoriónicos.[5] Esta condição pode afetar qualquer tipo de nascimento múltiplo, o que origina múltiplos monocoriónicos.
Infeções
Estudos recentes indicam que o cório pode ser suscetível a infeções patogénicas.[6] Descobertas recentes indicam que a bactéria Ureaplasma parvum pode infetar o tecido do cório, afetando assim o resultado da gravidez.[7] Além disso, foram detetados os perfis genéticos do poliomavírus JC e do poliomavírus de células de Merkel nas vilosidades coriónicas em mulheres que sofreram abortos espontâneos e em mulheres grávidas.[8][9] Outro vírus, o poliomavírus BK detetou-se nos mesmos tecidos, mas em menor grau.[10]
Referências
- ↑ "Âmnion e córion" no site Colégio Web.com.br[ligação inativa]
- ↑ Chapman, R.F. (1998) "The insects: structure and function", Section The egg and embryology. Previewed in Google Books [1] on 26 Sep 2009.
- ↑ a b Genbačev, O; Vićovac, L; Larocque, N (julho de 2015). «The role of chorionic cytotrophoblasts in the smooth chorion fusion with parietal decidua.». Placenta. 36 (7): 716–22. PMC 4476638
 . PMID 26003500. doi:10.1016/j.placenta.2015.05.002
. PMID 26003500. doi:10.1016/j.placenta.2015.05.002
- ↑ Cordero L, Franco A, Joy SD, O'shaughnessy RW (dezembro de 2005). «Monochorionic diamniotic infants without twin-to-twin transfusion syndrome». Journal of Perinatology. 25 (12): 753–8. PMID 16281049. doi:10.1038/sj.jp.7211405
- ↑ a b Shulman, Lee S.; van Vugt, John M. G. (2006). Prenatal medicine. Washington, DC: Taylor & Francis. p. 447. ISBN 0-8247-2844-0
- ↑ Contini C, Rotondo JC, Magagnoli F, Maritati M, Seraceni S, Graziano A (2019). «Investigation on silent bacterial infections in specimens from pregnant women affected by spontaneous miscarriage.». J Cell Physiol. 34 (3): 433–440. PMID 30078192. doi:10.1002/jcp.26952. hdl:11392/2393176
- ↑ Contini C, Rotondo JC, Magagnoli F, Maritati M, Seraceni S, Graziano A, Poggi A, Capucci R, Vesce F, Tognon M, Martini F (2018). «Investigation on silent bacterial infections in specimens from pregnant women affected by spontaneous miscarriage.». J Cell Physiol. 234 (1): 100–9107. PMID 30078192. doi:10.1002/jcp.26952. hdl:11392/2397717
- ↑ Tagliapietra A, Rotondo JC, Bononi I, Mazzoni E, Magagnoli F, Maritati M (2019). «Footprints of BK and JC polyomaviruses in specimens from females affected by spontaneous abortion.». Hum Reprod. 34 (3): 433–440. PMID 30590693. doi:10.1002/jcp.27490. hdl:11392/2397717
- ↑ Tagliapietra A, Rotondo JC, Bononi I, Mazzoni E, Magagnoli F, Maritati M (2020). «Droplet-digital PCR assay to detect Merkel cell polyomavirus sequences in chorionic villi from spontaneous abortion affected females». J Cell Physiol. 235 (3): 1888–1894. PMID 31549405. doi:10.1002/jcp.29213. hdl:11392/2409453
- ↑ Tagliapietra A, Rotondo JC, Bononi I, Mazzoni E, Magagnoli F, Maritati M (2019). «Footprints of BK and JC polyomaviruses in specimens from females affected by spontaneous abortion.». Hum Reprod. 34 (3): 433–440. PMID 30590693. doi:10.1002/jcp.27490. hdl:11392/2397717