Hidrogenoftalato de potássio
Hidrogenoftalato de potássio
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||
| Nomes | |||||||||||||||||
| Nome IUPAC | Potassium hydrogen phthalate | ||||||||||||||||
| Outros nomes | hydrogen potassium phthalate, Sal de Ácido Ftálico, Biftalato de Potássio, Ftalato Ácido de Potássio, Ácido 1,2-benzenodicarboxílico, monopotassium salt, KHP, KHPh | ||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| Página de dados suplementares | |||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||
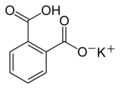
Hidrogeno ftalato de potássio ou biftalato de potássio, abreviado para simplesmente KHP (de seu nome em inglês com o símbolo do potássio, K hydrogen phthalate), é um sólido branco ou incolor e iônico que é sal de potássio do ácido ftálico de fórmula química KHC8H4O4 ou C8H5KO4. O hidrogênio é levemente ácido,e se apresenta como útil para ser usado como um padrão primário ácido-base titrimétrico porque é um sólido estável ao ar, fazendo-o fácil de ser pesado precisamente. É também usado como um padrão primário para calibração de pH-metros porque, pelas propriedades já mencionadas, seu pH em solução é muito estável. O pH de uma solução aquosa de KHP 0.05 mol.L−1 em várias temperaturas é dado pela seguinte tabela[1]:
| T (°C) | pH |
|---|---|
| 0 °C | 4.000 |
| 5 °C | 3.998 |
| 10 °C | 3.997 |
| 15 °C | 3.998 |
| 20 °C | 4.000 |
| 25 °C | 4.005 |
| 30 °C | 4.011 |
| 35 °C | 4.018 |
| 40 °C | 4.022 |
| 45 °C | 4.027 |
| 50 °C | 4.050 |
KHP pode ser usado como um agente tamponador (em combinação com HCl ou NaOH dependendo de qual lado do pH 4.0 o tampão deve situar-se) mas não deve ser usado como um tampão para reações de decarboxilização, pois tais reações degradam o KHP e destroem os grupos de conjugação.
Referências
- ↑ The Measurement of pH - Definition, Standards and Procedures Arquivado em 27 de setembro de 2007, no Wayback Machine. (em inglês)