Alelo letal
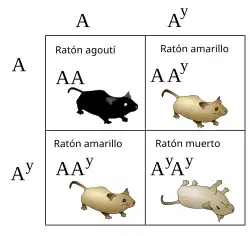
Para que um organismo possa sobreviver, são necessários muitos genes e se um alelo torna um desses genes não funcional ou faz com que o indivíduo tenha uma atividade anormal ou prejudicial, esse alelo passa a ser considerado o chamado “alelo letal” [1]
Alelo letal é o gene que sofreu uma mutação e seu aparecimento inviabiliza o embrião, ou caso o embrião sobreviva e atinja o estagio adulto[2], ele não irá contribuir com genes para a próxima geração[3]. É um dos tipos de variações das leis básicas da genética, as 1º e 2º Leis de Mendel.[4] Ao invés de resultar em proporção fenotípica de 3:1, ao ser cruzado dois indivíduos heterozigotos, como esperado para a 1º Lei de Mendel, a frequência fenotípica de uma característica que possua alelo letal é de 2:1, em um claro sinal de desvio da 1º Lei Mendeliana[5]
Em organismos diploides, se ambos os alelos estão mutados para causar a morte, então a mutação se comporta como letal recessivo. Em outros caos, ainda não tão bem compreendidos, a presença de apenas um alelo já é suficiente para que ocorra a letalidade, o que configura a condição como letal dominante.[6]
Um alelo recessivo letal pode ser passado para a próxima geração caso esteja em heterozigose, pois os heterozigotos apresentação características normais; no entanto, o alelo dominante letal será fatal muitas vezes antes de eles atingirem a maturidade sexual, não permitindo assim a passagem dele para as futuras geração[7]
Os genes ou alelos letais podem ser recessivos (em sua grande maioria) dominantes, condicionais, subletais ou sintéticos. Ter conhecimento sobre alelos letais se torna útil, pois nos mostra que aquele gene descoberto é essencial para a operação daquele organismo. Os alelos letais também nos indicam em qual estágio de desenvolvimento o gene normalmente atua, tendo em vista de que o alelo letal pode ocorrer de forma precoce ou tardia no desenvolvimento do embrião e também podemos saber se o fenótipo associado à morte de determinado organismo pode ser um informativo em relação à função que o gene representa [1][8].
Há indicativos de que ser um alelo letal ou não vai depender com frequência do local onde o organismo se desenvolve, pois um alelo pode ser letal em certo ambiente, mas tolerável em outro como por exemplo, quando citamos doenças hereditárias em humanos como a fibrose cística e a anemia falciforme que seriam letais sem tratamento [8].
História
O biólogo francês Lucien Cuénot foi o primeiro pesquisador a identificar a ocorrência de genes letais em animais, no início do século XX. Ele realizou estudos com camundongos de diferentes colorações, os quais revelaram um padrão de herança que não se enquadrava nas proporções estabelecidas por Gregor Mendel em suas leis da hereditariedade [9]
Cuénot observou que os camundongos de pelagem amarela apresentavam um caráter dominante, enquanto os camundongos de pelagem cinza expressavam o caráter recessivo . Quando realizava cruzamentos entre camundongos cinza (recessivos), todos os descendentes também nasciam cinza, conforme o esperado para indivíduos homozigotos recessivos (aa). No entanto, ao cruzar camundongos amarelos entre si, percebeu que a proporção fenotípica dos descendentes não correspondia ao padrão mendeliano clássico de 3:1, obtido quando Mendel cruzou plantas heterozigotas (Aa × Aa). No caso dos camundongos, a proporção observada era de 2:1, ou seja, dois indivíduos amarelos para um cinza.
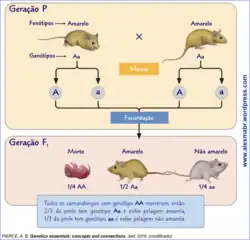
Assim, Cuénot passou a investigar o desenvolvimento embrionário dos camundongos e constatou que os embriões com genótipo homozigoto dominante (AA) (de pelagem amarela) não chegavam a nascer, pois morriam durante o desenvolvimento inicial. Essa condição foi interpretada como resultado de um gene letal dominante em homozigose. Durante a formação embrionária, indivíduos com genótipo AA apresentavam anormalidades no tecido cutâneo, incluindo o desenvolvimento de formações semelhantes a tumores, que inviabilizavam a sobrevivência. Assim, apenas os heterozigotos (Aa), de pelagem amarela, e os homozigotos recessivos (aa), de pelagem cinza, completavam o desenvolvimento e nasciam viáveis.
Seu experimento foi pioneiro ao demonstrar que determinados alelos dominantes podem ser letais em homozigose, introduzindo o conceito de gene letal na genética clássica. Esse achado ampliou a compreensão sobre os padrões de herança e mostrou que nem todos os alelos seguem rigidamente as proporções mendelianas, já que fatores letais podem alterar a sobrevivência e, consequentemente, a proporção fenotípica observada nas populações.
Tipos de alelos letais
Os alelos letais são caracterizados por um genótipo que resulta na morte de um indivíduo, quando isso ocorre e sua expressividade. Esses tipos podem ser: Letal recessivo, dominante, ligado ao sexo, completo, semiletal ou tardio.
Alelos letais recessivos (aa) são encontrados em doenças como fibrose cística, a qual portadores saudáveis são heterozigotos somente. Diferente do letal dominante, como no caso dos camundongos, que ao expressarem homozigose para o genótipo dominante, morrem precocemente antes do desenvolvimento completo do zigoto. Quando o alelo está associado a um cromossomo específico, como X, os indivíduos que possuem um alelo Y não sobrevivem devido a falha do cromossomo X com a letalidade do alelo.
Quando relacionados com o tempo ou fase que se manifesta a atuação do alelo, são encontradas três classificações. Letalidade completa, tipo mais comum dos alelos recessivos, se dá pela morte do organismo antes do desenvolvimento do sistema reprodutivo ou ainda na fase embrionária. A semi letal indica que, quando sobrevivem mesmo após o nascimento, poderão apresentar diversos problemas de saúde relacionados com a doença do gene. Diferentemente da classificação como tardio, a qual a morte ocorre após a idade reprodutiva, podendo passar o gene mais facilmente para as próximas gerações.
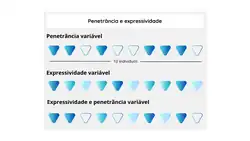
A penetrância se define pela porcentagem dos indivíduos que apresentam o fenótipo resultante do alelo associado. Algumas características como o ambiente (como temperatura) e a interação com outros genes pode resultar em um diferente fenótipo expressado, não seguindo o padrão do genótipo. Podendo ser classificado também como penetrância incompleta e variável. Em relação a expressividade, descreve a variação o qual o fenótipo é expressado, ou seja, seu grau de intensidade. Como exemplo prático de penetrância classificada como incompleta, as doenças genéticas humanas com genótipo associado a uma condição, quando apresentado uma mutação de penetrância incompleta, o indivíduo pode carregar o alelo, mas permanecer assintomático, dessa forma, não manifesta a doença ou nem seus principais sintomas.
Mutação Letal Recessiva
Quando há ausência completa de um produto gênico é letal, a modificação genética é, mais frequentemente, uma mutação de perda de função que determina a formação de um produto não-funcional. Muitas das vezes, a mutação é tolerada em caso de heterozigose, em que um alelo normal produz uma quantidade normal do produto suficiente para o desenvolvimento normal. No entanto, tal mutação se comporta como Letal Recessiva, levando os indivíduos homozigotos à morte. O período da morte é variável, em mamíferos, por exemplo, pode ocorrer durante o desenvolvimento, a primeira infância ou ainda na idade adulta.[6]
Em alguns casos, o alelo responsável pela letalidade, quando está em homozigose , também pode resultar em fenótipos mutante diferente , quando estiver em heterozigose.
Como exemplo de característica relacionada a mutação letal recessiva, temos a cor amarela do pelo de camundongos é condicionada por um alelo A, dominante sobre o alelo a, que condiciona a cor preta. Assim,todo cruzamento experimental realizado entre machos e fêmeas,ambos pretos, originava somente descendentes de pelagem preta, confirmando o esperado pela Primeira Lei de Mendel. No entanto, os cruzamentos entre machos e fêmeas amarelos nunca resultavam as proporções esperadas pela Primeira Lei de Mendel, pois:
1º- se pelo menos um dos animais cruzados fosse homozigótico, todos os descendentes deveriam ser amarelos – o que não acontecia; 2º- se ambos fossem heterozigóticos (híbridos), a proporção esperada seria de 3 amarelos para 1 preto – o que também não acontecia.
O resultado obtido do cruzamento entre indivíduos amarelos obedece sempre a proporção de 2 amarelos para 1 preto!Como explicar essa discrepância, em relação à Primeira Lei de Mendel? O primeiro cientista a estudar essa questão foi o geneticista francês Cuénot,em torno de 1905. Cuénot chegou a levantar a hipótese de que os espermatozoides portadores de cromossomos com o alelo A não conseguiam fecundar um óvulo também portador do mesmo alelo A. Essa hipótese foi, no entanto, rejeitada pelas pesquisas seguintes de vários cientistas, ficando demonstrado que a fecundação ocorre, o ovo se forma e se desenvolve, mas o indivíduo portador do genótipo AA morre no útero materno. Concluiu-se, então, que o alelo A, embora dominante em relação ao alelo a, é letal quando em dose dupla. Isso significa que quando nasce um camundongo de pelagem amarela, ele é certamente heterozigótico (Aa). Interessante é que, como o alelo A é letal somente em dose dupla, pode-se afirmar que ele é recessivo para letalidade.
As mutações recessivas letais são consideradas a maior classe de mutações.[10]
Mutação Letal Dominante
Em alguns casos a mutação letal se comporta com Dominante em relação a sua contrapartida de tipo selvagem. Nesse alelos letais dominantes, a presença de apenas um alelo já é suficiente para causar a morte do indivíduo. Isso ocorre devido ao fato de que a presença de apenas uma cópia do alelo produz o produto gênico em quantidade suficiente para ocasionar a letalidade, ou suprimindo o produto do alelo selvagem ou estando acima no limiar aceitável.[6]
Os alelos letais dominantes são relativamente raros. Para que permaneçam na população é necessário que chegue sejam transmitidos aos descendentes pelos portadores antes da sua manifestação. Se ocorrer a morte de todos os portadores do alelo, esse alelo letal irá desaparecer, retornando caso haja uma nova mutação para produzi-lo.[6]
Um importante exemplo de alelo letal dominante pode ser observado na doença de Huntington. Nessa doença, observa-se uma progressiva degeneração de nervos e motora que afeta, entre outras partes, a fala e a deglutição. É muito comum a instabilidade emocional do paciente, sendo frequentes relatos de depressão. Geralmente o início dos sintomas começa por volta dos 40 anos de idade e, como um único alelo é suficiente para determinar a doença, um filho de um doente possui 50% de chance de herdar o alelo letal.[11]
Mecanismos de morte causados por alelos letais
Os alelos letais podem provocar a morte do organismo ou inviabilizar o desenvolvimento embrionário ao interferirem em processos biológicos fundamentais. Esses efeitos resultam de diferentes mecanismos moleculares, celulares e fisiológicos.
Morte molecular
Um dos mecanismos mais diretos de letalidade é a morte celular induzida por mutação. Genes que participam da manutenção da estabilidade genômica e do reparo do DNA são essenciais para a sobrevivência das células embrionárias. Estudos recentes mostram que falhas nesses genes provocam acúmulo de dano genético, levando à ativação de vias apoptóticas e inviabilidade durante a embriogênese inicial [12].
Esses resultados indicam que a integridade do genoma é um fator determinante para a viabilidade embrionária.
Falhas em sistemas vitais
Alguns alelos letais afetam órgãos e sistemas essenciais, como o cardiovascular, respiratório e nervoso. Quando genes envolvidos na organogênese sofrem perda total de função, o resultado é a falha no desenvolvimento de estruturas vitais e, consequentemente, a morte do embrião. Pesquisas em genômica populacional também mostraram que haplótipos letais recessivos em animais e humanos estão frequentemente associados a mutações em genes de desenvolvimento e manutenção celular [13].
Interferência no desenvolvimento embrionário
Grande parte dos alelos letais atua durante o desenvolvimento embrionário, interrompendo processos como a gastrulação e a diferenciação de tecidos. Genes de sinalização e de ciclo celular são particularmente críticos nesses estágios. Há a confirmação de que a perda de genes associados à progressão do ciclo celular e à replicação do DNA causa morte embrionária precoce em modelos experimentais[14].
Alterações metabólicas e funções ceulares básicas
Alguns alelos letais atuam sobre genes de função essencial (“housekeeping”), que mantêm o metabolismo e a viabilidade celular. A perda de tais genes leva a falhas na produção de energia, na síntese de proteínas e em vias metabólicas indispensáveis, resultando em morte celular generalizada. Revisões recentes de telas CRISPR confirmam que a maioria dos genes essenciais está associada a essas funções básicas[15].
Toxicidade por ganho de função
Embora mais rara, a toxicidade causada por ganho de função também pode gerar letalidade. Nesse caso, a mutação produz uma proteína aberrante que interfere em processos celulares normais ou forma agregados tóxicos. Estudos de genômica funcional em larga escala têm identificado mutações dominantes que exercem efeitos pan-letais em células humanas[16].
Contribuições de estudos genômicos recentes
A integração de telas CRISPR, análises populacionais e modelos de organoides vem permitindo identificar milhares de genes cuja perda de função completa é incompatível com a vida. Esses resultados mostram que a letalidade genética pode ocorrer por diferentes vias — morte celular, falha de órgãos vitais, interrupção do desenvolvimento ou toxicidade molecular[17]</nowiki><ref></ref>.
Exemplos de alelos letais em organismos
Plantas
Um tipo de alelo letal em organismos fotossintetizantes, como as plantas, originalmente descoberto por Erwin Baur, em seu clássico experimento de 1907, é encontrado e descrito na planta boca-de-dragão (Antirrhinum) que possui uma cepa denominada “dourada” resultando em plantas com folhas amarelas, coincidentemente como os camundongos de Cuénot [1].
O que Erwin Baur observou é que quando duas plantas boca-de-leão douradas eram cruzadas, havia uma proporção de 2:1 entre mudas verdes e amarelas e não de 3:1; logo as plantas homozigotas douradas não apresentavam desenvolvimento comum de clorofila e morriam durante a fase embrionária ou morriam logo após o brotamento, com dois ou três dias de germinação. Uma razão 2:1 é quase sempre produzida por um alelo letal recessivo, onde os indivíduos que são aa não conseguem sobreviver, seja na fase embrionária ou após o nascimento[18].
Observar esta razão entre os descendentes de uma reprodução entre organismos com o mesmo fenótipo é uma forte pista de que um dos alelos seja letal. Neste exemplo, das folhas douradas na planta boca-de-dragão, o alelo letal é recessivo porque ele provoca a morte apenas nos homozigotos (aa) que tenham a cepa[1].
Drosófilas
Alelos letais podem ser vistos, também, em espécies do gênero Drosophila. Esses alelos foram estudados por geneticistas como Wright, Dobzhansky e Wallace, e mais recentemente por Salceda (2022) em populações naturais de Drosophila melanogaster, em Chapingo, no México. Seus experimentos consistiam em utilizar diversas linhagens portadoras de genes letais recessivos localizados no segundo cromossomo, o que o permitiu observar que quando duas linhagens de mesmo gene letal eram cruzadas, não havia descendentes viáveis homozigotos, resultando em uma proporção de sobrevivência de 2:1, ou seja, dois heterozigotos normais para cada homozigoto letal que morria ainda no estágio larval [19]. Assim, as populações de Drosophila mantêm esses alelos apenas em heterozigose, o que permite sua persistência natural mesmo sendo potencialmente deletérios.
Outro estudo sobre Drosophila willistoni[20], apontou uma aparição de genes letais recessivos, que, por sua vez, segundo o autor, contribuem para a manutenção da variabilidade genética. Esses genes letais são mantidos por um equilíbrio entre mutação e seleção, e sua ocorrência em heterozigose atua como um reservatório de diversidade genética, influenciando a estrutura populacional e a adaptação ecológica da espécie. Dessa forma, mesmo que prejudiciais quando em homozigose, os alelos letais podem persistir nas populações naturais, gerando um equilíbrio que reflete em processos evolutivos, como a deriva genética e seleção natural, o que promove estabilidade e diversidade às espécies ao longo do tempo[20].
Referências
- ↑ a b c d Lobo, Ingrid (2008). «Mendelian ratios and lethal genes.». Nature Education, 1(1), 138.
- ↑ «Alelos letais». Só Biologia. Consultado em 4 de maio de 2018
- ↑ Jorde, Lynn B.; CAREY, John C.; BAMSHAD, Michael J. (18 de janeiro de 2017). Genética Médica. [S.l.]: Elsevier Brasil. ISBN 9788535285383
- ↑ Bruno, Alessandra Nejar (6 de março de 2017). Biotecnologia II: Aplicações e Tecnologias. [S.l.]: Artmed - Grupo A Educação S/A. ISBN 9788582713853
- ↑ Mendonça, Vivian (2016). Biologia : o ser humano, genética, evolução: volume 3 : ensino médio. São Paulo: AJS
- ↑ a b c d Palladino, William S. Klug | Michael R. Cummings | Charlotte A. Spencer | Michael A. (1 de janeiro de 2009). Conceitos de Genética. [S.l.]: Artmed Editora. ISBN 9788536322148
- ↑ Reece, Jane B.; Wasserman, Steven A.; Urry, Lisa A.; Cain, Michael L.; Minorsky, Peter V.; Jackson, Robert B. Biologia de Campbell. [S.l.]: Artmed Editora. ISBN 9788582712306
- ↑ a b Griffiths, A. J. F; Peichel, C.; Doebley, J. (2022). Introdução à genética (12. ed.). [S.l.]: Guanabara Koogan
- ↑ Cuénot, L. La loi de Mendel et l’hérédité de la pigmentation chez les souris. Archives de Zoologie Expérimentale et Générale, v. 10, n. 3, p. XXVII–XXX, jan. 1902.
- ↑ Schaefer, G. Bradley; Thompson, James (1 de fevereiro de 2015). Genética Médica: Uma Abordagem Integrada. [S.l.]: AMGH Editora. ISBN 9788580554762
- ↑ «Alelos letais - Mundo Educação». Mundo Educação. Consultado em 6 de maio de 2018
- ↑ Kafer, G. R.; Cesare, A. J. (2020). “A Survey of Essential Genome Stability Genes Reveals That Replication Stress Mitigation Is Critical for Peri-Implantation Embryogenesis.” Frontiers in Cell and Developmental Biology, 8:416. doi:10.3389/fcell.2020.00416
- ↑ Young, A. I. et al. (2023). “Quantifying the fraction of new mutations that are recessive lethal.” Evolution, 77(7):1539–1549. doi:10.1093/evolut/qpad045 .
- ↑ Ding, Y. et al. (2024). “Systematic Comparison of CRISPR and shRNA Screens to Identify Essential Genes Using a Graph-Based Unsupervised Learning Model.” Cells, 13(19):1653. doi:10.3390/cells13191653
- ↑ Schraivogel, D.; Steinmetz, L. M.; Parts, L. (2023). “Pooled Genome-Scale CRISPR Screens in Single Cells.” Annual Review of Genetics, 57:223–244. doi:10.1146/annurev-genet-072920-013842
- ↑ Krill-Burger, J. M. et al. (2023). “Partial gene suppression improves identification of cancer vulnerabilities when CRISPR-Cas9 knockout is pan-lethal.” Genome Biology, 24:192. doi:10.1186/s13059-023-03020-w
- ↑ Liang, J. et al. (2023). “In-organoid single-cell CRISPR screening reveals determinants of hepatocyte differentiation and maturation.” Genome Biology, 24:251. doi:10.1186/s13059-023-03084-8<nowiki>
- ↑ Ingram, G. C., et al. (1998). The Antirrhinum ERG gene encodes a protein related to bacterial small GTPases and is required for embryonic viability. Current Biology, Volume 8, Issue 19, 1079 - 1082.
- ↑ Salceca, Victor M. Alelismo para genes letales en una población natural de Drosophila melanogaster originaria de chapingo, estado de México. Brazilian Journal of Animal and Environmental Research, v. 5, n. 2, p. 1844-1851, 2022.
- ↑ a b Garcia, Rosane Nunes. Variabilidade Genética e ecológica de Drosophila willistoni (DIPTERA, DROSOPHILIDAE): uma abordagem molecular através do isolamento e caracterização de fragmentos heterogêneos de DNA. 2004.