Adipogênese
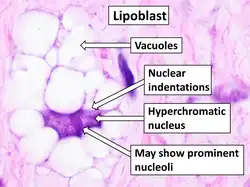
A adipogênese é a formação de adipócitos (células de gordura) a partir de células-tronco.[1] Envolve duas fases: determinação e diferenciação terminal. A determinação é que as células-tronco mesenquimais se comprometem com as células precursoras dos adipócitos, também conhecidas como lipoblastos ou pré-adipócitos, que perdem o potencial de se diferenciar em outros tipos de células, como condrócitos, miócitos e osteoblastos.[2] A diferenciação terminal ocorre quando os pré-adipócitos se diferenciam em adipócitos maduros. Os adipócitos podem surgir de pré-adipócitos residentes no tecido adiposo ou de células progenitoras derivadas da medula óssea que migram para o tecido adiposo.[3]
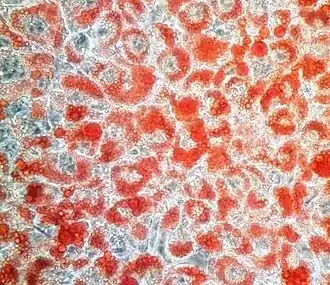
Os adipócitos desempenham um papel vital na homeostase energética e processam a maior reserva de energia como triglicerol no corpo dos animais.[4] Os adipócitos permanecem em um estado dinâmico, eles começam a se expandir quando a ingestão energética é maior que o gasto e sofrem mobilização quando o gasto energético excede a ingestão. Esse processo é altamente regulado por hormônios contrarreguladores aos quais essas células são muito sensíveis. O hormônio insulina promove a expansão, enquanto os contra-hormônios epinefrina, glucagon e ACTH promovem a mobilização. A adipogênese é um processo de diferenciação celular rigorosamente regulado, no qual células-tronco mesenquimais se transformam em pré-adipócitos e os pré-adipócitos se diferenciam em adipócitos. A diferenciação celular é uma mudança nos padrões de expressão genética que altera a expressão genética multipotente para a expressão genética específica do tipo de célula. Portanto, fatores de transcrição são cruciais para a adipogênese. Fatores de transcrição, receptor ativado por proliferador de peroxis γ (PPARγ) e proteínas de ligação ao intensifcador CCAAT (C/EBPs) são os principais reguladores da adipogênese.[5] Comparando com células de outras linhagens, a diferenciação in vitro de células de gordura é autêntica e recapitula a maioria das características da diferenciação in vivo. As principais características dos adipócitos diferenciados são parada do crescimento, alteração morfológica, alta expressão de genes lipogênicos e produção de adipocinas como adiponectina, leptina, resistina (no camundongo, não em humanos) e TNF-alfa.[6][7]
Diferenciação
Estudos in vitro sobre diferenciação utilizaram a linhagem de pré-adipócitos pré-comprometidos, como as linhas celulares 3T3-L1 e 3T3-F442A, ou pré-adipócitos isolados da fração estromal-vascular do tecido adiposo branco. A diferenciação in vitro é um processo altamente ordenado. Em primeiro lugar, os pré-adipócitos em proliferação interrompem o crescimento, geralmente por inibição de contato. A parada do crescimento foi seguida pelos primeiros eventos, incluindo uma mudança morfológica do pré-adipócito do formato de fibroblasto para o formato redondo e a indução dos fatores de transcrição C/EBPβ e C/EBPδ. A segunda fase da parada do crescimento é a expressão de dois fatores-chave de transcrição, PPARγ e C/EBPα, que promovem a expressão de genes que conferem as características de adipócitos maduros. Esses genes incluem proteína de adipócitos (aP2), receptor de insulina, glicerofosfato desidrogenase, sintase de ácidos graxos, acetil CoA carboxilase, transportador de glicose tipo 4 (Glut 4) e assim por diante.[8] Por meio desse processo, gotículas lipídicas se acumulam no adipócito. Entretanto, as linhagens celulares de pré-adipócitos têm dificuldade em se diferenciar em adipócitos. Os pré-adipócitos apresentam marcadores de superfície CD45− CD31− CD34+ CD29+ SCA1+ CD24+ que podem proliferar e se diferenciar em adipócitos in vivo.[9]
Modelos de diferenciação in vitro
| Linha Celular | Origem | Protocolo de Diferenciação |
|---|---|---|
| Pré-adipócitos comprometidos | ||
| 3T3-L1 | Subclone do Swiss 3T3[10] | FBS+ I+ D+ M |
| 3T3-F442A | Subclone do Swiss 3T3[11] | FBS + I |
| Ob17 | Adipócitos diferenciados da gordura epididimal de camundongos C57BL/6J ob/ob[12] | FBS + I + T3 |
| TA1 | Subclone de C3H10T1/2[13] | FBS + D + I |
| 30A5 | Subclone de C3H10T1/2[14] | FBS + D + M + I |
| 1246 | Subclone adipogênico da linha celular de teratocarcinoma de camundongo CH3 T984[15] | D + M + I |
| Não comprometido com potencial adipogênico | ||
| NIH3T3 | Células embrionárias de camundongo NIH Swiss[16] | Expressão ectópica de PPAR-gama, C/EBP-alfa ou C/EBP-beta + D + M + I |
| Swiss 3T3 | Células embrionárias de camundongo suíço[17] | Expressão ectópica de C/EBP-alfa |
| Balb/3T3 | Células embrionárias de camundongo Balb/c[18] | Expressão ectópica de C/EBP-alfa |
| C3H 10T1/2 | Células embrionárias de camundongo C3H[19] | Ligante PPAR-gama |
| Kusa 4b10 | linhagem de células estromais da medula óssea de camundongo[20] | FBS + I + D + M |
| C2C12 | Músculos da coxa de camundongos C3H[21] | Tiazolidinedionas |
| G8 | Músculos dos membros posteriores do feto de camundongo suíço webster[22] | Expressão ectópica de PPAR-gama + CEBP/alfa + D + I |
| FBS = Soro Fetal Bovino, D = Dexametasona, I = Insulina, M = Metilisobutilxantina, T3 = Triiodotironina | ||
Regulamentos transcricionais
PPARγ
PPARγ é um membro da superfamília de receptores nucleares e é o principal regulador da adipogênese. O PPARγ heterodimeriza com o receptor retinoide X (RXR) e então se liga ao DNA, que ativa os promotores dos genes posteriores. PPARγ induz genes específicos de células de gordura, incluindo aP2, adiponectina e fosfoenolpiruvato carboxiquinase (PEPCK). A ativação do PPARg tem efeitos em vários aspectos das características dos adipócitos maduros, como alterações morfológicas, acúmulo de lipídios e aquisição de sensibilidade à insulina.[23] O PPARγ é necessário e suficiente para promover a diferenciação das células de gordura. O PPARγ é necessário para a diferenciação das células-tronco embrionárias (células ES) em adipócitos.[24] A expressão do próprio PPARγ é suficiente para converter fibroblastos em adipócitos in vitro.[25] Foi demonstrado que outros fatores pró-adipogênicos, como C/EBPs e fatores semelhantes a Krüppel (KLFs), induzem o promotor PPARγ. Além disso, o PPARγ também é necessário para manter a expressão de genes que caracterizam o adipócito maduro.[26] Tiazolidinedionas (TZDs), agentes antidiabéticos que apresentam um coquetel de diferenciação bem utilizado in vitro, promovendo a atividade do PPARγ.[27][28]
C/EBPs, fatores de transcrição, são membros da classe de zíper de leucina básica. O AMPc, um indutor da adipogênese, pode promover a expressão de C/EBPβ e C/EBPδ.[29] No estágio inicial da diferenciação, acredita-se que o aumento transitório dos níveis de mRNA e proteína C/EBPβ e C/EBPδ ativa os fatores de transcrição adipogênicos, PPARγ e C/EBPα. PPARγ e C/EBPα podem retroalimentar-se para induzir a expressão um do outro, bem como dos seus genes posteriores.[30] C/EBPα também desempenha um papel importante na sensibilidade à insulina dos adipócitos.[31] Entretanto, C/EBPγ suprime a diferenciação que pode ser devida à inativação por C/EBPβ.[32]
Cascata transcricional
Embora PPARγ e C/EBPα sejam os principais reguladores da adipogênese, outros fatores de transcrição atuam na progressão da diferenciação. O fator de determinação e diferenciação de adipócitos 1 (ADD1) e a proteína de ligação ao elemento regulador de esterol 1 (SREBP1) podem ativar o PPARγ pela produção de um ligante endógeno do PPARγ ou promover diretamente a expressão do PPARγ. A proteína de ligação ao elemento responsivo ao AMPc promove a diferenciação, enquanto a ativação de PPARγ e C/EBPα também responde à regulação negativa. O fator de ligação ao fator de células T/intensificador linfoide (TCF/LEF),[33] GATA2/3,[34] receptor de ácido retinóico α,[35] e SMAD6/7[36] não afetam a expressão de C/EBPβ e C/EBPδ, mas inibem a indução de PPARγ e C/EBPα.[37]
Outros regulamentos
Produtos do sistema endócrino, como insulina, IGF-1, AMPc, glicocorticóide e triiodotironina induzem efetivamente a adipogênese em pré-adipócitos.[38][39][40]
Insulina e IGF1
A insulina regula a adipogênese por meio da sinalização do receptor do fator de crescimento semelhante à insulina 1 (IGF1). A insulina/IGF1 promove os fatores de transcrição de indução que regulam a diferenciação terminal.[41]
Sinalização WNT
A sinalização Wnt/β-catenina suprime a adipogênese, promovendo a diferenciação de células-tronco mesenquimais em miócitos e osteócitos, mas bloqueando o comprometimento com a linhagem adipocítica.[42] Wnt/β-catenina inibe a diferenciação de pré-adipócitos ao inibir a indução de PPARγ e C/EBPα.[43]
BMPs
As proteínas morfogenéticas ósseas (BMPs) são membros da superfamília do fator de crescimento transformador β (TGFβ). A BMP2 pode estimular a determinação de células multipotentes ou induzir a osteogênese por meio de diferentes heterômeros receptores.[44] As BMPs também promovem a diferenciação de pré-adipócitos.[45][46]
Células senescentes
Foi demonstrado que células progenitoras adiposas senescentes no tecido adiposo subcutâneo suprimem a diferenciação adipogênica.[47] A redução da adipogênese em pessoas obesas é devida ao aumento de células senescentes no tecido adiposo, e não à redução do número de células-tronco/progenitoras.[48]
Notas
- Este artigo foi inicialmente traduzido, total ou parcialmente, do artigo da Wikipédia em inglês cujo título é «Adipogenesis».
Referências
- ↑ «Adipogenesis». Merriam-Webster. Consultado em 3 de janeiro de 2020
- ↑ Gregoire FM, Smas CM, Sul HS (julho de 1998). «Understanding adipocyte differentiation». Physiological Reviews. 78 (3): 783–809. PMID 9674695. doi:10.1152/physrev.1998.78.3.783
- ↑ Hausman GJ, Hausman DB (2006). «Search for the preadipocyte progenitor cell». Journal of Clinical Investigation. 116 (12): 3103–3106. PMC 1679717
 . PMID 17143324. doi:10.1172/JCI30666
. PMID 17143324. doi:10.1172/JCI30666
- ↑ Cornelius P, MacDougald OA, Lane MD (1994). «Regulation of adipocyte development». Annual Review of Nutrition. 14: 99–129. PMID 7946535. doi:10.1146/annurev.nu.14.070194.000531
- ↑ Rosen ED, MacDougald OA (dezembro de 2006). «Adipocyte differentiation from the inside out». Nature Reviews. Molecular Cell Biology. 7 (12): 885–96. PMID 17139329. doi:10.1038/nrm2066
- ↑ Mubtasim, Noshin; Gollahon, Lauren (9 de agosto de 2023). «Characterizing 3T3-L1 MBX Adipocyte Cell Differentiation Maintained with Fatty Acids as an In Vitro Model to Study the Effects of Obesity». Life (Basel, Switzerland) (8). 1712 páginas. ISSN 2075-1729. PMC 10455818
 . PMID 37629569. doi:10.3390/life13081712. Consultado em 1 de maio de 2025
. PMID 37629569. doi:10.3390/life13081712. Consultado em 1 de maio de 2025
- ↑ Stacey, D. Heath; Hanson, Summer E.; Lahvis, Garet; Gutowski, Karol A.; Masters, Kristyn S. (novembro de 2009). «In vitro Adipogenic Differentiation of Preadipocytes Varies with Differentiation Stimulus, Culture Dimensionality, and Scaffold Composition». Tissue Engineering Part A (11): 3389–3399. ISSN 1937-3341. doi:10.1089/ten.tea.2008.0293. Consultado em 1 de maio de 2025
- ↑ Rosen ED, Walkey CJ, Puigserver P, Spiegelman BM (junho de 2000). «Transcriptional regulation of adipogenesis». Genes & Development. 14 (11): 1293–307. PMID 10837022. doi:10.1101/gad.14.11.1293

- ↑ Rodeheffer MS, Birsoy K, Friedman JM (outubro de 2008). «Identification of white adipocyte progenitor cells in vivo». Cell. 135 (2): 240–9. PMID 18835024. doi:10.1016/j.cell.2008.09.036

- ↑ Green H, Kehinde O (28 de fevereiro de 1974). «Sublines of mouse 3T3 cells that accumulate lipid». Cell. 1 (3): 113–116. doi:10.1016/0092-8674(74)90126-3
- ↑ Green H, Kehinde O (janeiro de 1976). «Spontaneous heritable changes leading to increased adipose conversion in 3T3 cells». Cell. 7 (1): 105–13. PMID 949738. doi:10.1016/0092-8674(76)90260-9
- ↑ Négrel R, Grimaldi P, Ailhaud G (dezembro de 1978). «Establishment of preadipocyte clonal line from epididymal fat pad of ob/ob mouse that responds to insulin and to lipolytic hormones». Proceedings of the National Academy of Sciences of the United States of America. 75 (12): 6054–8. Bibcode:1978PNAS...75.6054N. PMC 393116
 . PMID 216011. doi:10.1073/pnas.75.12.6054
. PMID 216011. doi:10.1073/pnas.75.12.6054
- ↑ Chapman AB, Knight DM, Dieckmann BS, Ringold GM (dezembro de 1984). «Analysis of gene expression during differentiation of adipogenic cells in culture and hormonal control of the developmental program». The Journal of Biological Chemistry. 259 (24): 15548–55. PMID 6392298. doi:10.1016/S0021-9258(17)42583-X

- ↑ Pape ME, Kim KH (maio de 1988). «Effect of tumor necrosis factor on acetyl-coenzyme A carboxylase gene expression and preadipocyte differentiation». Molecular Endocrinology. 2 (5): 395–403. PMID 2901666. doi:10.1210/mend-2-5-395

- ↑ Darmon M, Serrero G, Rizzino A, Sato G (abril de 1981). «Isolation of myoblastic, fibro-adipogenic, and fibroblastic clonal cell lines from a common precursor and study of their requirements for growth and differentiation». Experimental Cell Research. 132 (2): 313–27. PMID 7215448. doi:10.1016/0014-4827(81)90107-5
- ↑ Jainchill JL, Aaronson SA, Todaro GJ (novembro de 1969). «Murine sarcoma and leukemia viruses: assay using clonal lines of contact-inhibited mouse cells». Journal of Virology. 4 (5): 549–53. PMC 375908
 . PMID 4311790. doi:10.1128/jvi.4.5.549-553.1969
. PMID 4311790. doi:10.1128/jvi.4.5.549-553.1969
- ↑ Todaro GJ, Green H (maio de 1963). «Quantitative studies of the growth of mouse embryo cells in culture and their development into established lines». The Journal of Cell Biology. 17 (2): 299–313. PMC 2106200
 . PMID 13985244. doi:10.1083/jcb.17.2.299
. PMID 13985244. doi:10.1083/jcb.17.2.299
- ↑ Aaronson SA, Todaro GJ (outubro de 1968). «Development of 3T3-like lines from Balb-c mouse embryo cultures: transformation susceptibility to SV40». Journal of Cellular Physiology. 72 (2): 141–8. PMID 4301006. doi:10.1002/jcp.1040720208
- ↑ Reznikoff CA, Brankow DW, Heidelberger C (dezembro de 1973). «Establishment and characterization of a cloned line of C3H mouse embryo cells sensitive to postconfluence inhibition of division». Cancer Research. 33 (12): 3231–8. PMID 4357355
- ↑ Allan EH, Häusler KD, Wei T, Gooi JH, Quinn JM, Crimeen-Irwin B, et al. (agosto de 2008). «EphrinB2 regulation by PTH and PTHrP revealed by molecular profiling in differentiating osteoblasts». Journal of Bone and Mineral Research. 23 (8): 1170–81. PMID 18627264. doi:10.1359/jbmr.080324

- ↑ Yaffe D, Saxel O (22–29 de dezembro de 1977). «Serial passaging and differentiation of myogenic cells isolated from dystrophic mouse muscle». Nature. 270 (5639): 725–7. Bibcode:1977Natur.270..725Y. PMID 563524. doi:10.1038/270725a0
- ↑ Christian CN, Nelson PG, Peacock J, Nirenberg M (maio de 1977). «Synapse formation between two clonal cell lines». Science. 196 (4293): 995–8. Bibcode:1977Sci...196..995C. PMID 193191. doi:10.1126/science.193191
- ↑ Mota de Sá P, Richard AJ, Hang H, Stephens JM (março de 2017). «Transcriptional Regulation of Adipogenesis». Comprehensive Physiology. 7 (2): 635–674. ISBN 9780470650714. PMID 28333384. doi:10.1002/cphy.c160022
- ↑ Rosen ED, Sarraf P, Troy AE, Bradwin G, Moore K, Milstone DS, et al. (outubro de 1999). «PPAR gamma is required for the differentiation of adipose tissue in vivo and in vitro». Molecular Cell. 4 (4): 611–7. PMID 10549292. doi:10.1016/s1097-2765(00)80211-7

- ↑ Tontonoz P, Hu E, Spiegelman BM (dezembro de 1994). «Stimulation of adipogenesis in fibroblasts by PPAR gamma 2, a lipid-activated transcription factor». Cell. 79 (7): 1147–56. PMID 8001151. doi:10.1016/0092-8674(94)90006-x
- ↑ Tamori Y, Masugi J, Nishino N, Kasuga M (julho de 2002). «Role of peroxisome proliferator-activated receptor-gamma in maintenance of the characteristics of mature 3T3-L1 adipocytes». Diabetes. 51 (7): 2045–55. PMID 12086932. doi:10.2337/diabetes.51.7.2045

- ↑ Gardner, Olivia S.; Shiau, Chung-Wai; Chen, Ching-Shih; Graves, Lee M. (18 de março de 2005). «Peroxisome Proliferator-activated Receptor γ-independent Activation of p38 MAPK by Thiazolidinediones Involves Calcium/Calmodulin-dependent Protein Kinase II and Protein Kinase R: CORRELATION WITH ENDOPLASMIC RETICULUM STRESS*». Journal of Biological Chemistry (11): 10109–10118. ISSN 0021-9258. doi:10.1074/jbc.M410445200. Consultado em 1 de maio de 2025
- ↑ «Ciglitazone - an overview». sciencedirect.com. Consultado em 1 de maio de 2025
- ↑ Cao Z, Umek RM, McKnight SL (setembro de 1991). «Regulated expression of three C/EBP isoforms during adipose conversion of 3T3-L1 cells». Genes & Development. 5 (9): 1538–52. PMID 1840554. doi:10.1101/gad.5.9.1538

- ↑ MacDougald OA, Mandrup S (janeiro de 2002). «Adipogenesis: forces that tip the scales». Trends in Endocrinology and Metabolism. 13 (1): 5–11. PMID 11750856. doi:10.1016/s1043-2760(01)00517-3
- ↑ Wu Z, Rosen ED, Brun R, Hauser S, Adelmant G, Troy AE, et al. (fevereiro de 1999). «Cross-regulation of C/EBP alpha and PPAR gamma controls the transcriptional pathway of adipogenesis and insulin sensitivity». Molecular Cell. 3 (2): 151–8. PMID 10078198. doi:10.1016/s1097-2765(00)80306-8

- ↑ «CAAT Enhancer Binding - an overview». www.sciencedirect.com. Consultado em 1 de maio de 2025
- ↑ Ross SE, Hemati N, Longo KA, Bennett CN, Lucas PC, Erickson RL, MacDougald OA (agosto de 2000). «Inhibition of adipogenesis by Wnt signaling». Science. 289 (5481): 950–3. Bibcode:2000Sci...289..950R. PMID 10937998. doi:10.1126/science.289.5481.950
- ↑ Tong Q, Dalgin G, Xu H, Ting CN, Leiden JM, Hotamisligil GS (outubro de 2000). «Function of GATA transcription factors in preadipocyte-adipocyte transition». Science. 290 (5489): 134–8. Bibcode:2000Sci...290..134T. PMID 11021798. doi:10.1126/science.290.5489.134
- ↑ Schwarz EJ, Reginato MJ, Shao D, Krakow SL, Lazar MA (março de 1997). «Retinoic acid blocks adipogenesis by inhibiting C/EBPbeta-mediated transcription». Molecular and Cellular Biology. 17 (3): 1552–61. PMC 231881
 . PMID 9032283. doi:10.1128/mcb.17.3.1552
. PMID 9032283. doi:10.1128/mcb.17.3.1552
- ↑ Choy L, Skillington J, Derynck R (maio de 2000). «Roles of autocrine TGF-beta receptor and Smad signaling in adipocyte differentiation». The Journal of Cell Biology. 149 (3): 667–82. PMC 2174852
 . PMID 10791980. doi:10.1083/jcb.149.3.667
. PMID 10791980. doi:10.1083/jcb.149.3.667
- ↑ Guo, Ge; Wang, Wanli; Tu, Mengjie; Zhao, Binbin; Han, Jiayang; Li, Jiali; Pan, Yanbing; Zhou, Jie; Ma, Wen (2024). «Deciphering adipose development: Function, differentiation and regulation». Developmental Dynamics (em inglês) (11): 956–997. ISSN 1097-0177. doi:10.1002/dvdy.708. Consultado em 1 de maio de 2025
- ↑ Student AK, Hsu RY, Lane MD (maio de 1980). «Induction of fatty acid synthetase synthesis in differentiating 3T3-L1 preadipocytes». The Journal of Biological Chemistry. 255 (10): 4745–50. PMID 7372608. doi:10.1016/S0021-9258(19)85559-X

- ↑ Spiegelman BM, Green H (setembro de 1980). «Control of specific protein biosynthesis during the adipose conversion of 3T3 cells». The Journal of Biological Chemistry. 255 (18): 8811–18. PMID 6773950. doi:10.1016/S0021-9258(18)43575-2

- ↑ Amri EZ, Dani C, Doglio A, Etienne J, Grimaldi P, Ailhaud G (agosto de 1986). «Adipose cell differentiation: evidence for a two-step process in the polyamine-dependent Ob1754 clonal line». The Biochemical Journal. 238 (1): 115–22. PMC 1147104
 . PMID 3800927. doi:10.1042/bj2380115
. PMID 3800927. doi:10.1042/bj2380115
- ↑ Khan, Muhammad Zahid; Zugaza, Jose Luis; Torres Aleman, Ignacio (1 de janeiro de 2025). «The signaling landscape of insulin-like growth factor 1». Journal of Biological Chemistry (1). 108047 páginas. ISSN 0021-9258. doi:10.1016/j.jbc.2024.108047. Consultado em 1 de maio de 2025
- ↑ Christodoulides C, Lagathu C, Sethi JK, Vidal-Puig A (janeiro de 2009). «Adipogenesis and WNT signalling». Trends in Endocrinology and Metabolism. 20 (1): 16–24. PMC 4304002
 . PMID 19008118. doi:10.1016/j.tem.2008.09.002
. PMID 19008118. doi:10.1016/j.tem.2008.09.002
- ↑ Prestwich, Tyler C.; Macdougald, Ormond A. (dezembro de 2007). «Wnt/beta-catenin signaling in adipogenesis and metabolism». Current Opinion in Cell Biology (6): 612–617. ISSN 0955-0674. PMC 2709272
 . PMID 17997088. doi:10.1016/j.ceb.2007.09.014. Consultado em 1 de maio de 2025
. PMID 17997088. doi:10.1016/j.ceb.2007.09.014. Consultado em 1 de maio de 2025
- ↑ Chen D, Ji X, Harris MA, Feng JQ, Karsenty G, Celeste AJ, et al. (julho de 1998). «Differential roles for bone morphogenetic protein (BMP) receptor type IB and IA in differentiation and specification of mesenchymal precursor cells to osteoblast and adipocyte lineages». The Journal of Cell Biology. 142 (1): 295–305. PMC 2133031
 . PMID 9660882. doi:10.1083/jcb.142.1.295
. PMID 9660882. doi:10.1083/jcb.142.1.295
- ↑ Schulz, Tim J.; Tseng, Yu-Hua (2009). «Emerging role of bone morphogenetic proteins in adipogenesis and energy metabolism». Cytokine & Growth Factor Reviews (5-6): 523–531. ISSN 1879-0305. PMC 2799934
 . PMID 19896888. doi:10.1016/j.cytogfr.2009.10.019. Consultado em 1 de maio de 2025
. PMID 19896888. doi:10.1016/j.cytogfr.2009.10.019. Consultado em 1 de maio de 2025
- ↑ Suenaga, Masashi; Kurosawa, Norio; Asano, Hiroki; Kanamori, Yohei; Umemoto, Takenao; Yoshida, Hirofumi; Murakami, Masaru; Kawachi, Hiroyuki; Matsui, Tohru (1 de outubro de 2013). «Bmp4 expressed in preadipocytes is required for the onset of adipocyte differentiation». Cytokine (1): 138–145. ISSN 1043-4666. doi:10.1016/j.cyto.2013.07.011. Consultado em 1 de maio de 2025
- ↑ Eckel-Mahan K, Latre AR, Kolonin MG (2020). «Adipose Stromal Cell Expansion and Exhaustion: Mechanisms and Consequences». Cells. 9 (4). 863 páginas. PMC 7226766
 . PMID 32252348. doi:10.3390/cells9040863
. PMID 32252348. doi:10.3390/cells9040863
- ↑ Gustafson B, Nerstedt A, Smith U (2019). «Reduced subcutaneous adipogenesis in human hypertrophic obesity is linked to senescent precursor cells». Nature Communications. 10 (1). 2757 páginas. Bibcode:2019NatCo..10.2757G. PMC 6588633
 . PMID 31227697. doi:10.1038/s41467-019-10688-x
. PMID 31227697. doi:10.1038/s41467-019-10688-x