Adenilato ciclase
A adenilato ciclase (AC, EC 4.6.1.1), também chamada adenilil ciclase ou adenil ciclase, é uma enzima que exerce uma função reguladora essencial na célula. É a enzima mais polifilética conhecida, uma vez que foram descobertas seis classes desta enzima, todas catalisando a mesma reação, mas representando famílias de genes que não estão relacionados entre si e não apresentam homologia estrutural ou de sequência. A classe mais conhecida de adenilato ciclase é a classe III ou AC-III (utilizam-se números romanos para as classes). A AC-III está amplamente distribuída entre os eucariotas e desempenha funções importantes em muitos tecidos humanos. Algumas bactérias também possuem AC.
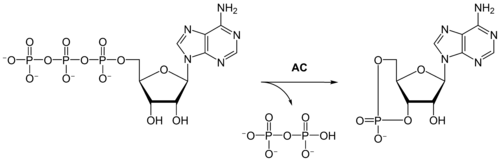
Todas as classes de AC catalisam a conversão de ATP em AMP 3',5'-cíclico (cAMP) e pirofosfato. Geralmente, requerem catiãos divalentes (normalmente Mg2+) para que a reação ocorra, os quais parecem estar muito envolvidos no mecanismo enzimático. O cAMP produzido pela AC serve depois como sinal regulador que atua por meio de proteínas que se ligam ao cAMP, como factores de transcrição ou outras enzimas como, por exemplo, cinases dependentes de cAMP. No mecanismo de ação das hormonas que ativam a AC, o cAMP é denominado segundo mensageiro (o primeiro mensageiro é a hormona).
AC de classe I
As AC de classe I estão presentes em muitas bactérias, como a E. coli. Esta foi a primeira classe de AC a ser caraterizada. Observou-se que a E. coli, quando privada de glicose, produz cAMP que serve como sinal interno para ativar a expressão de genes para importar e metabolizar outros açúcares. O cAMP exerce este efeito ao ligar-se ao factor de transcrição CRP, também chamado CAP. As AC de classe I são grandes enzimas citosólicas (de ~100 kDa) com um grande domínio regulador (de ~50 kDa) que indiretamente deteta os níveis de glicose. Em 2012, ainda não tinha sido obtida nenhuma estrutura cristalina destas enzimas de classe I.
AC de classe II
Estas AC são toxinas secretadas por bactérias patogénicas como a Bacillus anthracis e a Bordetella pertussis durante a infeção. Estas bactérias também secretam proteínas que facilitam a entrada da AC-II na célula hóspede, onde a atividade de adenilato ciclase exógena afeta os processos celulares normais. O gene para as AC de classe II denomina-se cyaA. Conhecem-se várias estruturas cristalinas de enzimas AC-II.
AC de classe III
Estas AC são as mais conhecidas devido aos intensos estudos realizados sobre elas, dado o seu papel fundamental na saúde humana. Também se encontram em algumas bactérias, nomeadamente na Mycobacterium tuberculosis, na qual parecem ter um papel chave na sua patogénese. A maioria das AC-III são proteínas de membrana integrais envolvidas na transdução de sinais extracelular para gerar respostas intracelulares. O funcionamento geral das adenilato ciclases humanas é o seguinte: as adenilato ciclases são frequentemente ativadas ou inibidas por proteínas G, que estão acopladas a recetores de membrana e, assim, podem responder a estímulos hormonais. Quando a adenilato ciclase é ativada, produz-se AMP cíclico, que funciona como segundo mensageiro (sendo a hormona o primeiro), que interage e regula outras proteínas como a proteína cinase A e os canais iónicos de abertura regulada por nucleótidos cíclicos.
O prémio Nobel foi concedido a Earl Sutherland em 1971 pelo descobrimento do papel crucial da AC-III no fígado humano, onde a adrenalina estimula indiretamente a AC para mobilizar a energia armazenada na resposta de "luta ou fuga". O efeito da adrenalina é exercido por meio da cascata de sinalização da proteína G, a qual transmite sinais químicos do exterior da célula, através da membrana, até ao interior da célula (citoplasma). O sinal externo (neste caso, a adrenalina) liga-se a um recetor, o qual transmite um sinal à proteína G, que por sua vez transmite um sinal à adenilato ciclase, e esta converte o ATP em cAMP. O cAMP funciona como segundo mensageiro.[1]
Descobriu-se uma adenilato ciclase fotoativável (PAC) na Euglena gracilis, que pode ser expressa noutros organismos por meio de manipulações genéticas. Ao iluminar uma célula que conteña PAC com luz azul, esta enzima é ativada e aumenta bruscamente a velocidade de conversão do ATP em cAMP. Esta é uma técnica útil para investigadores em neurociência porque permite aumentar os níveis intracelulares de cAMP em determinados neurónios, e estudar o efeito desse incremento na atividade neural e no comportamento do organismo. Por exemplo, a expressão da PAC em certos neurónios altera o comportamento de higiene das moscas da fruta expostas à luz azul.[2]
Estrutura das AC-III
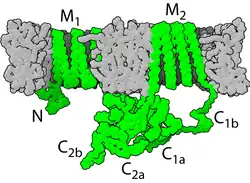
A maioria das AC de classe III são proteínas transmembranares com 12 segmentos transmembranares. A proteína está organizada começando por 6 segmentos transmembranares, seguidos de um domínio citoplasmático C1, mais 6 segmentos de membrana e, finalmente, um segundo domínio citoplasmático chamado C2. As partes importantes para o seu funcionamento são as regiões N-terminal e as C1 e C2. Os subdomínios C1a e C2a são homólogos e formam um "dímero" intramolecular onde se situa o centro ativo. Na Mycobacterium tuberculosis, o polipéptido AC-III tem apenas metade do comprimento, compreendendo um domínio de seis segmentos transmembranares seguido de um domínio citoplasmático, mas dois destes formam um homodímero funcional que recorda a arquitetura do de mamíferos.
Tipos de AC-III
Nos mamíferos conhecem-se 10 isoformas de adenilato ciclases, que são: ADCY1, ADCY2, ADCY3, ADCY4, ADCY5, ADCY6, ADCY7, ADCY8, ADCY9 e ADCY10. Estas são por vezes denominadas simplesmente AC1, AC2, etc., e, gerando alguma confusão, por vezes utilizam-se números romanos para estas isoformas, as quais pertencem todas às AC de classe III. Diferenciam-se principalmente no modo como são reguladas e expressam-se de forma diferencial em vários tecidos durante o desenvolvimento dos mamíferos.
Regulação da AC-III
A adenilato ciclase é regulada de forma dual pelas proteínas G (a Gs estimula a atividade e a Gi inibe-a), pela forscolina e também por outros efetores específicos de certas isoformas:
- As isoformas III, V e VIII são também estimuladas pelo Ca2+/calmodulina.
- As isoformas I e VI são inibidas pelo Ca2+ de maneira independente da calmodulina.
- As isoformas II, IV e IX são estimuladas pelas subunidades beta e gama da proteína G.
- As isoformas I, V e VI são inibidas com maior clareza pela Gi, enquanto outras isoformas apresentam uma menor regulação dual pela proteína G inibitória.
- A AC solúvel (sAC) não é uma forma transmembranar e não é regulada por proteínas G nem pela forscolina, mas atua como um sensor de bicarbonato/pH. A AC solúvel está presente no interior da mitocôndria.[3]
Nas neurónios, as adenilato ciclases sensíveis ao cálcio estão localizadas perto de canais iónicos de cálcio para poderem reagir rapidamente ao fluxo de entrada de Ca2+; suspeita-se que desempenham um papel importante no processo de aprendizagem.
AC de classe IV
As AC-IV foram encontradas primeiro na bactéria Aeromonas hydrophila, e posteriormente foi descrita a estrutura da AC-IV de Yersinia pestis. Estas são as mais pequenas de todas as classes de enzimas AC; a AC-IV de Yersinia é um dímero de subunidades de apenas 19 kDa sem componentes reguladores conhecidos.
ACs de classes V e VI
Estas formas de adenilato ciclase foram encontradas em espécies concretas de bactérias, nomeadamente a Prevotella ruminicola e a Rhizobium etli, respetivamente, e ainda não estão caraterizadas em detalhe.
Referências
- ↑ Reece J, Campbell N (2002). Biology. San Francisco: Benjamin Cummings. 207 páginas. ISBN 0-8053-6624-5
- ↑ Schröder-Lang S, Schwärzel M, Seifert R, Strünker T, Kateriya S, Looser J, Watanabe M, Kaupp UB, Hegemann P, Nagel G (Janeiro de 2007). «Fast manipulation of cellular cAMP level by light in vivo». Nat. Methods. 4 (1): 39–42. PMID 17128267. doi:10.1038/nmeth975
- ↑ Acin-Perez R, Salazar E, Kamenetsky M, Buck J, Levin LR, Manfredi G (Março de 2009). «Cyclic AMP produced inside mitochondria regulates oxidative phosphorylation». Cell Metab. 9 (3): 265–76. PMC 2684673
 . PMID 19254571. doi:10.1016/j.cmet.2009.01.012
. PMID 19254571. doi:10.1016/j.cmet.2009.01.012