AMPA
AMPA
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||
| Nomes | |||||||||||||||||
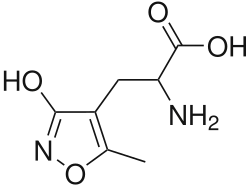
| Nome IUPAC | 2-Amino-3-(3-hydroxy-5-methyl-isoxazol-4-yl)propanoic acid | ||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| Página de dados suplementares | |||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||
O ácido α-amino-3-hidróxi-5-metil-4-isoxazol propiônico, mais conhecido como AMPA, é um composto químico que atua como um agonista específico sintético seletivo de receptores ionotrópicos do tipo receptor AMPA (AMPAR), mimetizando os efeitos do neurotransmissor glutamato.[1][2]
Existem vários tipos de canais iônicos glutamatérgicos no sistema nervoso central, incluindo AMPA, ácido kainico e ácido N-metil-D-aspártico (NMDA). Na sinapse, esses receptores atendem a propósitos distintos. O AMPA pode ser usado experimentalmente para distinguir a atividade de um receptor do outro, a fim de compreender a diferença de suas funções.[3] O AMPA gera potenciais pós-sinápticos excitatórios (EPSP) rapidamente.[1] AMPA ativa receptores AMPAR, sendo canais catiônicos não seletivos, permitindo a passagem de sódio (Na+) e potássio (K+) e, portanto, apresentam um potencial de equilíbrio próximo de 0 mV.[4]
O AMPA foi sintetizado pela primeira vez, juntamente com diversos outros derivados do ácido ibotênico, por Krogsgaard-Larsen, Honoré e colaboradores, visando distinguir farmacologicamente os receptores sensíveis ao glutamato daquelas sensíveis ao aspartato.[5] AMPA é utilizado em pesquisas em neurociência para estudar os mecanismos de excitação glutamatérgica.[6][7]
Ototoxicidade
A administração exógena de AMPA em modelos experimentais simula a ativação excessiva desses receptores, permitindo a investigação dos efeitos da excitotoxicidade coclear.[8] Esse processo patológico é desencadeado pelo acúmulo extracelular de glutamato e ativação prolongada de receptores AMPA e NMDA. A base para essa abordagem é a expressão de receptores AMPA nas sinapses entre as células ciliadas internas e as fibras aferentes do nervo vestibulococlear (nervo auditivo), sendo fundamentais para a transmissão de sinais auditivos.[6] Essa hiperestimulação resulta na entrada descontrolada de íons sódio (Na⁺) e cálcio (Ca²⁺) nos neurônios pós-sinápticos, sobrecarregando as mitocôndrias, promovendo a produção de espécies reativas de oxigênio e desencadeando vias de apoptose.[8][9]
A subunidade GluR2 (GRIA2) dos receptores AMPA exerce papel crucial na regulação da permeabilidade ao cálcio, sua presença impede a entrada excessiva de Ca²⁺, protegendo contra danos induzidos por glutamato.[10][11] Estudos evidenciaram que a ausência ou subregulação de GluR2 pode aumentar a vulnerabilidade das células neurais à excitotoxicidade, tanto em modelos auditivos quanto no sistema nervoso central mais amplo.[12][13]
Estudos experimentais demonstram que a exposição coclear a AMPA causa perda sináptica e neurodegeneração em fibras auditivas, efeitos semelhantes aos observados após trauma acústico ou administração de ototóxicos como cisplatina e aminoglicosídeos.[11][12] Tais agentes podem aumentar a liberação de glutamato ou sensibilizar receptores ionotrópicos, amplificando o risco de excitotoxicidade coclear.[14]
Alguns compostos com ação sobre os receptores AMPA, como os moduladores alostéricos positivos que potencializam a transmissão sináptica mediada por AMPA pela regulação positiva da transmissão sináptica sem causar excitotoxicidade direta.[6] A farmacologia coclear dos moduladores AMPA também é estudada com foco na contribuição dos TARPs (Proteínas Regulatórias Transmembrana dos Receptores AMPA), que regulam a atividade e a farmacodinâmica desses receptores.[6]
Derivados de sulfonamidas e compostos como a deoxissizandrina a apresentam ação sobre o sistema nervoso central também oferecem novas perspectivas para agentes que possam atuar seletivamente sobre subtipos de receptores glutamatérgicos, como os AMPA, contribuindo para a prevenção de desfechos neurotóxicos associados a condições ototóxicas.[7][14]
Ver também
Referências
- ↑ a b Purves, Dale; George J. Augustine; David Fitzpatrick; William C. Hall; Anthony-Samuel LaMantia; James O. McNamara (2008). Neuroscience 4th ed. [S.l.]: Sinauer Associates. pp. 128–33. ISBN 978-0-87893-697-7
- ↑ Puel, Jean-Luc; Ruel, Jérôme; dʼAldin, Christine Gervais; Pujol, Rémy (junho de 1998). «Excitotoxicity and repair of cochlear synapses after noise-trauma induced hearing loss:». NeuroReport (em inglês) (9): 2109–2114. ISSN 0959-4965. doi:10.1097/00001756-199806220-00037. Consultado em 8 de agosto de 2025
- ↑ Dinh, L; Nguyen T; Salgado H; Atzori M (2009). «Norepinephrine homogeneously inhibits alpha-amino-3-hydroxyl-5-methyl-4-isoxazole-propionate- (AMPAR-) mediated currents in all layers of the temporal cortex of the rat». Neurochem Res. 34 (11): 1896–906. PMID 19357950. doi:10.1007/s11064-009-9966-z
- ↑ Midgett, Charles R.; Madden, Dean R. (outubro de 2008). «The Quaternary Structure of a Calcium-Permeable AMPA Receptor: Conservation of Shape and Symmetry across Functionally Distinct Subunit Assemblies». Journal of Molecular Biology (em inglês) (3): 578–584. doi:10.1016/j.jmb.2008.07.021. Consultado em 8 de agosto de 2025
- ↑ Krogsgaard-Larsen, P; Honore T; Hansen JJ; Curtis DR; Lodge D (1980). «New class of glutamate agonist structurally related to ibotenic acid». Nature. 284 (5751): 64–66. Bibcode:1980Natur.284...64K. PMID 6101908. doi:10.1038/284064a0
- ↑ a b c d Radin, Daniel P.; Li, Yong-Xin; Rogers, Gary; Purcell, Richard; Lippa, Arnold (agosto de 2018). «Tarps differentially affect the pharmacology of ampakines». Biochemical Pharmacology (em inglês): 446–451. doi:10.1016/j.bcp.2018.06.013. Consultado em 8 de agosto de 2025
- ↑ a b Blicharz-Futera, Klaudia; Kamiński, Michał; Grychowska, Katarzyna; Canale, Vittorio; Zajdel, Paweł (março de 2025). «Current development in sulfonamide derivatives to enable CNS-drug discovery». Bioorganic Chemistry (em inglês). 108076 páginas. doi:10.1016/j.bioorg.2024.108076. Consultado em 8 de agosto de 2025
- ↑ a b Isaac, John T.R.; Ashby, Michael C.; McBain, Chris J. (junho de 2007). «The Role of the GluR2 Subunit in AMPA Receptor Function and Synaptic Plasticity». Neuron (em inglês) (6): 859–871. doi:10.1016/j.neuron.2007.06.001. Consultado em 8 de agosto de 2025
- ↑ Kim, Hyung-Jin; Lee, Jeong-Han; Kim, Se-Jin; Oh, Gi Su; Moon, Hae-Dalma; Kwon, Kang-Beom; Park, Channy; Park, Byung Hyun; Lee, Ho-Kyun (17 de março de 2010). «Roles of NADPH Oxidases in Cisplatin-Induced Reactive Oxygen Species Generation and Ototoxicity». Journal of Neuroscience (em inglês) (11): 3933–3946. ISSN 0270-6474. PMID 20237264. doi:10.1523/JNEUROSCI.6054-09.2010. Consultado em 8 de agosto de 2025
- ↑ Sheng, Morgan; Lee, Sang Hyoung (junho de 2001). «AMPA Receptor Trafficking and the Control of Synaptic Transmission». Cell (em inglês) (7): 825–828. doi:10.1016/S0092-8674(01)00406-8. Consultado em 8 de agosto de 2025
- ↑ a b Bie, Bihua; Brown, David L.; Naguib, Mohamed (fevereiro de 2011). «Increased synaptic GluR1 subunits in the anterior cingulate cortex of rats with peripheral inflammation». European Journal of Pharmacology (em inglês) (1-3): 26–31. doi:10.1016/j.ejphar.2010.11.027. Consultado em 8 de agosto de 2025
- ↑ a b Qneibi, Mohammad; Bdir, Sosana; Bdair, Mohammad; Aldwaik, Samia Ammar; Sandouka, Dana; Heeh, Maram; Idais, Tala Iyad (fevereiro de 2024). «AMPA receptor neurotransmission and therapeutic applications: A comprehensive review of their multifaceted modulation». European Journal of Medicinal Chemistry (em inglês). 116151 páginas. doi:10.1016/j.ejmech.2024.116151. Consultado em 8 de agosto de 2025
- ↑ Salussolia, Catherine L.; Wollmuth, Lonnie P. (novembro de 2012). «Flip-Flopping to the Membrane». Neuron (em inglês) (3): 463–465. PMC 4292898
 . PMID 23141057. doi:10.1016/j.neuron.2012.10.022. Consultado em 8 de agosto de 2025
. PMID 23141057. doi:10.1016/j.neuron.2012.10.022. Consultado em 8 de agosto de 2025
- ↑ a b Yan, Tingxu; Xu, Mengjie; Wan, Shutong; Wu, Bo; Xiao, Feng; Bi, Kaishun; Jia, Ying (dezembro de 2018). «Deoxyschizandrin attenuates Aβ1–42-induced cognitive impairments through up-regulation of AMPA receptors in mice». Phytochemistry Letters (em inglês): 24–31. doi:10.1016/j.phytol.2018.09.009. Consultado em 8 de agosto de 2025