5-Metil-MDA
5-Metil-MDA
| |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||
| Nomes | |||||||||||
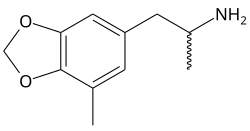
| Nome IUPAC | 1-(7-metil-1,3-benzodioxol-5-il)propan-2-amina | ||||||||||
| |||||||||||
| |||||||||||
| |||||||||||
| Página de dados suplementares | |||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||
5-Metil-MDA, também conhecida como 5-metil-3,4-metilenodioxianfetamina (5-Me-MDA), é uma droga sintética entactógena e psicodélica da classe das anfetaminas. É um homólogo metilado no anel aromático do MDA, configurando um isômero estrutural do MDMA.[1]
Farmacologia
O 5-metil-MDA atua como um agente de liberação de serotonina (SSRA) com valores de IC50 de 107 nM, 11.600 nM e 1.494 nM para a liberação de serotonina, dopamina e noradrenalina, respectivamente (quanto menor o número, maior a afinidade de ligação).[1]
2-metil-MDA e 5-metil-MDA foram usados para ajudar a orientar a modelagem computacional do complexo transportador de serotonina.[2]
Sociedade e cultura
Legalidade
Internacional
O 5-metil-MDA não está listado pela Convenção das Nações Unidas sobre Substâncias Psicotrópicas.[3]
Estados Unidos
O 5-metil-MDA não está explicitamente listado a nível federal nos Estados Unidos,[4] no entanto, o 5-metil-MDA é um isómero estrutural do MDMA, portanto sua venda ou posse podem ser alvo de processos ao abrigo da Lei Federal de Análogos [en].[5]
Ver também
Referências
- ↑ a b Parker MA, Marona-Lewicka D, Kurrasch D, Shulgin AT, Nichols DE (março de 1998). «Synthesis and pharmacological evaluation of ring-methylated derivatives of 3,4-(methylenedioxy)amphetamine (MDA)». Journal of Medicinal Chemistry. 41 (6): 1001–5. PMID 9526575. doi:10.1021/jm9705925
- ↑ Walline CC, Nichols DE, Carroll FI, Barker EL (junho de 2008). «Comparative molecular field analysis using selectivity fields reveals residues in the third transmembrane helix of the serotonin transporter associated with substrate and antagonist recognition». The Journal of Pharmacology and Experimental Therapeutics. 325 (3): 791–800. PMC 2637348
 . PMID 18354055. doi:10.1124/jpet.108.136200
. PMID 18354055. doi:10.1124/jpet.108.136200
- ↑ «Convention on Psychotropic Substances, 1971». Consultado em 9 de junho de 2016. Arquivado do original em 19 de janeiro de 2022
- ↑ «§1308.11 Schedule I.». Consultado em 9 de junho de 2016. Arquivado do original em 27 de agosto de 2009
- ↑ «Erowid Analog Law Vault : Federal Controlled Substance Analogue Act Summary». www.erowid.org. Consultado em 17 de novembro de 2025. Cópia arquivada em 6 de setembro de 2025