2-Mercaptoetanol
2-Mercaptoetanol
| |
|---|---|
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
O 2-mercaptoetanol (também denominado β-mercaptoetanol, BME, 2BME, 2-ME ou β-met) é o composto químico com a fórmula HOCH2CH2SH. O ME ou βME, como se costuma abreviar, utiliza-se para reduzir pontes disulfeto e pode actuar como um antioxidante biológico ao agir contra radicais hidroxilo (entre outros). Utiliza-se muito porque o grupo hidroxilo proporciona solubilidade em água e diminui a volatilidade. Devido à sua pressão de vapor reduzida, o seu desagradável cheiro é menos rejeitavel que o de outros tióis relacionados.
Preparação
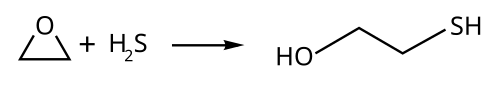
O 2-mercaptoetanol pode ser preparado pela acção do sulfeto de hidrogénio sobre o óxido de etileno:[1]
Reacções
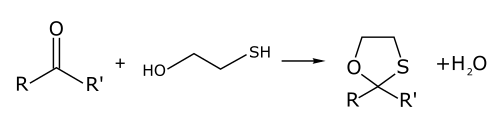
O 2-mercaptoetanol reage com aldeído e cetonas para dar os correspondentes oxatiolanos. Por esta razão o 2-mercaptoetanol é útil como grupo protector.[2]
Aplicações
Redução de proteínas
Algumas proteínas podem ser desnaturalizadas pelo 2-mercaptoetanol, o qual cliva as ligações dissulfeto que se podem formar entre os grupos tiol de resíduos de cisteína. No caso de haver um excesso de 2-mercaptoetanol, o seguinte equilíbrio fica deslocado à direita:
- RS–SR + 2 HOCH2CH2SH
 HOCH2CH2S–SCH2CH2OH + 2 RSH
HOCH2CH2S–SCH2CH2OH + 2 RSH
Ao romperem a ligações S-S presentes em algumas proteínas, podem ser alteradas tanto a sua estrutura terciaria como a quaternária. Dada a sua capacidade de alterar a estrutura das proteínas, foi utilizado na análise de proteínas, por exemplo, para assegurar que uma solução de proteínas contém moléculas de proteínas monoméricas, em vez de dímeros proteicos ligados por ligações dissulfeto ou oligómeros de maior ordem. Porém, como o 2-mercaptoetanol forma adutos com cisteínas livres e é algo tóxico, é mais comummente utilizado o ditiotreitol (DTT) especialmente em SDS-PAGE. O DTT é também um agente redutor mais poderoso com um potencial redox (a pH 7) de −0,33 V, comparado com o −0.26 V do 2-mercaptoetanol.[3][4]
O 2-mercaptoetanol costuma ser utilizado em vez do ditiotreitol (DTT) ou o composto inodoro tris(2-carboxietil)fosfina (TCEP) em aplicações biológicas.
Ainda que o 2-mercaptoetanol possua uma maior volatilidade que o DTT, é mais estável: a vida média do 2-mercaptoetanol é de mais de 100 horas a pH 6,5 e de 4 horas a pH 8,5; a vida média do DTT é de 40 horas a pH 6,5 e de 1,5 horas a pH 8,5.[5][6]
Prevenção da oxidação de proteínas
O 2-mercaptoetanol e agentes redutores relacionados (p. ex., DTT) são frequentemente incluídos em reações enzimáticas para inibir a oxidação de resíduos sulfidrila livres, mantendo assim a atividade proteica. É utilizado em diversos ensaios enzimáticos como tampão padrão.
Desnaturalização de ribonucleases
O 2-mercaptoetanol utiliza em alguns procedimentos de isolamento de ARN para eliminar ribonucleases liberadas durante a lise celular. As numerosas ligações dissulfeto que possuem as ribonucleases fazem com que sejam enzimas muito estáveis, e o 2-mercaptoetanol é utilizado para reduzir as ditas ligações e desnaturalizar irreversivelmente as proteínas. Isto impede que as ribonucleases digiram o ARN durante o seu procedimento de extração.[7]
Segurança
O 2-mercaptoetanol é considerado tóxico, causando irritação nas vias nasais e no trato respiratório se inalado, irritando também a pele e, se ingerido, causando vómitos e dor de estômago e potencialmente morte se houver exposição grave.[8]
Notas
- ↑ Knight, J. J. (2004) "2-Mercaptoethanol" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette), J. Wiley & Sons, New York. doi:10.1002/047084289.
- ↑ «1,3-Dithiolanes, 1,3-Dithianes». Organic Chemistry Portal. Consultado em 27 de maio de 2008. Cópia arquivada em 17 de maio de 2008
- ↑ «Copia arquivada». Chemicalland21.com. Consultado em 15 de março de 2018. Arquivado do original em 23 de julho de 2013
- ↑ Aitken CE (2008). «An oxygen scavenging system for improvement of dye stability in single-molecule fluorescence experiments». Biophys J. 94 (5): 1826–35. PMC 2242739
 . PMID 17921203. doi:10.1529/biophysj.107.117689
. PMID 17921203. doi:10.1529/biophysj.107.117689
- ↑ Yeh, J. I. (2009) "Additives and microcalorimetric approaches for optimization of crystallization" in Protein Crystallization, 2nd Edition (Ed: T. Bergfors), International University Line, La Jolla, CA. ISBN 978-0-9720774-4-6.
- ↑ Stevens R. (1983). «The Stabilities of Various Thiol Compounds used in Protein Purifications». Biochemical Education. 11 (2): 70. doi:10.1016/0307-4412(83)90048-1
- ↑ Nelson, David R.; Lehninger, Albert L; Cox, Michael. Lehninger principles of biochemistry. [S.l.]: W.H. Freeman. ISBN 0-7167-4339-6
- ↑ «Material Safety Data Sheet». JT Baker. Consultado em 31 de julho de 2011. Arquivado do original em 3 de março de 2016