1,1'-Bi-2-naftol
1,1'-Bi-2-naftol
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
-BINOL.svg.png) | |||||||||||||
 | |||||||||||||
| Nomes | |||||||||||||
| Nome IUPAC | 1,1'-Binaftaleno-2,2'-diol | ||||||||||||
| Outros nomes | 1,1'-Bi-2-naftol 1,1-Binaftol BINOL | ||||||||||||
| |||||||||||||
| |||||||||||||
| Página de dados suplementares | |||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||
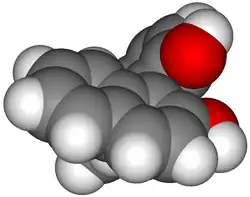
BINOL (bifenilnaftol ou 1,1'-Bi-2-naftol) é um composto orgânico freqüentemente usado como um ligante para síntese assimétrica catalisada por metais de transição. A molécula BINOL apresenta quiralidade axial forma por isso dois enantiômeros diferentes (R, S) que são opticamente ativos. Estes podem ser separados facilmente, sendo estáveis quanto à racemização. A rotação específica dos dois enantiômeros é +/- 3,5° (c=1 em THF).
BINOL é também precursor de outro ligante quiral proeminente chamado BINAP (bifenilfosfina).[1]
Preparação
A preparação de uma mistura racêmica de BINOL não apresenta dificuldades excepconais, sendo difícil no entanto, a obtenção direta dos enantiomêros individualmente.
Preparação do produto racêmico
Pode ser produzido por exemplo a partir de 2-naftol e usando-se cloreto de ferro (III) como oxidante. O mecanismo de formação envolve complexação do Fe3+ pelas hidroxilas, seguido de uma reação de ligação de radicais dos anéis de naftol desencadeada pelo Fe-(III), que se oxida a Fe-(II).
Preparação dos enantiomeros
Por síntese direta
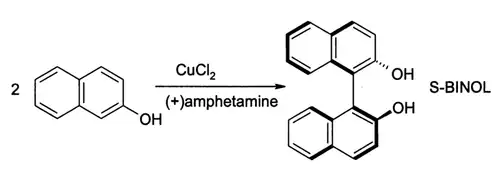
(S)-BINOL pode ser sintetizado diretamente de uma ligação oxidativa assimétrica de 2-naftol com cloreto de cobre(II). O ligante quiral usado nesta reação é a (+)-anfetamina.
Por resolução racêmica
BINOL reage com cloreto de pentanoíla para formar um componente di-éster. A enzima colesterol esterase é adicionada na forma de pó-de-acetona de pâncreas bovino, que tem capacidade de hidrolisar o (S)-di-éster mas não o (R)-di-éster.[2] O (R)-dipentanoato é hidrolisado em uma segunda etapa metóxido de sódio.[3]
A molécula opticamente ativa também pode ser obtida por cristalização enatiomérica. Em um método, o alcalóide cloreto de N-benzylcinchonidinium formaria um composto de inclusão cristalino. O composto de inclusão do enantiômero S é solúvel em acetonitrila mas o do enantiômero R não.[2]
Referências
- ↑ "Binap: An industrial approach to manufacture"
- ↑ a b "RESOLUTION OF 1,1'-BI-2-NAPHTHOL", Dongwei Cai, David L. Hughes, Thomas R. Verhoeven, and Paul J. Reider, Coll. Vol. 10, p.93; Vol. 76, p.1
- ↑ "(S)-(−)- AND (R)-(+)-1,1'-BI-2-NAPHTHOL", Romas J. Kazlauskas in organic Syntheses, Coll. Vol. 9, p.77; Vol. 70, p.60