Óxido de césio
Óxido de césio</ref>[1]
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
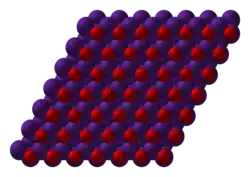 | |||||||||||||||
| Nomes | |||||||||||||||
| Nome IUPAC | Caesium oxide | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
Óxido de césio (nome IUPAC) descreve compostos inorgânicos compostos de césio e oxigênio. Os seguintes óxidos de césio binários (contendo somente Cs e O) são conhecidos: Cs11O3, Cs4O, Cs7O e Cs2O.[3]
Cs2O é higroscópico, formando o hidróxido corrosivo CsOH em contato com água.
Referências
- ↑ .
- ↑ a b Caesiumoxid bei webelements.com.
- ↑ Simon, A. (1997), «Group 1 and 2 Suboxides and Subnitrides — Metals with Atomic Size Holes and Tunnels», Coord. Chem. Rev., 163: 253–270, doi:10.1016/S0010-8545(97)00013-1.