Ácido vulpínico
Ácido vulpínico
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
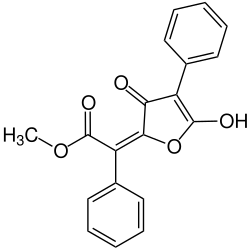 Estrutura química do ácido vulpínico
| |||||||||||||
 | |||||||||||||
| Nomes | |||||||||||||
| Nome IUPAC | Metil (‘'E’')-(5-hidroxi-3-oxo-4-fenilfurano-2(3'‘H’')-ilideno)fenilacetato | ||||||||||||
| |||||||||||||
| |||||||||||||
| Página de dados suplementares | |||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||
Ácido vulpínico é um produto natural importante na simbiose que fundamenta a biologia dos líquenes.[1] Trata-se de um derivado simples na forma de éster metílico de seu composto precursor, o ácido pulvínico [en], e é quimicamente próximo das pulvinonas [en], ambos originados de aminoácidos aromáticos como a fenilalanina por meio do metabolismo secundário [en]. As funções do ácido vulpínico ainda não estão totalmente estabelecidas, mas podem incluir propriedades que o tornam um inibidor alimentar para herbívoros. O composto é relativamente tóxico para mamíferos.
Descrição química
O ácido vulpínico foi isolado pela primeira vez a partir de líquenes em 1925.[2] Como substância isolada e purificada, apresenta coloração amarelo-vivo.[3]
O ácido vulpínico é derivado biossinteticamente por esterificação a partir do ácido pulvínico;[4] o próprio ácido pulvínico origina-se dos aminoácidos aromáticos fenilalanina e tirosina, por meio de dimerização [en] e clivagem oxidativa do anel de ácidos arilpirúvicos, processo que também gera as pulvinonas relacionadas.[5]
Diversas sínteses orgânicas do ácido vulpínico já foram relatadas. Em uma delas, butenolidas [en] foram funcionalizadas de maneira eficiente por reações de acoplamento Suzuki por meio dos correspondentes triflatos [en] de enol.[6]
Ocorrência em líquenes

O ácido pulvínico é encontrado em diversas espécies de líquen, bem como em alguns fungos não liquenizados.[2] Foi identificado no fungo boleto Pulveroboletus ravenelii.[8][5] Em 2016, um novo grupo de basidiomicetos, distinto do parceiro fúngico liquênico tradicionalmente conhecido, foi implicado na produção de ácido vulpínico.[1]
Bioatividades
O ácido vulpínico é relativamente tóxico para mamíferos carnívoros, bem como para insetos e moluscos. Entretanto, não apresenta toxicidade significativa para coelhos e camundongos. Uma possível função biológica do ácido vulpínico é atuar como repelente desenvolvido pelos líquenes para impedir que os herbívoros os comessem.[9] Os líquenes também podem explorar as propriedades de bloqueio de radiação ultravioleta da molécula, protegendo os fotobiontes subjacentes.[10] Por exemplo, acredita-se que o ácido vulpínico funcione como um filtro de luz azul em Letharia vulpina [en].[11] Estudos anteriores demonstraram que o composto pode proteger queratinócitos humanos em cultura de tecidos contra danos induzidos por radiação ultravioleta B.[12]
Os seres humanos já exploraram sua toxicidade para mamíferos, utilizando líquenes que contêm grandes quantidades da substância (como Letharia vulpina) para envenenar lobos na Escandinávia, às vezes adicionando-os a iscas contendo sangue de rena e vidro.[3]
O ácido vulpínico apresenta certa atividade antibiótica contra bactérias gram-positivas e demonstrou ser capaz de interferir na divisão celular de MRSA.[13][14]
Ver também
Referências
- ↑ a b Spribille T, Tuovinen V, Resl P, Vanderpool D, Wolinski H, Aime MC, et al. (2016). «Basidiomycete yeasts in the cortex of ascomycete macrolichens». Science. 353 (6298): 488–492. Bibcode:2016Sci...353..488S. PMC 5793994
 . PMID 27445309. doi:10.1126/science.aaf8287
. PMID 27445309. doi:10.1126/science.aaf8287
- ↑ a b Mazza, Franc Paolo (1925). «Constitution and physical properties of vulpinic acid». Rendiconto dell'Accademia delle Scienze Napoli. 31: 182–190
- ↑ a b Brodo, Irwin M.; Sharnoff, Sylvia Duran; Sharnoff, Stephen (2001). Lichens of North America. [S.l.]: Yale University Press. p. 83. ISBN 978-0300082494
- ↑ Crout, D.H.G. (2012). «The Biosynthesis of Carbocyclic Compounds». In: Lloyd, D. Carbocyclic Chemistry. One. [S.l.]: Springer Science & Business Media. pp. 63–198, esp. 147. ISBN 9781468482706. Consultado em 3 de janeiro de 2020
- ↑ a b Gill, M.; Steglich, W. (1987). «Pigments of Fungi (Macromycetes)». Fortschritte der Chemie organischer Naturstoffe / Progress in the Chemistry of Organic Natural Products. 51. [S.l.: s.n.] pp. 1–297. ISBN 978-3-7091-7456-2. PMID 3315906. doi:10.1007/978-3-7091-6971-1_1
- ↑ Ahmed, Zafar; Langer, Peter (2004). «Suzuki cross-coupling reactions of γ-alkylidenebutenolides: application to the synthesis of vulpinic acid». Journal of Organic Chemistry. 69 (11): 3753–3757. PMID 15153005. doi:10.1021/jo049780a
- ↑ Galun, Margalith (1988). CRC Handbook of Lichenology, Volume III. Boca Raton: CRC. pp. 98–99. ISBN 0-8493-3583-3
- ↑ Duncan, Christine J.G.; Cuendet, Muriel; Fronczek, Frank R.; Pezzuto, John M.; Mehta, Rajendra G.; Hamann, Mark T.; Ross, Samir A. (2003). «Chemical and biological investigation of the fungus Pulveroboletus ravenelii». Journal of Natural Products. 66 (1): 103–107. Bibcode:2003JNAtP..66..103D. PMC 4969011
 . PMID 12542354. doi:10.1021/np0203990
. PMID 12542354. doi:10.1021/np0203990
- ↑ Nash, Thomas H. (1996). Lichen Biology. [S.l.]: Cambridge University Press. p. 179. ISBN 978-0-521-45974-7
- ↑ Legouin, Béatrice; Lohézic-Le Dévéhat, Françoise; Ferron, Solenn; Rouaud, Isabelle; Le Pogam, Pierre; Cornevin, Laurence; Bertrand, Michel; Boustie, Joël (2017). «Specialized metabolites of the lichen Vulpicida pinastri act as photoprotective agents». Molecules. 22 (7). 1162 páginas. PMC 6152234
 . PMID 28704942. doi:10.3390/molecules22071162
. PMID 28704942. doi:10.3390/molecules22071162
- ↑ Phinney, Nathan H.; Gauslaa, Yngvar; Solhaug, Knut Asbjørn (2018). «Why chartreuse? The pigment vulpinic acid screens blue light in the lichen Letharia vulpina». Planta. 249 (3): 709–718. PMID 30374913. doi:10.1007/s00425-018-3034-3
- ↑ Varol, Mehmet; Türk, Ayşen; Candan, Mehmet; Tay, Turgay; Koparal, Ayşe Tansu (2016). «Photoprotective activity of vulpinic and gyrophoric acids toward ultraviolet B-induced damage in human keratinocytes». Phytotherapy Research. 30 (1): 9–15. PMID 26463741. doi:10.1002/ptr.5493
- ↑ Bačkor M, Hudá J, Repčák M, Ziegler W, Bačkorová M (1998). «The Influence of pH and Lichen Metabolites (Vulpinic Acid and (+)-Usnic Acid) on the Growth of the Lichen Photobiont Trebouxia irregularis». The Lichenologist. 30 (6): 577–582. doi:10.1017/S0024282992000574
- ↑ Shrestha G, Thompson A, Robison R, St Clair LL (28 de abril de 2015). «Letharia vulpina, a vulpinic acid containing lichen, targets cell membrane and cell division processes in methicillin-resistant Staphylococcus aureus». Pharmaceutical Biology. 54 (3): 413–8. PMID 25919857. doi:10.3109/13880209.2015.1038754