Ácido ortocarbônico
Ácido ortocarbônico
| |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||
| Nomes | |||||||||||
| Nome IUPAC | ácido ortocarbônico | ||||||||||
| Nome sistemático | Metanotetrol[1] | ||||||||||
| |||||||||||
| |||||||||||
| Página de dados suplementares | |||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||
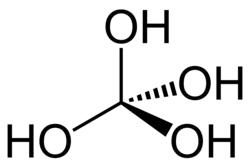
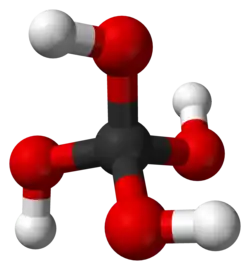
Ácido ortocarbônico (metanotetrol) é o composto hipotético de fórmula H4CO4 ou C(OH)4. Sua estrutura consiste em único átomo de carbono ligado a quatro grupos hidroxila (OH). Na teoria, poderia perder quatro prótons para dar origem ao hipotético ânion
CO4−
4 (ortocarbonato), sendo, portanto, considerado um oxiácido de carbono.
O composto possuiria alta instabilidade e rapidamente haveria sua decomposição em ácido carbônico, segundo a reação:[2][3]
- H4CO4 → H2CO3 + H2O.
O ácido Ortocarbônico é do grupo de ácidos orto-carboxílicos, que têm a estrutura geral RC(OH)3. O termo "ácido orto" também é usado para se referir ao ácido mais hidroxilado em um conjunto de oxoácidos. Seu desenho molecular se assemelha a uma suástica e, portanto, tem sido chamado de "ácido de Hitler".[4]
Pesquisadores do Instituto de Física e Tecnologia de Moscou acreditam que o ácido ortocarbônico seja estável em alta pressão, podendo formar-se no interior dos planetas, como em Netuno e Urano.[4][5]
Ânions
Com a perda de prótons, ele pode reduzir-se em quatro ânions:
H3CO−
4,
H2CO2−
4,
HCO3−
4 e
CO4−
4.
Os sais destes ânions nunca foram observados, mas estudos teóricos de 2002, apontam que o Na4CO4 seja estável.[6]
Esteres de ortocarbonato
A fração tetravalente CO4 é encontrada em compostos orgânicos estáveis; eles são formalmente esteres do ácido ortocarbônico e, portanto, são chamados de ortocarbonatos. Por exemplo, o tetraetoximetano pode ser preparado pela reação entre cloropicrina e etóxido de sódio em etanol.[7] O trinitroetilortocarbonato possui um núcleo de ortocarbonato.
Referências
- ↑ «Methanetetrol - PubChem Public Chemical Database». The PubChem Project. USA: National Center for Biotechnology Information
- ↑ Bohm S.; Antipova D.; Kuthan J. (1997). «A Study of Methanetetraol Dehydration to Carbonic Acid». International Journal of Quantum Chemistry. 62: 315–322. doi:10.1002/(SICI)1097-461X(1997)62:3<315::AID-QUA10>3.3.CO;2-N
- ↑ Carboxylic Acids and Derivatives IUPAC Recommendations on Organic & Biochemical Nomenclature
- ↑ a b GRAY, Richard (7 de setembro de 2016). «Weird materials like 'Hitler's Acid' hide inside Neptune and Uranus». Dailymail. Consultado em 22 de dezembro de 2017
- ↑ G. Saleh; A. R. Oganov (2016). «Novel Stable Compounds in the C-H-O Ternary System at High Pressure». Scientific Reports. doi:10.1038/srep32486
- ↑ Al-Shemali Musstafa; Boldyre Alexander I (2002). «Search for Ionic Orthocarbonates: Ab Initio Study of Na4CO4». J. Phys. Chem. A. 106 (38): 8951–8954. doi:10.1021/jp020207+
- ↑ Orthocarbonic acid, tetraethyl ester Organic Syntheses, Coll. Vol. 4, p.457 (1963); Vol. 32, p.68 (1952)