Ácido nitroacético
Ácido nitroacético
| |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Nomes | |||||||||
| Nome IUPAC | 2-Nitroacetic acid | ||||||||
| Outros nomes | Nitroacetato | ||||||||
| |||||||||
| |||||||||
| |||||||||
| Página de dados suplementares | |||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||
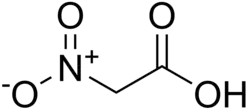
Ácido nitroacético é o composto químico com a fórmula (NO2)CH2CO2H. Este ácido carboxílico substituído é usado como um potential precursor do nitrometano, comumente usado como um combustível em dragsters e como um reagente orgânico em síntese química.
Síntese
Ácido nitroacético pode ser sintetizado pela adição de ácido cloroacético frio em uma solução aquosa levemente alcalina fria, seguido pela mistura com solução de nitrito de sódio aquosa. É importante durante este procedimento não tornar a solução muito alcalina e mantê-la fria para evitar a formação de glicolato de sódio.
Reações
Ácido nitroacético pode ser usado na produção de nitrometano pelo aquecimento de um sal correspondente para descarboxilação a 80 °C.[2]
Referências
- ↑ Dippy, J.F.J., Hughes, S.R.C., Rozanski, A., J. Chem. Soc., 1959, 2492.
- ↑ Organic Syntheses, Coll. Vol. 1, p.401 (1941); Vol. 3, p.83 (1923)