Ácido isovalérico
3-Methylbutanoic acid
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||
| Nomes | |||||||||||||||
| Nome IUPAC | 3-Methylbutanoic acid | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
3-Methylbutanoic acid
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||
| Nomes | |||||||||||||||
| Nome IUPAC | 3-Methylbutanoic acid | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
O ácido isovalérico, também chamado ácido 3-metilbutanoico ou ácido β-metilbutírico, é um composto orgânico com a fórmula (CH3)2CHCH2CO2H. É por vezes classificado como ácido gordo de cadeia curta.[3] É um líquido incolor que é moderadamente solúvel em água, mas muito solúvel na maioria dos solventes orgânicos. O ácido 3-metilbutanoico é um composto que se encontra na natureza e pode ser encontrado em muitos produtos alimentares, como o queijo, leite de soja e sumo de maçã.
O ácido isovalérico tem um cheiro forte pungente a queijo ou doce e os seus ésteres voláteis são amplamente usados em perfumaria. Propôs-se que é o agente anticonvulsivo da valeriana.[4] É o responsável principal pela causa do intenso cheiro a pés que produzem as bactérias da pele que metabolizam a leucina.[5]
O ácido isovalérico é considerado a causa primária dos aromas que adicionam ao vinho os levedos Brettanomyces.[6] Outros compostos produzidos por Brettanomyces são o 4-etilfenol, o 4-vinilfenol e o 4-etilguaiacol.[7] Um excesso de ácido isovalérico no vinho costuma ser considerado um defeito,[7] já que pode fazer com que cheire a suor, a couro ou como um estábulo, mas em pequenas quantidades pode parecer um odor fumado, especiado ou medicinal.[6] Estes fenómenos podem ser impedidos matando os levedos Brettanomyces por meio de filtração estéril, ou por adição de quantidades relativamente grandes de dióxido de enxofre e às vezes de ácido sórbico, ou misturando-o com bebidas alcoólicas fortes para originar um vinho fortificado com força suficiente para matar todos os levedos e bactérias, ou por pasteurização. O ácido isovalérico pode ser encontrado também na cerveja, e, exceto nalgumas cervejas ale de estilo inglês, é considerado um defeito.[8] Pode ser produzido pela oxidação de resinas de lúpulo ou pelos levedos Brettanomyces presentes.[8]
Usos
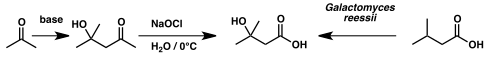
O ácido isovalérico foi utilizado para sintetizar o ácido β-hidroxi-isovalérico (também chamado ácido β-hidroxi β-metilbutírico) por oxidação microbiana feita pelo fungo Galactomyces reessii.[9]
Referências
- ↑ Solubility of isovaleric acid in methanol
- ↑ Solubility of isovaleric acid in methanol
- ↑ Pubchem Isolaveric acid
- ↑ Eadie, Mervyn J. (novembro de 2004). «Could Valerian Have Been the First Anticonvulsant?». Epilepsia. 45 (11): 1338–1343. PMID 15509234. doi:10.1111/j.0013-9580.2004.27904.x
- ↑ Ara, Katsutoshi; Hama, Masakatsu; Akiba, Syunichi; Koike, Kenzo; Okisaka, Koichi; Hagura, Toyoki; Kamiya, Tetsuro; Tomita, Fusao (abril de 2006). «Foot odor due to microbial metabolism and its control». Canadian Journal of Microbiology. 52 (4): 357–364. PMID 16699586. doi:10.1139/w05-130
- ↑ a b Jackson, Ron S. (2008). Wine Science: Principles and Applications 3rd ed. [S.l.]: Academic Press. p. 495. ISBN 9780123736468. Consultado em 22 de dezembro de 2012
- ↑ a b Kirk-Othmer (2007). «Wine». Food and Feed Technology, Volume 2. [S.l.]: John Wiley & Sons. p. 702. ISBN 9780470174487. Consultado em 22 de dezembro de 2012
- ↑ a b Oliver, Garrett, ed. (2012). The Oxford Companion to Beer. [S.l.]: Oxford University Press. p. 498. ISBN 9780195367133. Consultado em 22 de dezembro de 2012
- ↑ Lee IY, Nissen SL, Rosazza JP (1997). «Conversion of beta-methylbutyric acid to beta-hydroxy-beta-methylbutyric acid by Galactomyces reessii» (PDF). Applied and Environmental Microbiology. 63 (11): 4191–5. PMC 168736
 . PMID 9361403. doi:10.1128/AEM.63.11.4191-4195.1997. Consultado em 1 de setembro de 2020. Cópia arquivada (PDF) em 3 de setembro de 2020
. PMID 9361403. doi:10.1128/AEM.63.11.4191-4195.1997. Consultado em 1 de setembro de 2020. Cópia arquivada (PDF) em 3 de setembro de 2020